Všeobecná farmakológia. Farmakodynamika. Faktory ovplyvňujúce farmakokinetiku a farmakodynamiku. Klinický význam biotransformácie liečiva. Faktory ovplyvňujúce ich btotransformáciu. Metabolické liekové interakcie. Udržiavacie dávky, ich terapie
1. Koncepcia liečby ako riadená korekcia fyziologických porúch v tele. Výhody a riziká užívania liekov. Dôvody ich aplikácie. Hodnotenie bezpečnosti.
Farmakológia – teoretický základ farmakoterapia.
Dôvody užívania drog:
1) na nápravu a odstránenie príčiny ochorenia
2) v prípade nedostatočných preventívnych opatrení
3) zo zdravotných dôvodov
4) zjavná potreba založená na úrovni vedomostí a skúseností
5) snaha o zlepšenie kvality života
Výhody pri predpisovaní liekov:
1) korekcia alebo odstránenie príčiny ochorenia
2) zmiernenie príznakov ochorenia, ak nie je možné ho liečiť
3) nahradenie liečivých látok prírodnými biologicky aktívnymi látkami, ktoré organizmy neprodukujú v dostatočnom množstve
4) implementácia prevencie chorôb (vakcíny atď.)
Riziko- pravdepodobnosť, že v dôsledku expozície dôjde k poškodeniu alebo poškodeniu; sa rovná pomeru počtu nežiaducich (averzívnych) udalostí k veľkosti rizikovej skupiny.
A) neprijateľné (škoda> prospech)
B) prijateľné (výhoda> škoda)
B) nevýznamné (105 - bezpečnostný stupeň)
D) pri vedomí
Hodnotenie bezpečnosti liekov sa začína na úrovni chemických laboratórií syntetizujúcich lieky. Predklinické hodnotenie bezpečnosti lieku vykonáva Ministerstvo zdravotníctva, FDA atď. Ak liek úspešne prejde tejto fáze, začína sa jeho klinické hodnotenie, ktoré pozostáva zo štyroch fáz: I. fáza - hodnotenie tolerancie na zdravých dobrovoľníkoch vo veku 20-25 rokov, II. veľké skupiny ľudí (do 1000 osôb), IV fáza - sledovanie lieku počas 5 rokov po jeho oficiálnom schválení. Ak liek úspešne prejde všetkými týmito fázami, považuje sa za bezpečný.
2. Podstata farmakológie ako vedy. Sekcie a odbory modernej farmakológie. Hlavné pojmy a pojmy farmakológie sú farmakologická aktivita, pôsobenie, účinnosť chemikálií.
Farmakológia- veda o liekoch vo všetkých aspektoch - teoretický základ terapie:
A) veda o interakcii chemikálií so živými systémami
B) veda o riadení životne dôležitých procesov tela pomocou chemikálií.
Časti modernej farmakológie:
1) Farmakodynamika- študuje a) vplyv liekov na ľudský organizmus, b) vzájomné pôsobenie rôznych liekov v organizme pri ich predpisovaní, c) vplyv veku a rôznych chorôb na účinok liekov
2) Farmakokinetika- študuje absorpciu, distribúciu, metabolizmus a vylučovanie liekov (t. j. ako telo pacienta reaguje na lieky)
3) Farmakogenetika- študuje úlohu genetických faktorov pri vytváraní farmakologickej odpovede organizmu na lieky
4) Farmakoekonomika- zhodnotí výsledky užívania a náklady na lieky pre rozhodnutie o ich následnom praktickom použití
5) Farmakoepidemiológia- študuje užívanie drog a ich účinky na úrovni populácie alebo veľkých skupín ľudí s cieľom zabezpečiť užívanie najúčinnejších a najbezpečnejších liekov
Farmakologická (biologická) aktivita- vlastnosť látky spôsobovať zmeny v biosystéme (ľudskom tele). Farmakologické látky = biologicky aktívne látky (BAS)
farmakologický účinok- vplyv drog na objekt a jeho ciele
Farmakologický účinok- výsledok pôsobenia látky v organizme (úprava fyziologických, biochemických procesov, morfologických štruktúr) - kvantitatívna, nie však kvalitatívna zmena stavu biosystémov (buniek, tkanív, orgánov).
Účinnosť liekov- schopnosť liekov vyvolať v organizme určité farmakologické účinky nevyhnutné v tomto prípade. Posúdené na základe „podstatných dôkazov“ – adekvátne dobre kontrolované štúdie a klinické štúdie vykonávané odborníkmi s primeraným vedeckým vzdelaním a skúsenosťami vo výskume liekov tohto typu (FDA)
3. Chemická podstata liečiv. Faktory poskytujúce terapeutický účinok lieky- farmakologický účinok a placebové účinky.
Existujú lieky 1) rastlinné 2) živočíšne 3) mikrobiálne 4) minerálne 5) syntetické
Syntetické lieky sú zastúpené takmer všetkými triedami chemických zlúčenín.
farmakologický účinok- vplyv drog na objekt a jeho cieľ.
Placebo- akákoľvek zložka terapie, ktorá nemá žiadny špecifický biologický účinok na ochorenie, ktoré je predmetom liečby.
Používa sa na účely kontroly pri hodnotení účinku liekov a v prospech pacienta bez akýchkoľvek farmakologických látok v dôsledku iba psychického vplyvu (t.j. Placebo efekt).
Všetky typy liečby majú psychologickú zložku alebo uspokojujúcu ( Placebo efekt) alebo znepokojujúce ( Nocebo efekt). Príklad placebo efektu: rýchle zlepšenie u pacienta s vírusovou infekciou pri užívaní antibiotík, ktoré nepôsobia na vírusy.
Prínos placebo efektu súvisí s psychologickým dopadom na pacienta. Maximálny bude len pri jeho používaní. V kombinácii s liečebnými metódami ktoré majú výrazný špecifický účinok. Drahé látky ako placebo tiež pomáhajú dosiahnuť väčšiu odozvu.
Indikácie pre použitie placeba:
1) slabé duševné poruchy
2) psychologická podpora pre pacienta s nevyliečiteľnou chronickou chorobou alebo s podozrením na zložitú diagnózu
4. Zdroje a štádiá tvorby drog. Vymedzenie pojmov liečivá látka, liek, liek a lieková forma. Názov liekov.
Zdroje tvorby drog:
A) prírodné suroviny: rastliny, zvieratá, minerály atď. (srdcové glykozidy, bravčový inzulín)
B) modifikované prírodné biologicky aktívne látky
B) syntetické zlúčeniny
D) produkty genetického inžinierstva (rekombinantný inzulín, interferóny)
Etapy výroby lieku:
1. Syntéza liečiv v chemickom laboratóriu
2. Predklinické hodnotenie aktivity a nežiaducich účinkov liečiv MZ a iných organizmov
3. Klinické skúšky liekov (podrobnejšie pozri časť 1)
Medicína- akákoľvek látka alebo produkt používaný na úpravu alebo vyšetrenie fyziologických systémov alebo patologických stavov v prospech príjemcu (podľa WHO, 1966); jednotlivé látky, zmesi látok alebo kompozície neznámeho zloženia s preukázanými liečivými vlastnosťami.
Liečivá látka- jednotlivá chemická zlúčenina používaná ako liečivo.
Lieková forma- vhodné pre praktické uplatnenie forma podávaná liečivu na dosiahnutie požadovaného terapeutického alebo profylaktického účinku.
Liečivo- liek v určitej liekovej forme schválený orgánom štátnej správy.
5. Cesty podávania liečiva do organizmu a ich charakteristika. Presystémová eliminácia liekov.
1. Na systémové pôsobenie
A. Enterálny spôsob podávania: orálny, sublingválny, bukálny, rektálny, trubicový
B. Parenterálny spôsob podávania: intravenózne, subkutánne, intramuskulárne, inhalačné, subarachnoidálne, transdermálne
2. Pre lokálnu expozíciu: kožné (epikutárne), na slizniciach, v dutine (brušnej, pleurálnej, kĺbovej), v tkanive (infiltrácia)
|
Spôsob podávania lieku |
Dôstojnosť |
nevýhody |
|
Orálne - ústami |
1. Pohodlné a jednoduché pre pacienta 2. Sterilita liekov sa nevyžaduje |
1. Absorpcia mnohých liekov závisí od príjmu potravy, funkčného stavu gastrointestinálneho traktu a ďalších faktorov, ktoré sa v praxi takmer nezohľadňujú 2. Nie všetky lieky sa v tráviacom trakte dobre vstrebávajú 3. Niektoré lieky sa ničia v žalúdku (inzulín, penicilín) 4. Časť lieku má NLR na sliznici tráviaceho traktu (NSAID - slizničné prejavy, antacidá - potláčajú motoriku) 5. Neaplikovateľné pre pacientov v bezvedomí a so zhoršeným prehĺtaním |
|
Sublingválne a bukálne |
1. Pohodlný a rýchly úvod 2. Rýchla absorpcia liečiv 3. Lieky nepodliehajú presystémovej eliminácii 4. Pôsobenie lieku možno rýchlo prerušiť |
1. Nepríjemnosti spôsobené častým pravidelným užívaním tabletiek 2. Podráždenie ústnej sliznice, nadmerné slinenie, uľahčenie prehĺtania liekov a zníženie jeho účinnosti 3. Zlý vkus |
|
Rektálne |
1. Polovica liekov nepodlieha presystémovému metabolizmu 2. Sliznica tráviaceho traktu nie je podráždená 3. Vhodné, keď sú iné spôsoby podania neprijateľné (vracanie, kinetóza, dojčatá) 4. Miestna akcia |
1. Nepríjemné psychické momenty pre pacienta 2. Absorpcia liekov sa výrazne spomalí pri nevyprázdnení konečníka. |
|
Intravaskulárne (zvyčajne intravenózne). |
1. Rýchly vstup do krvného obehu (núdzové stavy) 2. Rýchla tvorba vysokej systémovej koncentrácie a schopnosť ju zvládať 3. Umožňuje zavedenie liekov, ktoré sú zničené v gastrointestinálnom trakte |
1. Technické ťažkosti intravaskulárneho prístupu 2. Riziko infekcie v mieste vpichu 3. Žilová trombóza v mieste vpichu liekov (erytromycín) a bolesť (chlorid draselný) 4. Niektoré lieky sa adsorbujú na stenách kvapkadiel (inzulín) |
|
Intramuskulárne |
Dostatočne rýchla absorpcia liečiva do krvi (10-30 min) |
Riziko lokálnych komplikácií |
|
Subkutánne |
1. Pacient si môže po tréningu podať injekciu samostatne. 2. Dlhodobý účinok liekov |
1. Pomalá absorpcia a prejav účinku lieku 2. Atrofia tukového tkaniva v mieste vpichu a zníženie rýchlosti absorpcie liekov |
|
Inhalácia |
1. Rýchly nástup účinku a vysoká koncentrácia v mieste vpichu pri liečbe ochorení dýchacích ciest. spôsoby 2. Dobrá ovládateľnosť akcie 3. Zníženie toxických systémových účinkov |
1. Potreba špeciálneho zariadenia (inhalátora) 2. Ťažkosti pri používaní tlakových aerosólov u niektorých pacientov |
|
Miestny PM |
1. Vysoká účinná koncentrácia liečiv v mieste vpichu 2. Zabráni sa nežiaducim systémovým účinkom tohto lieku |
Ak je narušená celistvosť kože, liek sa môže dostať do systémového obehu - prejav nežiaducich systémových účinkov. |
Presystémová eliminácia liekov (first pass effect)- proces biotransformácie liečiva predtým, ako sa liečivo dostane do systémového obehu. Na presystémovej eliminácii pri perorálnom podaní liečiva sa podieľajú enzymatické systémy čreva, portálnej žilovej krvi a hepatocytov.
Pri intravenóznom podaní nedochádza k presystémovej eliminácii.
Aby malo perorálne užívané liečivo priaznivý účinok, je potrebné zvýšiť jeho dávku, aby sa kompenzovali straty.
6. Transport liečiv cez biologické bariéry a jeho odrody. Hlavné faktory ovplyvňujúce transport liečiv v tele.
Spôsoby absorpcie (transportu) liečiv cez biologické membrány:
1) Filtrácia (difúzia vody) - pasívny pohyb molekúl látok po koncentračnom gradiente cez póry vyplnené vodou v membráne každej bunky a medzi susednými bunkami, typický pre vodu, niektoré ióny, malé hydrofilné molekuly (močovina).
2) Pasívna difúzia (lipidová difúzia) je hlavným mechanizmom prenosu liečiva, procesom rozpúšťania liečiva v membránových lipidoch a pohybu cez ne.
3) Transport pomocou špecifických nosičov - prenos liečiva pomocou nosičov zabudovaných v membráne (zvyčajne proteínov) je charakteristický pre hydrofilné polárne molekuly, množstvo anorganických iónov, cukrov, aminokyselín, pyrimidínov:
a) uľahčená difúzia – uskutočňuje sa pozdĺž koncentračného gradientu bez spotreby ATP
b) aktívny transport - proti koncentračnému gradientu s nákladmi na ATP
Saturovateľný proces - to znamená, že rýchlosť absorpcie sa zvyšuje len dovtedy, kým sa počet molekúl liečiva nerovná počtu nosičov.
4) Endocytóza a pinocytóza – liek sa naviaže na špeciálnu rozpoznávaciu zložku bunkovej membrány, dôjde k invaginácii membrány a vytvorí sa vezikula obsahujúca molekuly lieku. Následne sa liečivo uvoľní z vezikuly do bunky alebo transportuje von z bunky. Typické pre polypeptidy s vysokou molekulovou hmotnosťou.
Faktory ovplyvňujúce transport liečiv v tele:
1) fyzikálne a chemické vlastnosti látky (hydro- a lipofilita, ionizácia, polarizovateľnosť, veľkosť molekúl, koncentrácia)
2) štruktúra transferových bariér
3) prietok krvi
7. Transport liečivých látok s premenlivou ionizáciou cez membrány (Henderson-Hasselbalchova ionizačná rovnica). Princípy riadenia prenosu.
Všetky lieky sú slabé kyseliny alebo slabé zásady, ktoré majú svoje vlastné hodnoty ionizačnej konštanty (pK). Ak sa hodnota pH média rovná hodnote pK liečiva, potom 50 % jeho molekúl bude v ionizovanom stave a 50 % v neionizovanom stave a médium pre liečivo bude neutrálne.
V kyslom prostredí (pH menšie ako pK), kde je nadbytok protónov, bude slabá kyselina v nedisociovanej forme (R-COOH), t.j. bude naviazaná na protón - protónovaná. Táto forma kyseliny je bez náboja a je ľahko rozpustná v lipidoch. Ak sa pH posunie na alkalickú stranu (tj pH sa stane vyšším ako pK), potom kyselina začne disociovať a strácať protón, prechádzajúc do neprotónovanej formy, ktorá má náboj a je slabo rozpustná v lipidoch. .
V alkalickom prostredí, kde je nedostatok protónov, bude slabá báza v nedisociovanej forme (R-NH2), to znamená, že bude neprotónovaná a bez náboja. Táto forma bázy je vysoko rozpustná v tukoch a rýchlo sa vstrebáva. V kyslom prostredí je nadbytok protónov a slabá zásada sa začne disociovať, pričom viaže protóny a vytvára protónovanú nabitú formu zásady. Táto forma je slabo rozpustná v lipidoch a slabo absorbovaná.
teda Absorpcia slabých kyselín prebieha hlavne v kyslom prostredí a slabých zásad v alkalickom prostredí.
Vlastnosti metabolizmu slabých kyselín (SC):
1) žalúdok: SA v kyslom obsahu žalúdka nie je ionizovaný a v alkalickom prostredí tenkého čreva sa disociuje a molekuly SA získajú náboj. Preto bude absorpcia slabých kyselín najintenzívnejšia v žalúdku.
2) v krvi je médium dostatočne zásadité a absorbované molekuly SC sa premenia na ionizovanú formu. Filter renálneho glomerulu umožňuje prechod ionizovaných aj neionizovaných molekúl, preto sa napriek náboju molekuly SC vylúči do primárneho moču
3) ak je moč alkalický, potom kyselina zostane v ionizovanej forme, nebude sa môcť reabsorbovať späť do krvného obehu a bude sa vylučovať močom; Ak je moč kyslý, potom liek prejde do neionizovanej formy, ktorá sa ľahko reabsorbuje späť do krvi.
Vlastnosti metabolizmu slabých zásad: oproti SC (v čreve sa lepšie vstrebáva, v alkalickom moči sa reabsorbuje)
to., Na urýchlenie vylučovania slabej kyseliny z tela je potrebné alkalizovať moč a na urýchlenie vylučovania slabej zásady okysliť (detoxikácia podľa Popova).
Kvantitatívna závislosť procesu ionizácie liečiva pri rôznych hodnotách pH média umožňuje získať rovnicu Henderson— Hasselbach:
Kde pKa zodpovedá hodnote pH, pri ktorej sú koncentrácie ionizovaných a neionizovaných foriem v rovnováhe .
Henderson-Hasselbachova rovnica umožňuje odhadnúť stupeň ionizácie liečiva pri danej hodnote pH a predpovedať pravdepodobnosť jeho prieniku cez bunkovú membránu.
(1)Pre zriedenú kyselinu A,
HA ↔ H + + A -, kde HA je koncentrácia neionizovanej (protónovanej) formy kyseliny a A - je koncentrácia ionizovanej (neprotónovanej) formy.
(2) Pre slabá základňa, B,
BH + ↔ H + + B, kde BH + je koncentrácia protónovanej formy bázy, B je koncentrácia neprotónovanej formy
Pri znalosti pH média a pKa látky je možné z vypočítaného logaritmu určiť stupeň ionizácie liečiva, a teda stupeň jeho absorpcie z gastrointestinálneho traktu, reabsorpcie alebo vylučovania obličkami pri rôznych hodnoty pH moču atď.
8. Prenos liečiv v organizme. Difúzia vody a difúzia v lipidoch (Fickov zákon). Aktívna doprava.
Prenos liečiv v tele sa môže uskutočňovať difúziou vody a lipidov, aktívnym transportom, endo- a pinocytózou.
Vlastnosti prenosu liečiv v tele difúziou vody:
1. Epitelové vrstvy (sliznice tráviaceho traktu, ústna dutina a pod.) - difúzia vody len veľmi malých molekúl (metanol, ióny lítia a pod.)
2. Kapiláry (okrem mozgových) - filtrácia látok s molekulovou hmotnosťou do 20-30 tis.. Áno.
3. Kapiláry mozgu - v zásade nemajú vodné póry, s výnimkou oblastí hypofýzy, epifýzy, komory IV zóny, plexus choroideus, eminencia mediánu
4. Placenta – nemá žiadne vodné póry (hoci táto otázka je kontroverzná).
5. Väzba liečiv na krvné bielkoviny bráni ich výstupu z krvného obehu, a tým aj difúzii vody
6. Difúzia vo vode závisí od veľkosti molekúl liečiva a vodných pórov
Vlastnosti lipidovej difúzie:
1. Hlavný mechanizmus prenosu liečiva cez bunkové membrány
2. Určená lipofilitou difúznej látky (t. j. distribučným koeficientom „olej/voda“) a koncentračným gradientom, môže byť obmedzená veľmi nízkou rozpustnosťou látky vo vode (ktorá zabraňuje prenikaniu liečiva do vodná fáza membrán)
3. Nepolárne zlúčeniny ľahko difundujú, ióny ťažko difundujú.
Akákoľvek difúzia (voda aj lipidy) sa riadi Fickovým zákonom difúzie:
Rýchlosť difúzie - počet molekúl liečiva prenášaných za jednotku času; C1 je koncentrácia látky mimo membrány; C2 je koncentrácia látky zvnútra membrány.
Dôsledok Fickovho zákona:
1) filtrácia liečiva je tým vyššia, čím väčšia je jeho koncentrácia v mieste vpichu (S absorbovaného povrchu v čreve je väčšie ako v žalúdku, preto je absorpcia liečiva do čreva rýchlejšia)
2) čím vyššia je koncentrácia liečiva v mieste vpichu, tým vyššia je filtrácia liečiva
3) filtrácia liečiv je tým vyššia, čím menšia je hrúbka biologickej membrány, ktorá sa má prekonať (hrúbka bariéry v pľúcnych alveolách je oveľa menšia ako hrúbka kože, preto je rýchlosť absorpcie vyššia v pľúca)
Aktívna doprava- prenos liečiv bez ohľadu na koncentračný gradient s využitím energie ATP je charakteristický pre hydrofilné polárne molekuly, množstvo anorganických iónov, cukrov, aminokyselín, pyrimidínov. Charakterizované: a) selektivita pre určité zlúčeniny b) možnosť konkurencie dvoch látok pre jeden transportný mechanizmus c) saturácia pri vysokých koncentráciách látky d) možnosť transportu proti koncentračnému gradientu e) spotreba energie.
9. Centrálnym postulátom farmakokinetiky je koncentrácia liečiva v krvi – hlavný parameter na kontrolu terapeutického účinku. Problémy riešené na základe poznania tohto postulátu.
Centrálny postulát (dogma) farmakokinetiky: koncentrácia liečiv v krvnej plazme určuje (kvantitatívne určuje) farmakologický účinok.
Vo väčšine prípadov je rýchlosť absorpcie, distribúcie, metabolizmu a vylučovania liečiv úmerná ich koncentrácii v krvnej plazme (podriaďuje sa zákonu hromadného pôsobenia), takže je možné:
1) určiť polčas rozpadu (pre lieky s kinetikou prvého rádu)
2) vysvetliť trvanie niektorých toxických účinkov liekov (pre lieky v vysoké dávky s kinetikou nasýtenia)
10. Biologická dostupnosť liečiv - definícia, podstata, kvantitatívne vyjadrenie, determinanty. Biologická dostupnosť
Biologická dostupnosť (F) – charakterizuje úplnosť a rýchlosť absorpcie liekov s extrasystémovými cestami podania – odráža množstvo nezmenenej látky, ktoré sa dostalo do systémového obehu, v pomere k počiatočnej dávke lieku.
F je 100 % pre lieky, ktoré sa podávajú intravenózne. Pri podávaní inými cestami je F zvyčajne menej v dôsledku neúplnej absorpcie a čiastočného metabolizmu v periférnych tkanivách. F je 0, ak sa liek neabsorbuje z lumen gastrointestinálneho traktu.
Na odhadnutie F sa vynesie krivka ako funkcia koncentrácie liečiva v krvi v závislosti od času po jeho intravenóznom podaní, ako aj po podaní skúmanou cestou. Ide o tzv. farmakokinetické krivky vzťahu „čas-koncentrácia“. Plocha pod farmakokinetickou krivkou sa zistí integráciou a F sa vypočíta ako pomer:
![]() ≤ 1, kde AUC je plocha pod krivkou
≤ 1, kde AUC je plocha pod krivkou
Biologická dostupnosť > 70 % sa považuje za vysokú, pod 30 % za nízku.
Determinanty biologickej dostupnosti:
1) rýchlosť odsávania
2) úplnosť absorpcie - nedostatočné vstrebávanie liečiv pre ich veľmi vysokú hydrofilitu alebo lipofilitu, metabolizmus črevnými baktériami pri enterálnom podaní a pod.
3) presystémová eliminácia – pri vysokej biotransformácii v pečeni sú F lieky nízke (nitroglycerín pri perorálnom podaní).
4) lieková forma - sublingválne tablety a rektálne čapíky pomáhajú liekom vyhnúť sa presystémovej eliminácii.
11. Distribúcia liečiv v organizme. Oddiely, ligandy. Hlavné determinanty distribúcie.
Distribúcia Drogy - proces šírenia liekov cez orgány a tkanivá po ich vstupe do systémového obehu.
Distribučné polia:
1. Extracelulárny priestor (plazma, medzibunková tekutina)
2. Bunky (cytoplazma, membrána organel)
3. Tukové a kostné tkanivo (ukladanie liečiv)
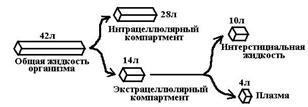 U osoby s hmotnosťou 70 kg je objem tekutého média celkovo 42 litrov, potom ak:
U osoby s hmotnosťou 70 kg je objem tekutého média celkovo 42 litrov, potom ak:
[Vd = 3-4 l, potom sa všetok liek distribuuje do krvi;
[Vd = 4-14 l, potom je všetko liečivo distribuované v extracelulárnej tekutine;
[Vd = 14-42 l, potom je všetka droga približne rovnomerne rozložená v tele;
[Vd> 42 L, potom sa všetko liečivo nachádza hlavne v extracelulárnom priestore.
Molekulové ligandy liečiv:
A) špecifické a nešpecifické receptory
B) krvné bielkoviny (albumín, glykoproteín) a tkanivá
C) polysacharidy spojivového tkaniva
D) nukleoproteíny (DNA, RNA)
Distribučné determinanty:
· Povaha drog- čím menšia je veľkosť molekuly a čím je liečivo lipofilnejšie, tým je jeho distribúcia rýchlejšia a rovnomernejšia.
· Veľkosť orgánu- čím väčší je orgán, tým viac drogy sa doň môže dostať bez výrazná zmena koncentračný gradient
· Prietok krvi orgánom- v dobre prekrvených tkanivách (mozog, srdce, obličky) sa terapeutická koncentrácia látky vytvorí oveľa skôr ako v slabo prekrvených tkanivách (tuk, kosti)
· Prítomnosť histohematogénnych bariér- lieky ľahko prenikajú do tkanív so slabo exprimovaným GHB
· Väzba na plazmatické bielkoviny- čím väčšia je naviazaná frakcia liečiva, tým horšia je jeho distribúcia v tkanive, pretože kapiláru môžu opustiť iba voľné molekuly.
· Ukladanie liečiva v tkanivách- väzba liečiv na tkanivové proteíny prispieva k jeho akumulácii v nich, pretože koncentrácia voľných liečiv v perivaskulárnom priestore klesá a medzi krvou a tkanivami sa neustále udržiava vysoký koncentračný gradient.
Kvantitatívna charakteristika distribúcie liečiva je zdanlivý distribučný objem (Vd).
Zdanlivý distribučný objemVd Je hypotetický objem tekutiny, v ktorom môže byť rozdelená celá podaná dávka liečiva, aby sa vytvorila koncentrácia rovnajúca sa koncentrácii v krvnej plazme.
Vd sa rovná pomeru podanej dávky (celkového množstva liečiva v tele) k jeho koncentrácii v krvnej plazme:
 .
.
Čím väčší je zdanlivý distribučný objem, tým viac liečiv sa distribuuje do tkaniva.
12. Eliminačná konštanta, jej podstata, rozmer, vzťah s ostatnými farmakokinetickými parametrami.
Konštanta rýchlosti eliminácie(kel, min-1) - ukazuje, aká časť liekov sa z tela vylúči za jednotku času Þ Kel = Avid / Atot, kde Avid je množstvo uvoľnených liekov v jednotkách. čas, generál - celková suma Drogy v tele.
Hodnota kel sa zvyčajne zistí riešením farmakokinetickej rovnice opisujúcej proces eliminácie liečiva z krvi, preto sa kel nazýva modelový kinetický index. Kel priamo nesúvisí s plánovaním dávkovacieho režimu, ale jeho hodnota sa používa na výpočet iných farmakokinetických parametrov.
Eliminačná konštanta je priamo úmerná klírensu a nepriamo úmerná distribučnému objemu (z definície klírensu): Kel = CL / Vd; = hodina-1 / min-1 = zlomok za hodinu.
13. Polčas rozpadu liečiv, jeho podstata, rozmer, vzťah s ostatnými farmakokinetickými parametrami.
Polovičné eliminačné obdobie(t½, min) je čas potrebný na zníženie koncentrácie liečiva v krvi presne o polovicu. V tomto prípade nezáleží na tom, akým spôsobom sa dosiahne zníženie koncentrácie - pomocou biotransformácie, vylučovania alebo vďaka kombinácii oboch procesov.
Polčas je určený vzorcom:
![]()
Polčas je najdôležitejším farmakokinetickým parametrom, ktorý umožňuje:
B) určiť čas úplného vylúčenia lieku
C) predpovedať koncentráciu liečiv kedykoľvek (pre liečivá s kinetikou prvého poriadku)
14. Klírens ako hlavný farmakokinetický parameter na riadenie dávkovacieho režimu. Jeho podstata, rozmer a vzťah s ostatnými farmakokinetickými parametrami.
Odbavenie(Cl, ml / min) - objem krvi, ktorý sa vyčistí z liekov za jednotku času.
Keďže plazma (krv) je „viditeľná“ časť distribučného objemu, klírens je zlomok distribučného objemu, z ktorého sa liek uvoľní za jednotku času. Ak označíme celkové množstvo liečiva v organizme cez generál a suma, ktorá bola pridelená po Avyd, potom:
![]() Na druhej strane z definície distribučného objemu vyplýva, že celkové množstvo liečiva v organizme je Absh =Vd´
CTer / plazma... Nahradením tejto hodnoty do vzorca vôle dostaneme:
Na druhej strane z definície distribučného objemu vyplýva, že celkové množstvo liečiva v organizme je Absh =Vd´
CTer / plazma... Nahradením tejto hodnoty do vzorca vôle dostaneme:
![]() .
.
Klírens je teda pomer rýchlosti eliminácie liečiva k jeho koncentrácii v krvnej plazme.
V tejto forme sa klírensový vzorec používa na výpočet udržiavacej dávky lieku ( DNS), t.j. dávka lieku, ktorá by mala kompenzovať stratu lieku a udržiavať jeho hladinu na konštantnej úrovni:
Injekčná rýchlosť = rýchlosť vylučovania =Cl´ CTer(dávka/min)
DNS= rýchlosť vstrekovania´ T (T- interval medzi užitím lieku)
Svetlá výška je aditívna, teda k vylučovaniu látky z tela môže dôjsť za účasti procesov v obličkách, pľúcach, pečeni a iných orgánoch: Clsystem = Clrenal. + Cl pečeň + Cld.
Povolenie viazané S polčasom rozpadu lieku a distribučným objemom: t1/2 = 0,7 * Vd / Cl.
15. Dávka. Druhy dávok. Jednotky dávkovania lieku. Ciele dávkovania liečiva, spôsoby a možnosti podávania, interval podávania.
Účinok liekov na telo je do značnej miery určený ich dávkou.
Dávka- množstvo látky zavedenej do tela naraz; vyjadrené v hmotnosti, objeme alebo konvenčných (biologických) jednotkách.
Typy dávok:
A) jednorazová dávka – množstvo látky na dávku
B) denná dávka - množstvo lieku predpísané na deň v jednej alebo viacerých dávkach
C) kurzová dávka - celkové množstvo liečiva na priebeh liečby
D) terapeutické dávky - dávky, v ktorých sa liek používa na terapeutické alebo profylaktické účely (prahové, alebo minimálne účinné, priemerné terapeutické a vyššie terapeutické dávky).
E) toxické a smrteľné dávky - dávky liekov, pri ktorých začínajú mať výrazné toxické účinky alebo spôsobujú smrť tela.
E) nasycovacia (úvodná) dávka - počet vstreknutých liečiv, ktorý vyplní celý distribučný objem organizmu v efektívnej (terapeutickej) koncentrácii: VD = (Css * Vd) / F
G) udržiavacia dávka - systematicky podávané množstvo liečiva, ktoré kompenzuje stratu liečiva s klírensom: PD = (Css * Cl * DT) / F
Farmaceutické dávkové jednotky:
1) v gramoch alebo zlomkoch gramu liečiva
2) počet liekov na 1 kg telesná hmotnosť (napríklad 1 Mg/kg) alebo na jednotku plochy tela (napríklad 1 Mg/m2)
Ciele dávkovania liekov:
1) určiť množstvo liekov potrebné na dosiahnutie požadovaného terapeutického účinku s určitým trvaním
2) vyhnúť sa javom intoxikácie a vedľajším účinkom pri zavádzaní liekov
Spôsoby podávania liekov: 1) enterálne 2) parenterálne (pozri časť 5)
Možnosti podávania liekov:
A) kontinuálne (dlhodobou intravaskulárnou infúziou liečiv po kvapkách alebo prostredníctvom automatických dávkovačov). Pri kontinuálnom podávaní liekov sa jeho koncentrácia v organizme plynule mení a nepodlieha výraznejším výkyvom.
B) prerušované podávanie (injekčnými alebo neinjekčnými metódami) - podávanie lieku v pravidelných intervaloch (dávkovacie intervaly). Pri prerušovanom podávaní liekov jeho koncentrácia v organizme neustále kolíše. Po užití určitej dávky najskôr stúpa a potom postupne klesá, pričom pred ďalším podaním lieku dosahuje minimálne hodnoty. Kolísanie koncentrácie je tým výraznejšie, čím väčšia je podaná dávka liečiva a interval medzi injekciami.
Interval vstrekovania- interval medzi podávanými dávkami zabezpečujúci udržanie terapeutickej koncentrácie látky v krvi.
16. Podávanie liekov konštantnou rýchlosťou. Kinetika koncentrácie liečiva v krvi. Stacionárna koncentrácia liečiva v krvi ( Css), čas jeho dosiahnutia, výpočet a hospodárenie s ním.
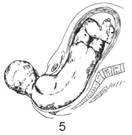 Zvláštnosťou zavádzania liekov konštantnou rýchlosťou je hladká zmena jeho koncentrácie v krvi po podaní, pričom:
Zvláštnosťou zavádzania liekov konštantnou rýchlosťou je hladká zmena jeho koncentrácie v krvi po podaní, pričom:
1) čas na dosiahnutie ustálenej koncentrácie liečiva je 4-5 t½ a nezávisí od rýchlosti infúzie (veľkosti podanej dávky)
2) so zvýšením rýchlosti infúzie (vstreknutá dávka) sa hodnota СSS tiež zvyšuje proporcionálne
3) eliminácia lieku z tela po ukončení infúzie trvá 4-5 t½.
SSs- rovnovážna stacionárna koncentrácia- koncentrácia liečiv dosiahnutá pri rýchlosti podávania rovnajúcej sa rýchlosti vylučovania, preto:
![]() (z definície povolenia)
(z definície povolenia)
Pre každý nasledujúci polčas sa koncentrácia liečiva zvyšuje o polovicu zostávajúcej koncentrácie. Všetky lieky, ktoré dodržiavajú zákon o eliminácii prvého poriadku, sú DosiahneCsspo 4-5 polčasoch rozpadu.
Manažérske prístupy úrovne CSs: zmeniť podanú dávku lieku alebo interval podávania
17. Prerušované podávanie liekov. Kinetika koncentrácie liečiva v krvi, rozsah terapeutických a toxických koncentrácií. Výpočet stacionárnej koncentrácie ( CSs), hranice jeho kmitov a jeho ovládanie. Primeraný diskrétny interval dávkovania.
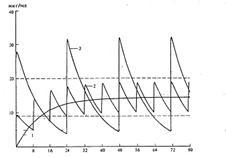 Kolísanie koncentrácie liečiv v krvnej plazme: 1 - s konštantným intravenóznym kvapkaním; 2 - s čiastočným zavedením rovnakej dennej dávky s intervalom 8 hodín; 3 - so zavedením dennej dávky s intervalom 24 hodín.
Kolísanie koncentrácie liečiv v krvnej plazme: 1 - s konštantným intravenóznym kvapkaním; 2 - s čiastočným zavedením rovnakej dennej dávky s intervalom 8 hodín; 3 - so zavedením dennej dávky s intervalom 24 hodín.
Prerušované podávanie lieku- zavedenie určitého množstva liekov v určitých intervaloch.
Rovnovážna koncentrácia v rovnovážnom stave sa dosiahne po 4-5 polovičných eliminačných periódach, čas na jej dosiahnutie nezávisí od dávky (na začiatku, keď je hladina koncentrácie liečiva nízka, je nízka aj rýchlosť jeho eliminácie; s narastajúcim množstvom látky v organizme sa zvyšuje aj rýchlosť jej vylučovania, preto skôr či neskoro príde okamih, keď zvýšená rýchlosť vylučovania vyrovná podanú dávku liečiva a ďalšie zvyšovanie koncentrácie sa zastaví)
Css je priamo úmerná dávke liečiva a nepriamo úmerná intervalu medzi injekciami a klírensom liečiva.
Hranice swingu CSS: ![]() ; Cssmin = Cssmax × (1 – email). Kolísanie koncentrácie liečiva je úmerné T/t1/2.
; Cssmin = Cssmax × (1 – email). Kolísanie koncentrácie liečiva je úmerné T/t1/2.
Terapeutický rozsah (bezpečnostná chodba, terapeutické okienko) Je rozsah koncentrácie od minimálneho terapeutického po spôsobujúci vzhľad prvé príznaky vedľajších účinkov.
Toxický rozsah- rozsah koncentrácie od najvyššej terapeutickej po smrteľnú.
Adekvátne podávanie oddelených dávok: spôsob podávania, pri ktorom kolísanie koncentrácie liečiva v krvi spadá do terapeutického rozsahu. Na určenie adekvátneho režimu podávania lieku je potrebné vypočítať. Rozdiel medzi Cssmax a Cssmin by nemal presiahnuť 2Css.
Ovládanie oscilácieCss:
Rozsah hojdačkyCsspriamo úmerná dávke liekov a nepriamo úmerná intervalu jej podávania.
1. Zmeňte dávku liekov: so zvyšovaním dávky liečiva sa úmerne zvyšuje rozsah kolísania jeho Css
2. Zmeňte interval podávania lieku: s predlžovaním intervalu podávania lieku úmerne klesá rozsah kolísania jeho Css
3. Súčasne zmeňte dávku a interval podávania
18. Úvodná (nasycovacia) dávka. Terapeutický význam, výpočet podľa farmakokinetických parametrov, podmienky a obmedzenia jeho použitia.
Úvodná (nasycovacia) dávka- dávka podaná naraz a vypĺňajúca celý distribučný objem v aktuálnej terapeutickej koncentrácii. VD = (Css * Vd) / F; = mg/l, = l/kg
Terapeutický význam: úvodná dávka rýchlo zabezpečí účinnú terapeutickú koncentráciu liečiva v krvi, čo umožňuje napríklad rýchlo zastaviť záchvat astmy, arytmie atď.
Úvodná dávka sa môže podať len vtedy, keď Proces distribúcie látky sa ignoruje
Obmedzenie používania VD: ak je liek distribuovaný Výrazne pomalší ako jeho vstup do krvného obehu, podanie celej nárazovej dávky naraz (najmä intravenózne) vytvorí koncentráciu výrazne vyššiu ako je terapeutická a spôsobí výskyt toxických účinkov. Podmienka používania VD: preto zavedenie nárazových dávok Malo by byť vždy pomalé alebo zlomkové.
19. Udržiavacie dávky, ich terapeutický význam a výpočet pre optimálny dávkovací režim.
Udržiavacia dávka- dávka liečiva podávaná systematicky, ktorá vypĺňa klírensový objem, to znamená fragment Vd, ktorý sa zbavuje liečiv počas intervalu DT: PD = (Css * Cl * DT) / F.
Terapeutický význam: PD kompenzuje straty klírensom počas intervalu medzi injekciami lieku.
Výpočet optimálneho dávkovania liekov (na rýchlu úľavu od záchvatu):
1. Vypočítajte VD: VD = (Css * Vd) / F
2. Vyberte interval injekcie DT (zvyčajne sa väčšina liekov predpisuje s intervalom blízkym t1 / 2) a vypočítajte AP: AP = (Css * Cl * DT) / F
3. Výpočtom Cssmax a Cssmin skontrolujte, či kolísanie liečiva v krvi nepresahuje terapeutický rozsah: ![]() ; Cssmin = Cssmax × (1 – email). Rozdiel medzi Cssmax a Cssmin by nemal presiahnuť dve Css.
; Cssmin = Cssmax × (1 – email). Rozdiel medzi Cssmax a Cssmin by nemal presiahnuť dve Css.
Časť, ktorá sa má odstrániť, sa zistí podľa grafu (pozri časť 16) alebo podľa vzorca: ![]()
4. Ak pri nami zvolenom intervale podávania lieku jeho výkyvy presahujú terapeutické rozmedzie, zmeňte DT a výpočet zopakujte (bod 2 - bod 4)
NB! Ak liek nie je určený na zmiernenie núdzových stavov alebo sa užíva v tabletkách, VD sa nevypočítava.
20. Individuálne, vekové a pohlavné rozdiely vo farmakokinetike liečiv. Opravy pre výpočet jednotlivých hodnôt pre objem distribúcie liekov.
1. Vekové rozdiely vo farmakokinetike liečiv.
|
1. Stratum corneum je tenšie, preto sa pri aplikácii na kožu liečivá lepšie vstrebávajú. Lepšia je aj absorpcia liekov rektálnym podaním. 2. Objem tekutín v tele detí je 70-80%, kým u dospelých len »60%, preto je Vd hydrofilných liečiv, ktoré majú, vyššie a sú potrebné vyššie dávky. 3. U novorodenca je hladina albumínu v plazme nižšia ako u dospelých, preto je u nich väzba liečiv na bielkoviny menej intenzívna. 4. Novorodenci majú nízku intenzitu systémov cytochrómu P450 a konjugujúcich enzýmov, ale vysokú aktivitu metylačných systémov. 5. Rýchlosť glomerulárnej filtrácie v obličkách detí mladších ako 6 mesiacov je 30-40% rýchlosti dospelých, preto sa znižuje renálna exkrécia liekov. |
1. Dochádza k poklesu koncentrácie albumínu v krvnej plazme a frakcie liečiva spojenej s proteínom 2. Obsah vody v tele klesá zo 60% na 45%, preto sa zvyšuje akumulácia lipofilných liečiv. 3. Rýchlosť glomerulárnej filtrácie môže klesnúť až o 50 – 60 % rýchlosti zrelého pacienta, preto je renálna eliminácia liekov výrazne obmedzená. |
2. Pohlavné rozdiely v pôsobení drog... Pre ženy je charakteristická nižšia telesná hmotnosť ako pre mužov, preto by veľkosť dávok lieku pre nich mala byť spravidla na spodnej hranici rozsahu terapeutických dávok.
3. Patologické stavy organizmu a účinok liekov
A) ochorenie pečene: F lieky v dôsledku odstavenia metabolizmu prvého prechodu, zlomok neviazaných liekov pre nedostatok syntézy albumínu, účinky liekov sa predlžujú v dôsledku ich biotransformácie.
B) patológia obličiek: spomaľuje sa vylučovanie liekov, ktoré sa vylučujú obličkami
4. Genetické faktory- nedostatok niektorých enzýmov metabolizmu liečiv môže prispieť k predĺženiu ich účinku (pseudocholinesteráza a pod.)
Opravy na výpočet jednotlivých hodnôt distribučného objemu liekov:
A) pri obezite sú lipofóbne liečivá nerozpustné v tukovom tkanive Þ je potrebné vypočítať ideálna hmotnosť podľa výšky (Brocov vzorec: ideálna hmotnosť = výška (v cm) - 100) a prepočítajte Vd podľa ideálnej hmotnosti na výšku.
B) pri opuchoch si treba vypočítať prebytočný objem vody = nadváha - ideálne, Vd treba zvýšiť o liter z každého nadbytočného kilogramu vody.
Závislosť hlavných farmakokinetických parametrov od rôznych faktorov:
1. Absorpcia liečiv: vekom ¯ absorpcia liečiva, jeho metabolizmus pri presystémovej eliminácii, mení sa biologická dostupnosť liečiv.
2. Distribučný objem Vd: ¯ s vekom as obezitou, s edémom
3. Polčas: mení sa s vekom a obezitou (keďže Vd klesá)
4. Klírens: určuje sa podľa funkčného stavu obličiek a pečene
21. Renálny klírens liečiv, mechanizmy, ich kvantitatívne a kvalitatívne charakteristiky.
Renálny klírens je miera objemu krvnej plazmy, ktorá sa vylúči z liečiva za jednotku času obličkami: Cl (ml/min) = U × V/P, kde U je koncentrácia liečiva v ml moču, V je objem vylúčeného moču v min a P = koncentrácia liečiva v ml plazmy.
Mechanizmy renálneho klírensu a ich vlastnosti:
1. Filtrácia: Uvoľňované drogy Iba filtrácia(inzulín) bude mať klírens rovný GFR (125-130 ml/min)
Určené: prietokom krvi obličkami, neviazanou frakciou liečiva a filtračnou kapacitou obličiek.
Väčšina liekov má nízku molekulovú hmotnosť, a preto sa voľne filtruje z plazmy v glomerulu.
2. Aktívna sekrécia: Uvoľňované drogy Filtrácia a celková sekrécia(kyselina paraaminogipurová), bude mať klírens rovný renálnemu plazmatickému klírensu (650 ml/min)
Obličkový tubul obsahuje dva dopravné systémy ktorý dokáže rozdeliť liečivá do ultrafiltrátu, jeden pre organické kyseliny a ďalší pre organické zásady. Tieto systémy vyžadujú energiu na aktívny transport proti koncentračnému gradientu; sú miestom súťaženia nosiča niektorých liekov s inými.
Určené podľa: maximálnej rýchlosti sekrécie, objemu moču
3. Reabsorpcia: hodnoty klírensu medzi 130 a 650 ml/min naznačujú, že liek je Filtrovaný, vylučovaný a čiastočne reabsorbovaný
Reabsorpcia prebieha v celom obličkovom kanáli a závisí od polarity liečiva, nepolárne, lipofilné sú reabsorbované.
Určené: primárnou hodnotou pH a ionizáciou liečiva
Množstvo ukazovateľov ako napr Vek, spoločné užívanie viacerých liekov, choroby významne ovplyvňujú renálny klírens:
A) zlyhanie obličiek ® zníženie klírensu liečiva vysoký stupeň Drogy v krvi
B) glomerulonefritída ® strata sérového proteínu, ktorý bol zvyčajne dostupný a spojený s liekmi ® zvýšenie hladiny voľnej frakcie liečiv v plazme
22. Faktory ovplyvňujúce renálny klírens liečiv. Závislosť klírensu od fyzikálno-chemických vlastností liečiv.
Faktory ovplyvňujúce obličkyCl:
A) glomerulárna filtrácia
B) rýchlosť prietoku krvi obličkami
B) maximálna rýchlosť sekrécie
D) objem moču
E) frakcia neviazaná v krvi
Závislosť renálneho klírensu od fyzikálno-chemických vlastností liečiv:
Všeobecné vzory: 1) polárne liečivá nie sú reabsorbované, nepolárne liečivá sú reabsorbované 2) iónové liečivá sú vylučované, neiónové liečivá nie sú secernované.
I. Nepolárne neiónové látky: filtrované len v neviazaných formách, nevylučované, reabsorbované
Renálny klírens je malý a je určený: a) podielom liečiva neviazaného v krvi b) objemom moču
II. Polárne neiónové látky: filtrované v neviazanej forme, nevylučujú sa, neabsorbujú sa
Renálny klírens je vysoký, určený: a) podielom liečiva neviazaného v krvi b) rýchlosťou glomerulárnej filtrácie
III. Nepolárne ionizované v moči v neiónovej forme: filtrované, aktívne vylučované, nepolárne reabsorbované
Renálny klírens je určený: a) podielom liečiva neviazaného v krvi b) podielom liečiv ionizovaného v moči c) objemom moču
IV. Polárne ionizované v moči v neionizovanej forme: filtrované, aktívne vylučované, neabsorbované
Renálny klírens je určený: a) prietokom krvi obličkami a rýchlosťou glomerulárnej filtrácie b) maximálnou rýchlosťou sekrécie
23. Pečeňový klírens liečiv, jeho determinanty a obmedzenia. Enterohepatálny liekový cyklus.
Mechanizmy hepatálneho klírensu:
1) metabolizmus (biotransformácia) oxidáciou, redukciou, alkyláciou, hydrolýzou, konjugáciou atď.
Hlavná stratégia metabolizmu xenobiotík: nepolárne látky ® polárne (hydrofilné) metabolity vylučované močom.
2) sekrécia (vylučovanie netransformovaných látok do žlče)
Do žlče sú transportované iba polárne látky s molekulovou hmotnosťou > 250 aktívne (organické kyseliny, zásady).
Determinanty hepatálneho klírensu:
A) Rýchlosť prietoku krvi v pečeni
B) Maximálna rýchlosť vylučovania alebo metabolických premien
B) Km - Michaelisova konštanta
D) Frakcia neviazaná na bielkoviny
Obmedzenia hepatálneho klírensu:
1. Ak je Vmax / Km veľké → Cl pecs = rýchlosť prietoku krvi v pečeni
2. Ak sú stredné hodnoty Vmax / Km → Cl = súčet všetkých faktorov
3. Ak je Vmax / Km malé → Cl pec je malá, obmedzená
Enterohepatálny liekový cyklus - Množstvo liečiv a produktov ich premeny sa vo významných množstvách vylučuje žlčou do čriev, odkiaľ sa čiastočne vylučujú exkrementmi a čiastočne - Reabsorbované do krvi, opäť vstupuje do pečene a vylučuje sa do čriev.
Vylučovanie liekov pečeňou sa môže výrazne zmeniť Choroby pečene, vek, strava, genetika, dĺžka predpisovania liekov(napríklad v dôsledku indukcie pečeňových enzýmov) a iných faktorov.
24. Faktory, ktoré menia klírens liečivých látok.
1. Liekové interakcie na úrovni: renálnej sekrécie, biochemickej transformácie, fenoménov enzymatickej indukcie
2. Ochorenie obličiek: poruchy prietoku krvi, akútne a chronické poškodenie obličiek, následky dlhodobého ochorenia obličiek
3. Ochorenia pečene: alkoholická cirhóza, primárna cirhóza, hepatitída, hepatómy
4. Choroby gastrointestinálneho traktu a endokrinných orgánov
5. Individuálna intolerancia (nedostatok acetylačných enzýmov - intolerancia aspirínu)
25. Korekcia medikamentóznej terapie pri ochoreniach pečene a obličiek. Všeobecné prístupy. Korekcia dávkovacieho režimu pod kontrolou celkového klírensu liečiva.
1. Zrušte lieky, ktoré nie sú potrebné
2. Pri ochorení obličiek užívajte lieky vylučované pečeňou a naopak.
3. Znížte dávku alebo predĺžte interval medzi injekciami
4. Dôkladné sledovanie vedľajších a toxických účinkov
5. Pri absencii farmakologického účinku sa dávka musí zvyšovať pomaly a pod kontrolou farmakologických a toxických účinkov.
6. Ak je to možné, stanovte koncentráciu látky v plazme a individuálne korigujte medikamentóznu Cl terapiu
7. Použite nepriamu metódu hodnotenia Cl.
Úprava dávkovacieho režimu pod kontrolou celkového klírensu lieku:
Úprava dávky : Dind = Dtyp. × Clind. / Cltyp.
Pri kontinuálnom intravenóznom podávaní lieku: Individuálna rýchlosť podávania = Typická rýchlosť podávania × Cl ind. / Cl typické
Pri prerušovanom podávaní: 1) zmeňte dávku 2) zmeňte interval 3) zmeňte oba parametre. Napríklad, ak sa klírens zníži o 50 %, môžete znížiť dávku o 50 % a dodržať interval, alebo zdvojnásobiť interval a ponechať dávku. Výhodnejšie je znížiť dávku a zachovať interval podávania.
26. Korekcia dávkovacieho režimu pod kontrolou zvyškovej funkcie obličiek.
Klírens kreatinínu- najdôležitejší kvantitatívny ukazovateľ funkcie obličiek, na základe ktorého je možné upraviť dávkovací režim
Vieme:
A) zvyšková funkcia obličiek stanovená klírensom kreatinínu u daného pacienta Clcr / pacienta
B) celkový klírens daného lieku (CLP / celkový) a podiel renálneho klírensu lieku na celkovom klírens
B) normálny klírens kreatinínu Clcr / normogram
3) Css a F pre túto sieť LAN (z referencie)
Nájsť: dávka lieku pre tohto pacienta
ClPP / renálna rýchlosť = ClPP / celkový X podiel renálneho klírensu liečiva na celkovom klírense
Сlp / renálny pacient = Clcr / pacient / Сlcr / norma * Clls / renálna norma
ClPP / nerenálna frekvencia = ClPP / celková - ClPP / renálna frekvencia
ClPS / všeobecný pacient = CLPS / renálny pacient + ClPS / nerenálna norma
Dávka tohto lieku vo vnútri s normálnou funkciou obličiek je: norma PD = Css X Cl / F
Dávka tohto lieku vo vnútri pre nášho pacienta sa rovná: PD pacienta = norma PD X СlPS / všeobecný pacient / СlPS / celkom
Odpoveď: PDbolný
27. Korekcia medikamentóznej terapie poškodenia pečene a iných patologických stavov.
Ochorenie pečene môže znížiť klírens a predĺžiť polčas mnohých liekov. Pri niektorých liekoch, ktoré sa vylučujú pečeňou, sa však tieto parametre v prípade dysfunkcie pečene nemenia Ochorenie pečene nie vždy ovplyvňuje vlastný hepatálny klírens... V súčasnosti neexistuje žiadny spoľahlivý marker, ktorý by sa dal použiť na predpovedanie hepatálneho klírensu podobného klírensu kreatinínu.
Úprava dávkovacieho režimu pri ochorení obličiek, pozri odsek 26 vyššie, všeobecné zásady oprava - v.25.
28. Stratégia individuálnej medikamentóznej terapie.
Uznanie dôležitej úlohy koncentrácie ako prepojenia medzi farmakokinetikou a farmakodynamikou prispieva k vytvoreniu stratégie cieľovej koncentrácie – optimalizovať dávku u daného pacienta na základe merania koncentrácie liečiva. Pozostáva z nasledujúcich etáp:
1. Voľba cieľovej koncentrácie
2. Vypočítajte Vd a Cl na základe typických hodnôt a vykonajte úpravy pre faktory, ako je telesná hmotnosť a funkcia obličiek.
3. Zadanie nasycovacej dávky alebo udržiavacej dávky vypočítanej s prihliadnutím na hodnoty TC, Vd a Cl.
4. Registrácia reakcie pacienta a stanovenie koncentrácie liečiva
5. Revízia Vd a Cl na základe výsledkov meraní koncentrácie.
6. Opakujte kroky 3-6, aby ste upravili udržiavaciu dávku potrebnú na optimálnu odpoveď na liek.
29. Biotransformácia liečiv, jej biologický význam, hlavný smer a vplyv na aktivitu liečiv. Hlavné fázy metabolických premien liečiv v tele.
Biotransformácia liečiv- chemické premeny liečiv v organizme.
Biologický význam biotransformácie liečiv: vytvorenie substrátu vhodného na následnú likvidáciu (ako energetický alebo plastový materiál) alebo na urýchlenie vylučovania liečiv z tela.
Hlavný smer metabolických premien liekov: nepolárne liečivá → polárne (hydrofilné) metabolity vylučované močom.
Existujú dve fázy metabolických reakcií liekov:
1) Metabolická transformácia (nesyntetické reakcie, fáza 1)- premena látok v dôsledku mikrozomálnej a extramikrozomálnej oxidácie, redukcie a hydrolýzy
2) konjugácia (syntetické reakcie, fáza 2)- biosyntetický proces sprevádzaný pridaním množstva chemických skupín alebo molekúl endogénnych zlúčenín k liečivu alebo jeho metabolitom a) tvorbou glukuronidov b) glycerolestermi c) sulfoestermi d) acetyláciou e) metyláciou
Vplyv biotransformácie na farmakologickú aktivitu liečiv:
1) biotransformačné metabolity najčastejšie nemajú farmakologickú aktivitu alebo je ich aktivita v porovnaní s pôvodnou látkou znížená
2) v niektorých prípadoch si metabolity môžu zachovať aktivitu a dokonca prekročiť aktivitu materskej látky (kodeín sa metabolizuje na farmakologicky aktívnejší morfín)
3) niekedy pri biotransformácii vznikajú toxické látky (metabolity izoniazidu, lidokaínu)
4) niekedy v priebehu biotransformácie vznikajú metabolity s opačnými farmakologickými vlastnosťami (metabolity neselektívnych agonistov b2-adrenergných receptorov majú vlastnosti blokátorov týchto receptorov)
5) mnohé látky sú proliečivá, ktoré spočiatku nevykazujú farmakologické účinky, ale v priebehu biotransformácie sa premieňajú na biologicky aktívne látky (neaktívna L-dopa, prenikajúca do BBB, sa v mozgu mení na aktívny dopamín, pričom žiadne systémové účinky dopamínu).
30. Klinický význam biotransformácie liečiva. Vplyv pohlavia, veku, telesnej hmotnosti, environmentálnych faktorov, fajčenia, alkoholu na biotransformáciu drog.
Klinický význam biotransformácie liečiva: keďže dávka a frekvencia podávania potrebné na dosiahnutie účinnej koncentrácie v krvi a tkanivách sa môžu u pacientov líšiť v dôsledku individuálnych rozdielov v distribúcii, rýchlosti metabolizmu a eliminácii liečiv, je dôležité ich brať do úvahy v klinickej praxi.
Vplyv rôznych faktorov na biotransformáciu liečiv:
A) Funkčný stav pečene: v prípade jej chorôb sa klírens liekov zvyčajne znižuje a polčas eliminácie sa zvyšuje.
b) Vplyv environmentálnych faktorov: fajčenie podporuje indukciu cytochrómu P450, v dôsledku čoho sa zrýchľuje metabolizmus liečiv pri mikrozomálnej oxidácii
V) Vegetariáni biotransformácia liečiv je spomalená
D) starší a mladí pacienti sa vyznačujú tým precitlivenosť na farmakologický alebo toxický účinok liekov (u starších ľudí a detí do 6 mesiacov je znížená aktivita mikrozomálnej oxidácie)
E) u mužov je metabolizmus niektorých liekov rýchlejší ako u žien, pretože androgény stimulujú syntézu mikrozomálnych pečeňových enzýmov (etanol)
E) Vysoký obsah bielkovín v jedle a intenzívna fyzická aktivita: zrýchlenie metabolizmu liečiv.
f) Alkohol a obezita spomaliť metabolizmus liekov
31. Metabolické liekové interakcie. Choroby ovplyvňujúce ich biotransformáciu.
Metabolické interakcie liekov:
1) indukcia enzýmov metabolizmu liekov - absolútne zvýšenie ich počtu a aktivity v dôsledku vystavenia určitým liekom. Indukcia vedie k zrýchleniu metabolizmu liečiv a (spravidla, ale nie vždy) k zníženiu ich farmakologickej aktivity (rifampicín, barbituráty - induktory cytochrómu P450)
2) inhibícia enzýmov metabolizmu liečiv - inhibícia aktivity metabolických enzýmov pod vplyvom niektorých xenobiotík:
A) kompetitívna metabolická interakcia - lieky s vysokou afinitou k niektorým enzýmom znižujú metabolizmus liekov s nižšou afinitou k týmto enzýmom (verapamil)
B) väzba na gén, ktorý indukuje syntézu určitých izoenzýmov cytochrómu P450 (cymedin)
C) priama inaktivácia izoenzýmov cytochrómu P450 (flavonoidy)
Choroby ovplyvňujúce metabolizmus liečiv:
A) ochorenie obličiek (zhoršený prietok krvi obličkami, akútne a chronické ochorenie obličiek, následky dlhodobého ochorenia obličiek)
B) ochorenie pečene (primárna a alkoholická cirhóza, hepatitída, hepatóm)
C) ochorenia tráviaceho traktu a endokrinných orgánov
C) individuálna intolerancia niektorých liekov (nedostatok acetylačných enzýmov - intolerancia aspirínu)
32. Spôsoby a mechanizmy vylučovania liečiv z organizmu. Možnosti kontroly eliminácie liečiva.
Spôsoby a mechanizmy vylučovania liečiva: eliminácia liekov pečeňou a obličkami a niektorými ďalšími orgánmi:
A) obličkami filtráciou, sekréciou, reabsorpciou
B) pečeňou biotransformáciou, vylučovaním žlčou
C) cez pľúca, sliny, pot, mlieko atď., sekréciou, vyparovaním
Možnosti riadenia procesov vysadenia lieku:
1. kontrola pH: v alkalickom moči sa zvyšuje vylučovanie kyslých zlúčenín, v kyslom moči vylučovanie zásaditých zlúčenín.
2.užívanie choleretických liekov (cholenzým, alochol)
3.hemodialýza, peritoneálna dialýza, hemosorpcia, lymfosorpcia
4. Nútená diuréza (IV NaCl alebo glukóza na vodnú záťaž + furosemid alebo manitol)
5.výplach žalúdka, použitie klystírov
33. Pojem receptory vo farmakológii, molekulárna podstata receptorov, signalizačné mechanizmy účinku liečiva (typy transmembránovej signalizácie a sekundárne mediátory).
Receptory - Molekulárne zložky bunky alebo organizmu, ktoré interagujú s liečivami a vyvolávajú množstvo biochemických dejov vedúcich k rozvoju farmakologického účinku.
Koncept receptorov vo farmakológii:
1. Receptory určujú kvantitatívne vzorce účinku lieku
2. Receptory sú zodpovedné za selektivitu účinku liečiva
3. Receptory sprostredkúvajú pôsobenie farmakologických antagonistov
Koncept receptorov je základom pre cielené používanie liekov, ktoré ovplyvňujú regulačné, biochemické procesy a komunikáciu.
Molekulárna povaha receptorov:
1.regulačné proteíny, sprostredkovatelia pôsobenia rôznych chemických signálov: neurotransmitery, hormóny, autokoidy
2.enzýmy a transmembránové proteínové nosiče (Na +, K + ATPáza)
3. štrukturálne proteíny (tubulín, cytoskeletálne proteíny, bunkový povrch)
4.jadrové proteíny a nukleové kyseliny
Signálne mechanizmy účinku lieku:
1) penetrácia ligandov rozpustných v lipidoch cez membránu a ich účinok na intracelulárne receptory.
2) signálna molekula sa viaže na extracelulárnu doménu transmembránového proteínu a aktivuje enzymatickú aktivitu svojej cytoplazmatickej domény.
3) signálna molekula sa viaže na iónový kanál a reguluje jeho otvorenie.
4) signálna molekula sa viaže na receptor na bunkovom povrchu, ktorý je spojený s efektorovým enzýmom prostredníctvom G-proteínu. G-proteín aktivuje sekundárneho posla.
Typy transmembránovej signalizácie:
A) cez 1-TMS receptory s a bez tyrozínkinázovej aktivity
B) cez 7-TMS receptory spojené s G-proteínom
B) cez iónové kanály (závislé od ligandu, od napätia, medzerové kontakty)
Sekundárni sprostredkovatelia: cAMP, ióny Ca2 +, DAG, IF3.
34. Fyzikálno-chemické a chemické mechanizmy účinku liečivých látok.
A) Fyzikálnochemická interakcia s biosubstrátom- neelektrolytický účinok.
Hlavné farmakologické účinky: 1) narkotické 2) celkové depresívne 3) paralyzujúce 4) lokálne dráždivé 5) membranolytické pôsobenie.
Chemická povaha látok: chemicky inertné uhľovodíky, étery, alkoholy, aldehydy, barbituráty, plynné drogy
Mechanizmus účinku je reverzibilná deštrukcia membrán.
b) Chemický(molekulárno-biochemický) mechanizmus účinku liečiv.
Hlavné typy chemickej interakcie s biosubstrátom:
- Slabé (nekovalentné, reverzibilné interakcie) (vodíkové, iónové, monodipólové, hydrofóbne).
- Kovalentné väzby (alkylácia).
Význam nekovalentných liekových interakcií: účinok je nešpecifický, nezávisí od chemickej štruktúry látky.
Význam kovalentných interakcií liekov: pôsobenie je špecifické, kriticky závisí od chemickej štruktúry, realizuje sa prostredníctvom účinku na receptory.
35. Pojmy a pojmy kvantitatívnej farmakológie: účinok, účinnosť, aktivita, agonista (úplný, čiastočný), antagonista. Klinický rozdiel medzi pojmami aktivita a účinnosť liekov.
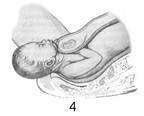 Účinok (odpoveď)- kvantitatívny výťažok reakcie interakcie bunky, orgánu, systému alebo organizmu s farmakologickým činidlom.
Účinok (odpoveď)- kvantitatívny výťažok reakcie interakcie bunky, orgánu, systému alebo organizmu s farmakologickým činidlom.
Efektívnosť- miera reakcie pozdĺž osi účinku - veľkosť odpovede biologického systému na farmakologický účinok; Toto je schopnosť liekov poskytnúť maximálny možný účinok.... To znamená, že v skutočnosti ide o maximálnu veľkosť účinku, ktorú možno dosiahnuť zavedením daného lieku. Číselne charakterizované hodnotou Emax. Čím vyšší je Emax, tým vyššia je účinnosť lieku.
Aktivita- miera citlivosti na liečivá pozdĺž koncentračnej osi, charakterizuje afinitu (afinitu ligandu k receptoru), ukazuje, aká dávka (koncentrácia) liečiva je schopná vyvolať vývoj štandardného účinku rovnajúceho sa 50 % maximálne možné pre tento liek. Číselne charakterizované hodnotou EC50 alebo ED50. Čím vyššia je aktivita lieku, tým nižšia je jeho dávka potrebná na reprodukciu terapeutického účinku.
Účinnosť: 1 = 2 > 3
Aktivita: 1> 3> 2
V klinickej aktivite je dôležitejšie poznať účinnosť, a nie aktivitu, keďže nás viac zaujíma schopnosť liekov vyvolať v tele určitý účinok.
Agonista- ligand, ktorý sa viaže na receptor a spôsobuje biologickú odpoveď, spúšťač fyziologický systém. Úplný agonista- maximálna odozva, Čiastočné- spôsobiť menšiu reakciu, aj keď sú obsadené všetky receptory.
Antagonista- ligandy, ktoré obsadzujú receptory alebo ich menia tak, že strácajú schopnosť interakcie s inými ligandami, ale samy nespôsobujú biologickú reakciu (blokujú pôsobenie agonistov).
 Konkurenčné antagonisty- interagujú s receptormi reverzibilne a tak súťažia s agonistami. Zvýšenie koncentrácie agonistu môže úplne eliminovať účinok antagonistu. Kompetitívny antagonista posúva krivku dávka-odozva pre agonistu, zvyšuje EC50, neovplyvňuje Emax.
Konkurenčné antagonisty- interagujú s receptormi reverzibilne a tak súťažia s agonistami. Zvýšenie koncentrácie agonistu môže úplne eliminovať účinok antagonistu. Kompetitívny antagonista posúva krivku dávka-odozva pre agonistu, zvyšuje EC50, neovplyvňuje Emax.
Nekonkurenčné antagonisty- ireverzibilne menia afinitu receptorov k agonistovi, často nedochádza k väzbe s aktívnym miestom receptora, zvýšenie koncentrácie agonistu neeliminuje účinok antagonistu. Nekompetitívny antagonista znižuje Emax, nemení EC50 a krivka dávka-účinok je stlačená okolo vertikálnej osi.
36. Kvantitatívne vzorce pôsobenia drogy. Zákon znižovania odozvy biologických systémov. Clarkov model a jeho dôsledky. Všeobecná forma závislosti koncentrácia - účinok v normálnych a lognormálnych súradniciach.
Model Clark-Ariens:
1. Interakcia medzi ligandom (L) a receptorom (R) je reverzibilná.
2. Všetky receptory pre daný ligand sú ekvivalentné a nezávislé (ich saturácia neovplyvňuje ostatné receptory).
3. Účinok je priamo úmerný počtu obsadených receptorov.
4. Ligand existuje v dvoch stavoch: voľný a viazaný na receptor.
A) ![]() , kde Kd je rovnovážna konštanta, Ke je vnútorná aktivita.
, kde Kd je rovnovážna konštanta, Ke je vnútorná aktivita.
B) Pretože so zvýšením počtu ligandov v určitom časovom bode budú obsadené všetky receptory, maximálny možný počet vytvorených komplexov ligand-receptor je opísaný vzorcom:
= [R] x ![]() (1)
(1)
Účinok je určený pravdepodobnosťou aktivácie receptora po naviazaní na ligand, t.j. jeho vnútornou aktivitou (Ke), preto E = Ke ×. V tomto prípade je účinok maximálny pri Ke = 1 a minimálny a Ke = 0. Prirodzene, maximálny účinok je opísaný pomerom Emax = Ke ×, kde je celkový počet receptorov pre daný ligand
Účinok tiež závisí od koncentrácie ligandu na [C] receptoroch
E = Emax ![]() (2)
(2)
Z vyššie uvedených vzťahov vyplýva, že EC50 = Kd
![]()
Emax je maximálny účinok, Bmax je maximálny počet naviazaných receptorov, EC50 je koncentrácia liečiva, pri ktorej nastáva účinok rovnajúci sa polovici maxima, Kd je konštanta disociácie látky z receptora, pri ktorej 50 % receptory sú viazané.
Zákon klesajúcej odozvy zodpovedá parabolická závislosť „koncentrácia – účinnosť“. Reakcia na nízke dávky liekov sa zvyčajne zvyšuje priamo úmerne s dávkou... Keď sa však dávka zvyšuje, zvýšenie odpovede sa znižuje a nakoniec možno dosiahnuť dávku, pri ktorej už nedochádza k ďalšiemu zvýšeniu odpovede (v dôsledku obsadenia všetkých receptorov pre daný ligand).
37. Zmena účinku liekov. Postupné a kvantové hodnotenie účinku, podstaty a klinických aplikácií. Opatrenia na kvantifikáciu aktivity a účinnosti liečiv v experimentálnej a klinickej praxi.
Všetky farmakologické účinky možno zhruba rozdeliť do dvoch kategórií:
A) Postupné (kontinuálne, integrálne) efekty- také účinky liekov, ktoré možno kvantitatívne merať (účinok antihypertenzív - podľa hladiny krvného tlaku). Je opísaná postupná „krivka účinku od dávky“ (pozri str. 36), na základe ktorej je možné odhadnúť: 1) individuálnu citlivosť na lieky 2) aktivitu lieku 3) maximálnu účinnosť lieku
b) Kvantové efekty- také účinky liekov, ktoré sú diskrétnou hodnotou, kvalitatívnym znakom, t.j. sú opísané len niekoľkými variantmi stavov (bolesť hlavy po užití analgetika, či už prítomného alebo nie). Je popísaná kvantová krivka dávka-účinok, kde je zaznamenaná závislosť prejavu účinku v populácii od hodnoty podanej dávky lieku. Graf dávka-účinok má kupolovitý tvar a je identický s Gaussovou normálnou distribučnou krivkou. Na základe kvantovej krivky je možné: 1) posúdiť populačnú citlivosť liekov; 2) zaznamenať prítomnosť účinku pri danej dávke; 3) vybrať priemernú terapeutickú dávku.
Rozdiely medzi postupnými a kvantovými charakteristikami dávka-účinok:
Kvantitatívne hodnotenie aktivity a účinnosti liekov sa vykonáva na základe konštrukcie kriviek dávka-účinok a ich následného hodnotenia (pozri odsek 35).
38. Druhy pôsobenia drog. Zmeny v účinku liekov pri ich opätovnom podaní.
Druhy účinku lieku:
1. Miestna akcia- účinok látky, ktorý sa vyskytuje v mieste jej aplikácie (anestetikum - na sliznicu)
2. Resorpčné (systémové) pôsobenie- účinok látky, ktorá sa vyvíja po jej absorpcii, vstupe do celkového krvného obehu a potom do tkanív. Závisí od ciest podávania liečiv a ich schopnosti prenikať cez biologické bariéry.
S lokálnym aj resorpčným pôsobením môžu mať lieky oboje Priamy alebo Reflex vplyv:
A) priamy vplyv - priamy kontakt s cieľovým orgánom (adrenalín na srdci).
B) reflex - zmena funkcie orgánov alebo nervových centier ovplyvnením extero - a interoreceptorov (horčičné náplasti reflexne zlepšujú ich trofizmus pri respiračnej patológii)
Zmeny v účinku liekov pri ich opätovnom zavedení:
1. Kumulácia- zvýšenie účinku v dôsledku akumulácie liečiv v tele:
a) kumulácia materiálu - hromadenie účinnej látky v organizme (srdcové glykozidy)
b) funkčná kumulácia - narastajúce zmeny vo funkcii telesných systémov (zmeny vo funkcii centrálneho nervového systému pri chronickom alkoholizme).
2. Tolerancia (závislosť) - Zníženie reakcie tela na opakované injekcie lieku; aby sa obnovila reakcia na lieky, musí sa podávať vo väčších a väčších dávkach (diazepam):
A) skutočná tolerancia – pozorovaná pri enterálnom aj parenterálnom podávaní liekov, nezávisí od stupňa ich absorpcie do krvného obehu. Je založená na farmakodynamických mechanizmoch závislosti:
1) desenzibilizácia - zníženie citlivosti receptora na liečivo (b-adrenergné agonisty pri dlhodobom používaní vedú k fosforylácii b-adrenergných receptorov, ktoré nie sú schopné reagovať na b-adrenergné agonisty)
2) Down-regulácia - zníženie počtu liekových receptorov (pri opakovanom podávaní narkotických analgetík sa počet opioidných receptorov znižuje a na vyvolanie želanej odpovede sú potrebné ďalšie a ďalšie dávky lieku). Ak liek blokuje receptory, mechanizmus tolerancie k nemu môže byť spojený s up-reguláciou – zvýšením počtu liekových receptorov (b-blokátorov)
3) zahrnutie kompenzačných mechanizmov regulácie (pri opakovaných injekciách antihypertenzív dochádza ku kolapsu oveľa menej často ako pri prvom podaní v dôsledku prispôsobenia baroreceptorov)
B) relatívna tolerancia (pseudotolerancia) - vyvíja sa iba so zavedením liekov do vnútra a je spojená so znížením rýchlosti a úplnosti absorpcie lieku
3. Tachyfylaxia- stav, pri ktorom časté podávanie liekov vyvoláva vznik tolerancie po niekoľkých hodinách, no pri skôr ojedinelých podaniach liekov je jeho účinok plne zachovaný. Rozvoj tolerancie je zvyčajne spojený s vyčerpaním efektorových systémov.
4. Drogová závislosť- neodolateľná túžba užiť predtým podanú látku. Alokovať duševnú (kokaín) a fyzickú (morfín) drogovú závislosť.
5. Precitlivenosť- alergická alebo iná imunologická reakcia na lieky pri opakovanom podaní.
39. Závislosť účinku liekov od veku, pohlavia a individuálnych vlastností organizmu. Význam cirkadiánnych rytmov.
A) Od veku: u detí a starších ľudí je zvýšená citlivosť na lieky (pretože deti majú nedostatok mnohých enzýmov, funkciu obličiek, zvýšenú permeabilitu BBB, v starobe je spomalené vstrebávanie liekov, menej efektívny metabolizmus, rýchlosť vylučovania lieky obličkami sa znižuje):
|
1. Novorodenci majú zníženú citlivosť na srdcové glykozidy, pretože majú viac Na + / K + -ATPáz (cieľov účinku glykozidov) na jednotku plochy kardiomyocytu. 2. Deti majú nižšiu citlivosť na sukcinylcholín a atrakúriu, ale zvýšenú citlivosť na všetky ostatné svalové relaxanciá. 3. Psychofarmaká môžu u detí vyvolať abnormálne reakcie: psychostimulanciá – môžu zvýšiť koncentráciu a znížiť motorickú hyperaktivitu, trankvilizéry – naopak, môžu vyvolať tzv. atypická agitácia. |
1. Citlivosť na srdcové glykozidy sa prudko zvyšuje v dôsledku zníženia počtu Na + / K + -ATPáz. 2. Znižuje citlivosť na b-blokátory. 3. Citlivosť na blokátory kalciových kanálov sa zvyšuje, pretože baroreflex je oslabený. 4. Existuje atypická reakcia na psychofarmaká, podobná reakcii detí. |
b) Z podlahy:
1) antihypertenzíva – klonidín, b-blokátory, diuretiká môžu spôsobiť sexuálne dysfunkcie u mužov, ale neovplyvňujú prácu reprodukčný systémženy.
2) anabolické steroidy sú účinnejšie u žien ako u mužov.
V) Z jednotlivých charakteristík organizmu: nedostatok alebo nadbytok niektorých enzýmov metabolizmu liečiv vedie k zvýšeniu alebo zníženiu ich účinku (nedostatok krvnej pseudocholínesterázy - abnormálne predĺžená svalová relaxácia pri použití sukcinylcholínu)
G) Z cirkadiánnych rytmov: zmena účinku liekov na organizmus, kvantitatívne a kvalitatívne, v závislosti od dennej doby (maximálny účinok s maximálnou aktivitou).
40. Variabilita a variabilita účinku liečiva. Hypo - a hyperreaktivita, tolerancia a tachyfylaxia, hypersenzitivita a idiosynkrázia. Dôvody variability účinku lieku a racionálna stratégia terapie.
Variabilita odráža rozdiely medzi jednotlivcami v reakcii na danú drogu.
Dôvody variability účinku lieku:
1) zmena koncentrácie látky v receptorovej zóne - v dôsledku rozdielov v rýchlosti absorpcie, jej distribúcie, metabolizmu, eliminácie
2) odchýlky v koncentrácii endogénneho ligandu receptora - propranololu (β-blokátora) spomaľujú srdcovú frekvenciu u ľudí so zvýšenou hladinou katecholamínov v krvi, ale neovplyvňujú srdcovú frekvenciu na pozadí u športovcov.
3) zmeny v hustote alebo funkcii receptorov.
4) zmeny v reakčných zložkách umiestnených distálne od receptora.
Stratégia racionálnej terapie: vymenovanie a dávkovanie liekov, berúc do úvahy vyššie uvedené dôvody variability účinku lieku.
Hyporeaktivita- zníženie účinku danej dávky liekov v porovnaní s účinkom, ktorý sa pozoruje u väčšiny pacientov. Hyperreaktivita- zvýšenie účinku danej dávky liekov v porovnaní s účinkom, ktorý sa pozoruje u väčšiny pacientov.
Tolerancia, tachyfylaxia, precitlivenosť – pozri bod 38
Idiosynkrázia- zvrátená reakcia tela na daný liek, spojená s genetickými charakteristikami metabolizmu liekov alebo s individuálnou imunologickou reaktivitou, vrátane alergických reakcií.
41. Hodnotenie bezpečnosti lieku. Terapeutický index a štandardné bezpečnostné rozpätia.
Hodnotenie bezpečnosti sa vykonáva na dvoch úrovniach:
A) predklinické (získanie informácií o toxicite liečiv, účinkoch na reprodukčné funkcie, embryotoxicite a teratogenite, dlhodobých účinkoch)
B) klinické (ďalšie posúdenie účinnosti a bezpečnosti liekov)
Ak po dosiahnutí plató účinku dávka lieku naďalej rastie, potom sa po určitom čase začne prejavovať jeho toxický účinok. Závislosť toxického účinku na dávke (koncentrácii) liečiva má rovnaký charakter ako jeho priaznivý účinok a možno ju opísať postupnými alebo kvantovými krivkami. Tieto krivky možno použiť aj na určenie hodnoty TD50 alebo TC50- toxická dávka (koncentrácia) liečiv, ktorá spôsobí toxický účinok rovnajúci sa 50 % maxima (pre kvantovú krivku - toxický účinok u 50 % jedincov v populácii). Niekedy namiesto TD50 používajú indikátor LD50 - smrteľná dávka, čo spôsobuje smrť 50% objektov v populácii.
Hodnotenie bezpečnosti lieku je charakterizované na základe graduálnych alebo kvantových kriviek dávka-účinok a nasledujúcich ukazovateľov:
A) Terapeutický index Je pomer medzi toxickými a účinnými dávkami liečiva, ktoré spôsobujú výskyt polovičného maximálneho účinku: TI = TD50 / ED50. Čím vyššia je hodnota terapeutického indexu, tým je liek bezpečnejší.
b) Terapeutická šírka (terapeutické okno) Je rozsah dávok medzi minimálnou terapeutickou a minimálnou toxickou dávkou liečiva. Je to správnejší indikátor bezpečnosti lieku, pretože umožňuje vziať do úvahy stupeň zvýšenia nežiaducich účinkov na krivke dávkového účinku.
V) Spoľahlivý bezpečnostný faktor Je pomer minimálnej toxickej dávky k maximálnej účinnej dávke (NFD = TD1 / ED99), ukazuje, koľkokrát je možné prekročiť terapeutickú dávku lieku bez rizika intoxikácie (nežiaduce účinky).
G) Terapeutická chodba Je rozsah účinných koncentrácií liečiva v krvi, ktoré musia byť vytvorené a udržiavané v tele, aby sa dosiahol požadovaný terapeutický účinok.
42,46. Interakcia liekov. Inkompatibilita liekov (keďže otázky spolu súvisia, vyberajte podľa okolností)
Drogová interakcia- ide o zmenu závažnosti a charakteru účinkov pri súčasnom alebo predbežnom užití viacerých liekov.
Dôvody nežiaducich interakcií:
1) polyfarmácia – 6 alebo viac liekov má 7-krát viac vedľajších účinkov, ako keď je liekov menej ako 6.
2) chyby lekárov
3) porušenie dávkovacieho režimu
Zdôvodnenie kombinovanej liečby:
1. Monoterapia nie je dostatočne účinná.
2. Absencia etiotropnej liečby u väčšiny ochorení Þ potreba pôsobenia liečiva na rôzne väzby patogenézy
3. Polymorbidita – čím je človek starší, tým má viac chorôb, ktoré sa vyskytujú súčasne
4. Potreba korigovať nežiaduce účinky drog
5. Zníženie počtu recepcií a podávania liekov (pohodlie pre pacienta, úspora práce zdravotníkov)
Typy interakcie:
ja. Farmaceutické interakcie - Typ interakcie spojenej s fyzikálno-chemickou reakciou medzi liekmi počas výrobného procesu liek, ešte pred zavedením týchto prostriedkov do ľudského tela
A) typické chyby vedúce k farmaceutickej inkompatibilite: vypisovanie zložitých receptov, nesprávne skladovanie, neberie sa do úvahy možnosť adsorpcie liečiv na povrchu plastov (organické dusičnany)
B) problémy s infúznou terapiou: miešanie rozpustných solí, derivátov nerozpustných slabých kyselín alebo zásad vedie k ich zrážaniu; v kvapaline dávkové formy srdcové glykozidy a alkaloidy sú hydrolyzované, AB sú zničené; pH média (alkaloidy sa vyzrážajú v alkalickom prostredí)
C) odporúčania: 1) Všetky zmesi je lepšie pripravovať ex tempore 2) Najspoľahlivejšie riešenie je s jedným liekom 3) Všetky roztoky sa musia pred použitím skontrolovať na suspenzie 4) K interakcii môže dôjsť bez viditeľných zmien roztokov 5) Lieky nemôžu pridávať do krvi a roztokov AK 6) Ak neexistujú špeciálne pokyny, prípravky sa majú rozpustiť v 5% roztoku glukózy (pH 3,5-6,5), izotonickom roztoku NaCl (pH 4,5-7,0).
Roztok glukózy stabilizovaný HCl je nekompatibilný s epinefrínom, benzylpenicilínom, apomorfínom, kanamycínom, vitamínom C, oleandomycínom, srdcovými glykozidmi. Srdcové glykozidy sú nekompatibilné s atropínom, papaverínom, platifilínom. AB sú inkompatibilné s heparínom, hydrokortizónom. Vitamíny skupiny B sú navzájom nekompatibilné, s vitamínmi PP, C. Vitamíny PP a C sú tiež navzájom nekompatibilné.
Nemožno miešať s inými liekmi: fenotiazid, chlórpromazín, barbituráty, prípravky vitamínu C, amfotericín B, furosemid, sulfadiazín, aminofylín, adrenomimetiká.
II... Farmakologické- lieková interakcia, ktorá sa prejaví až v ľudskom organizme po ich kombinovanom užití
A) farmakokinetické
1) počas fázy nasávania.
Pri predstavovaníZa Osinterakcia je určená:
1.kyslosť prostredia
2.priama interakcia v tráviacom trakte
Tetracyklíny interagujú s vápnikom, hliníkom, železom, horčíkom za vzniku chelátových komplexov. Cholestyramín interferuje s absorpciou derivátov kyselín, prípravkov vápnika, varvarínu, digoxínu, digitoxínu, vitamínov rozpustných v tukoch, trimetoprimu, klindamycínu, cefalexínu, tetracyklínu. Prípravky železa sa lepšie vstrebávajú s vitamínom C. Prípravky železa s uhličitanmi, tetracyklíny sa zle vstrebávajú.
3. Gastrointestinálna motilita
Spomaliť peristaltiku: niektoré antidepresíva, antihistaminiká, fenotiazínové antipsychotiká, narkotiká, zvyšujú vstrebávanie digoxínu, kortikosteroidy, antikoagulanciá, znižujú vstrebávanie levodopy. Posilniť peristaltiku a zvýšiť evakuáciu z gastrointestinálneho traktu: metoklopramid, laxatíva. Znížte absorpciu liečiva: fenobarbital - griseofulvín, aspirín - indometacín a diklofenak, PASK - rifampicín.
Metódy kontroly absorpcie počas parenterálneho podávania: lokálne anestetiká + epinefrín + fenylefrín - absorpcia lokálnych anestetík klesá
4.črevná flóra
5.výmena sacieho mechanizmu
2) pri distribúcii a ukladaní:
1.priama interakcia v krvnej plazme: gentamicín + ampicilín alebo karbenicilín - znižujú aktivitu gentamicínu
2. kompetitívne vytesnenie zo spojenia s albumínom v krvnej plazme: indometacín, digitoxín, warfarín sú spojené s krvnými bielkovinami o 90 – 98 %, preto dvojnásobné zvýšenie voľnej frakcie liečiv znamená prudký nárast toxických účinkov; NSAID nahrádzajú: warfarín, fenytoín, metotrexát.
Determinanty klinického významu tejto interakcie:
ü Hodnota Vd (veľká – žiadny problém, malá – možná)
ü vplyv jednej liečivej látky na aktivitu transportných mechanizmov prostredníctvom mechanizmov iných liečiv: transport liečiva sa zvyšuje v závislosti od dávky - inzulín, ACTH, angiotenzín, kiníny atď.; inzulín zvyšuje koncentráciu izoniazidu iba v pľúcach a koncentráciu cottonromazínu - iba v SMC.
3. Vytesnenie z väzby na tkanivové bielkoviny: chinidín vytláča digoxín + znižuje vylučovanie obličkami, čím sa zvyšuje riziko toxicity digoxínu
3) v procese metabolizmu
Lieky môžu zvýšiť alebo znížiť aktivitu cytochrómu P450 a jeho enzýmov (etanol zvyšuje aktivitu niektorých izoenzýmov cytochrómu)
Často interagujúce inhibítory enzýmov:
1. AB: ciprofloxacín, erytromycín, izoniazid, metronidazol
2. Kardiovaskulárne liečivá: amiodarón, diltiazem, chinidín, verapamil
3. Antidepresíva: fluoxetín, sertralen
4. Antisekrečné lieky: cimetidín, omeprazol
5. Antireumatiká: alopurinol
6. Fungicídy: flukonazol, intrakanazol, ketokonazol, mikonazol
7. Antivirotiká: indinavir, retonavir, saquinavir
8. Iné: disulfiram, valproát sodný
Lieky, ktoré majú toxické účinky pri inhibícii MAO: adrenomimetiká, sympatomimetiká, antiparkinsoniká, narkotické analgetiká, fenotiazíny, sedatíva, antihypertenzívne diuretiká, hypoglykemické lieky
4) V procese liahnutia- viac ako 90 % liekov sa vylučuje močom.
Vplyv na pH moču a na stupeň ionizácie liečiva, na ich lipofilitu a ich reabsorpciu
1.interakcia pri pasívnej difúzii: časť liečiva sa vylúči nezmenená, časť liečiva sa ionizuje pri pH moču 4,6-8,2. Klinicky významná je alkalizácia moču: otrava kyselinou acetylsalicylovou alebo fenobarbitalom, pri užívaní sulfónamidov (zníženie rizika kryštalúrie), užívanie chinidínu. Zvýšená kyslosť moču: zvýšené vylučovanie amfetamínu (praktický význam pre detekciu tejto drogy u športovcov)
2.interakcia v období aktívneho transportu: probenezid + penicilín zvyšuje trvanie pohybu penicilínu, probenecid + salicyláty - eliminácia urikozurického účinku probenecidu, penicilínu + CA - zníženie vylučovania penicilínu
Vplyv zloženia moču na vylučovanie liečiva:
Zvýšenie cukru v moči - zvýšenie vylučovania: vitamínu C, chloramfenikolu, morfínu, izoniazidu, glutatiónu a ich metabolitov.
B) farmakodynamické Je interakcia liekov spojená so zmenou farmakodynamiky jedného z nich pod vplyvom druhého (pod vplyvom hormónov štítnej žľazy sa zvyšuje syntéza b-adrenergných receptorov v myokarde a zvyšuje sa účinok adrenalínu na myokard ).
Príklady klinicky významných nežiaducich synergických interakcií:
NSAID + varvarín - zvýšené riziko krvácania
Alkohol + benzodiazepíny – zosilnenie sedatívneho účinku
ACE inhibítory + K + - šetriace diuretiká - zvýšené riziko hyperkaliémie
Verapamil + b-blokátory - bradykardia a asystólia
Alkohol je silným induktorom mikrozomálnych enzýmov, vedie k rozvoju tolerancie na lieky (najmä na anestetiká a hypnotiká), zvyšuje riziko drogovej závislosti.
43. Lieková interakcia. Antagonizmus, synergia, ich typy. Charakter zmeny účinku liekov (aktivita, účinnosť) v závislosti od typu antagonizmu.
Pri interakcii lieku sa môžu vyvinúť tieto stavy: a) zvýšenie účinkov kombinácie liekov b) oslabenie účinkov kombinácie liekov c) inkompatibilita liekov
Posilnenie účinkov kombinácie liekov sa realizuje tromi spôsobmi:
1) Súhrn účinkov alebo aditívnej interakcie- typ liekovej interakcie, pri ktorej sa účinok kombinácie rovná jednoduchému súčtu účinkov každého z liečiv samostatne. Tj. 1+1=2 ... Typické pre liečivá z jednej farmakologickej skupiny, ktoré majú spoločný cieľ účinku (kyselinoneutralizačná aktivita kombinácie hydroxidu hlinitého a horečnatého sa rovná súčtu ich kyselinoneutralizačných schopností samostatne)
2) synergia – typ interakcie, pri ktorej účinok kombinácie prevyšuje súčet účinkov každej z látok užívaných samostatne. Tj. 1+1=3 ... Synergia sa môže týkať požadovaných (terapeutických) aj nežiaducich účinkov liečiv. Kombinované podávanie tiazidového diuretika dichlórtiazidu a ACE inhibítora enalaprilu vedie k zvýšeniu hypotenzívneho účinku každého z činidiel, ktorý sa používa pri liečbe hypertenzie. Súčasné podávanie aminoglykozidových antibiotík (gentamicín) a slučkového diuretika furosemidu však spôsobuje prudké zvýšenie rizika ototoxického účinku a rozvoj hluchoty.
3) potenciácia – druh liekovej interakcie, pri ktorej jedno z liekov, ktoré samo o sebe nemá tento účinok, môže viesť k prudkému zvýšeniu účinku iného lieku. Tj. 1+0=3 (kyselina klavulanová nemá antimikrobiálny účinok, ale môže zvýšiť účinok β-laktámového antibiotika amoxicilínu, pretože blokuje β-laktamázu; adrenalín nemá lokálny anestetický účinok, ale po pridaní do roztoku ultrakaínu , výrazne predlžuje svoj anestetický účinok spomalením absorpcie anestetika z miesta vpichu).
Tlmiace efekty Lieky, keď sa užívajú spolu, sa nazývajú antagonizmus:
1) Chemický antagonizmus alebo antidotum- chemická interakcia látok medzi sebou za vzniku neaktívnych produktov (chemický antagonista iónov železa deferoxamín, ktorý ich viaže do neaktívnych komplexov; protamín sulfát, ktorého molekula má nadbytok kladného náboja - chemický antagonista heparínu, mol. ktorý má nadmerný záporný náboj). Chemický antagonizmus je základom pôsobenia antidot (protijedov).
2) Farmakologický (priamy) antagonizmus- antagonizmus spôsobený viacsmerným pôsobením 2 liečivých látok na rovnaké receptory v tkanivách. Farmakologický antagonizmus môže byť kompetitívny (reverzibilný) a nekompetitívny (ireverzibilný):
A) kompetitívny antagonizmus: kompetitívny antagonista sa reverzibilne viaže na aktívne centrum receptora, t.j. chráni ho pred pôsobením agonistu. Pretože stupeň väzby látky na receptor je úmerný koncentrácii tejto látky, účinok kompetitívneho antagonistu možno prekonať zvýšením koncentrácie agonistu. Vytlačí antagonistu z aktívneho miesta receptora a vyvolá úplnú odpoveď tkaniva. To. kompetitívny antagonista nemení maximálny účinok agonistu, ale na interakciu agonistu s receptorom je potrebná vyššia koncentrácia. Kompetitívny antagonista Posúva krivku dávka-odozva pre agonistu doprava vzhľadom na počiatočné hodnoty a zvyšuje EC50 pre agonistu bez ovplyvnenia hodnoty E Max.
V lekárskej praxi sa často používa konkurenčný antagonizmus. Keďže účinok kompetitívneho antagonistu možno prekonať, ak jeho koncentrácia klesne pod hladinu agonistu, pri liečbe kompetitívnymi antagonistami je potrebné jeho hladinu neustále udržiavať dostatočne vysokú. Inými slovami, klinický účinok kompetitívneho antagonistu bude závisieť od jeho polčasu eliminácie a koncentrácie úplného agonistu.
B) nekompetitívny antagonizmus: nekompetitívny antagonista sa takmer ireverzibilne viaže na aktívne centrum receptora alebo interaguje vo všeobecnosti s jeho alosterickým centrom. Preto bez ohľadu na to, ako sa koncentrácia agonistu zvyšuje, nie je schopný vytesniť antagonistu z jeho spojenia s receptorom. Pretože niektoré z receptorov, ktoré sú spojené s nekompetitívnym antagonistom, už nie je možné aktivovať , hodnota EMax klesá, afinita receptora k agonistovi sa nemení, takže hodnota EC50 zostáva rovnaká. Na krivke dávka-odozva sa pôsobenie nekompetitívneho antagonistu prejaví ako stlačenie krivky vzhľadom na vertikálnu os bez jej posunutia doprava.
Schéma 9. Typy antagonizmu.
A - kompetitívny antagonista posúva krivku dávka-účinok doprava, tj znižuje citlivosť tkaniva na agonistu bez zmeny jeho účinku. B - nekompetitívny antagonista znižuje veľkosť odpovede tkaniva (účinok), ale neovplyvňuje jeho citlivosť na agonistu. C - variant použitia čiastočného agonistu na pozadí plného agonistu. Keď sa koncentrácia zvyšuje, čiastočný agonista vytesňuje úplného agonistu z receptorov a v dôsledku toho sa tkanivová odozva znižuje z maximálnej odozvy na plného agonistu na maximálnu odozvu na čiastočného agonistu.
Nekompetitívne antagonisty sa v lekárskej praxi používajú menej často. Na jednej strane majú nepochybnú výhodu, pretože ich účinok sa po naviazaní na receptor nedá prekonať, a preto nezávisí od polovice eliminačného obdobia antagonistu ani od hladiny agonistu v organizme. Účinok nekompetitívneho antagonistu bude určený iba rýchlosťou syntézy nových receptorov. Ale na druhej strane, ak dôjde k predávkovaniu týmto liekom, bude veľmi ťažké odstrániť jeho účinok.
|
Konkurenčný antagonista |
Nekonkurenčný antagonista |
|
Štruktúrou podobný agonistu |
Štrukturálne odlišný od agonistu |
|
Viaže sa na aktívne centrum receptora |
Viaže sa na alosterické miesto receptora |
|
Posúva krivku dávka-odozva doprava |
Posúva krivku dávka-odozva vertikálne |
|
Antagonista znižuje citlivosť tkaniva na agonistu (EC50), ale neovplyvňuje maximálny účinok (Emax), ktorý možno dosiahnuť pri vyššej koncentrácii. |
Antagonista nemení citlivosť tkaniva na agonistu (EC50), ale znižuje vnútornú aktivitu agonistu a maximálnu odpoveď tkaniva na neho (Emax). |
|
Účinok antagonistu možno zvrátiť vysokou dávkou agonistu |
Antagonistický účinok nemožno zvrátiť vysokou dávkou agonistu. |
|
Účinok antagonistu závisí od pomeru dávky agonistu a antagonistu |
Účinok antagonistu závisí len od jeho dávky. |
Losartan je kompetitívny antagonista proti AT1 receptorom angiotenzínu, narúša interakciu angiotenzínu II s receptormi a pomáha znižovať krvný tlak. Účinky losartanu možno prekonať podaním vysokej dávky angiotenzínu II. Valsartan je nekompetitívny antagonista rovnakých receptorov AT1. Jeho účinok nie je možné prekonať ani podávaním vysokých dávok angiotenzínu II.
Zaujímavá je interakcia, ktorá prebieha medzi úplnými a čiastočnými agonistami receptora. Ak koncentrácia plného agonistu prekročí úroveň čiastočného, potom sa v tkanive pozoruje maximálna odpoveď. Ak hladina čiastočného agonistu začne stúpať, vytlačí plného agonistu z väzby na receptor a odozva tkaniva začne klesať z maxima pre plného agonistu na maximum pre čiastočného agonistu (tj úroveň, pri ktorej zaberá všetky receptory).
3) Fyziologický (nepriamy) antagonizmus- antagonizmus spojený s vplyvom 2 liečiv na rôzne receptory (ciele) v tkanivách, čo vedie k vzájomnému oslabeniu ich účinku. Napríklad medzi inzulínom a adrenalínom sa pozoruje fyziologický antagonizmus. Inzulín aktivuje inzulínové receptory, v dôsledku čoho sa zvyšuje transport glukózy do bunky a klesá hladina glykémie. Epinefrín aktivuje b2-adrenergné receptory pečene, kostrových svalov a stimuluje rozklad glykogénu, čo v konečnom dôsledku vedie k zvýšeniu hladiny glukózy. Tento typ antagonizmu sa často používa v núdzovej starostlivosti o pacientov s predávkovaním inzulínom, ktoré viedlo k hypoglykemickej kóme.
44. Vedľajšie a toxické účinky liekov. Teratogénne, embryotoxické, mutagénne účinky liekov.
Vedľajšie účinky- tie účinky, ktoré sa vyskytujú, keď sa látky používajú v terapeutických dávkach a tvoria spektrum ich farmakologického účinku (analgetický morfín v terapeutických dávkach spôsobuje eufóriu), môžu byť primárne a sekundárne:
A) primárne vedľajšie účinky- ako priamy dôsledok vplyvu tohto lieku na špecifickom substráte (hyposalivácia pri použití atropínu na odstránenie bradyarytmie)
B) sekundárne vedľajšie účinky – nepriame vedľajšie účinky (AB, potlačenie normálnej mikroflóry, môže viesť k superinfekcii)
Toxické účinky – nežiaduce účinky prejaví sa u tohto lieku, keď opustí terapeutické rozmedzie (predávkovanie liekom)
Selektivita účinku liečiva závisí od jeho dávky. Čím vyššia je dávka lieku, tým je menej selektívny.
Teratogénne pôsobenie- schopnosť liekov pri podávaní tehotnej žene spôsobiť anatomické anomálie vývoja plodu (talidomid: fokomélia, antiblastómy: mnohopočetné defekty)
Embryotoxický účinok- nepriaznivý účinok, ktorý nie je spojený s porušením organogenézy v prvých troch mesiacoch tehotenstva. Neskôr sa objaví Fetotoxický účinok.
Mutagénny účinok liekov- poškodenie zárodočnej bunky a jej genetického aparátu liečivami, ktoré sa prejavuje zmenou genotypu potomstva (adrenalín, cytostatiká).
Karcinogénny účinok liekov- schopnosť niektorých liekov vyvolať karcinogenézu.
45. Lekárske a sociálne aspekty boja proti drogovej závislosti, drogovej závislosti a alkoholizmu. Koncept zneužívania návykových látok.
« Je nepravdepodobné, že by sa ľudstvo ako celok niekedy zaobišlo bez umelého raja. Väčšina mužov a žien vedie taký bolestivý život, ktorý je prinajlepšom taký monotónny, úbohý a obmedzený, že túžba „opustiť“ ho, odpojiť sa aspoň na pár okamihov, je a vždy bola jednou z hlavných Prial Ny duše"(Huxley, práca" The Doors of Perception ")
1) Drogová závislosť- stav mysle a / alebo fyzický stav, ktorý je dôsledkom účinku drogy na telo a je charakterizovaný špecifickými behaviorálnymi reakciami, je ťažké prekonať túžbu znovu užívať drogy, aby sa dosiahol špeciálny mentálny efekt alebo aby sa predišlo nepohodliu pri absencii liekov v tele. Drogová závislosť je charakterizovaná:
A) Psychická závislosť- rozvoj emocionálneho stresu, keď prestanete užívať drogy. Človek sa cíti prázdny, upadá do depresie, prežíva pocit strachu, úzkosti, jeho správanie sa stáva agresívnym. Všetky tieto psychopatologické symptómy vznikajú na pozadí myšlienok o potrebe vstreknúť si drogu, ktorá spôsobila závislosť. Túžba brať drogy sa môže pohybovať od jednoduchej túžby až po vášnivý smäd po drogách, ktorý absorbuje všetky ostatné potreby a mení sa na zmysel života človeka. Verí sa, že psychická závislosť sa vyvinie, keď si človek uvedomí, že optimálnu pohodu môže dosiahnuť iba zavedením drog. Základom psychickej závislosti je viera človeka v pôsobenie drogy (prípady rozvoja psychickej závislosti na placebe sú popísané v literatúre).
b) Fyzická závislosť- porušenie normálneho fyziologického stavu tela, ktoré si vyžaduje neustálu prítomnosť liekov v ňom na udržanie stavu fyziologickej rovnováhy. Vysadenie lieku spôsobuje rozvoj špecifického komplexu symptómov - abstinenčného syndrómu - komplexu duševných a neurovegetatívnych porúch vo forme dysfunkcie v opačnom smere, ako je charakteristické pre pôsobenie (morfín tlmí bolesť, tlmí dýchacie centrum, zužuje zreničky, spôsobuje zápchu, s abstinenčnými príznakmi sa u pacienta objavia neznesiteľné bolesti, časté hlučné dýchanie, zreničky sú rozšírené a vzniká pretrvávajúca hnačka)
V) Tolerancia... Tolerancia na lieky, ktoré spôsobujú drogovú závislosť, je často prierezová, to znamená, že nevzniká len voči danej chemickej zlúčenine, ale aj voči všetkým štruktúrne podobným zlúčeninám. Napríklad u pacientov s drogovou závislosťou od morfínu vzniká tolerancia nielen naň, ale aj na iné opioidné analgetiká.
Pre vznik drogovej závislosti nie je nevyhnutnou podmienkou prítomnosť všetkých 3 kritérií, v tabuľke 3 sú uvedené hlavné typy drogovej závislosti a jej zložky.
Opioidy, barbituráty, alkohol spôsobujú silnú fyzickú a psychickú závislosť a toleranciu. Anxiolytiká (diazepam, alprazolam) spôsobujú prevažne psychickú závislosť.
2) Závislosť ( drogová závislosť) - Ide o mimoriadne ťažkú formu drogovej závislosti, nutkavé užívanie drog, charakterizované neustále sa zvyšujúcim, neodolateľným nutkaním podávať si tento liek, zvyšujúc jeho dávku. Kompulzívnosť túžby znamená, že potreba podať liek dominuje nad všetkými ostatnými (aj životne dôležitými) potrebami pacienta. Z hľadiska túto definíciu, túžba po morfíne je drogová závislosť, zatiaľ čo túžba po nikotíne je drogová závislosť.
3) Závislý na medicíne- charakterizuje menej intenzívnu túžbu po liekoch, keď odmietnutie liekov vyvoláva len pocit mierneho nepohodlia, bez rozvoja fyzickej závislosti alebo detailného obrazu psychickej závislosti. To. závislosť zahŕňa tú časť drogovej závislosti, ktorá nezodpovedá definícii závislosti. Napríklad už spomínaná drogová závislosť na nikotíne je formou závislosti.
4) Drogová závislosť- neoprávnené užívanie drog v takých dávkach a takými spôsobmi, ktoré sa líšia od uznávaných medicínskych alebo spoločenských štandardov v tejto kultúre a v daný čas... To. zneužívanie drog zahŕňa iba sociálne aspekty užívania drog. Príkladom zneužívania je použitie anabolické steroidy v športe alebo na zlepšenie fyzičky mladých mužov.
5) Alkoholizmus- chronické požívanie alkoholu (etylalkoholu), ktoré v dnešnej dobe vedie k poškodeniu viacerých orgánov (pečeň, gastrointestinálny trakt, centrálny nervový systém, kardiovaskulárny systém, imunitný systém) a sprevádzaná psycho-fyzickou závislosťou.
6) Zneužívanie látok- chronické zneužívanie rôznych drog (vrátane drog, alkoholu, halucinogénov), prejavujúce sa rôznymi duševnými a somatickými poruchami, poruchami správania, sociálnou degradáciou.
Liečba drogovej závislostiťažká a nevďačná úloha. Stále nevytvorené efektívna metodika, čo by zabezpečilo úspešnosť liečby u viac ako 30 – 40 % pacientov. Dosiahnutie akýchkoľvek badateľných výsledkov je možné len pri plnej spolupráci úsilia pacienta, lekára a sociálneho prostredia, v ktorom sa chorý človek nachádza (princíp dobrovoľnosti a individuality). Moderné techniky sú založené na nasledujúcich princípoch:
ü psychoterapeutické a pracovné terapeutické metódy;
ü skupinová liečba a rehabilitácia (spoločnosť anonymných alkoholikov, drogovo závislých)
ü postupné alebo náhle vysadenie lieku na pozadí detoxikačnej terapie
ü vykonávanie substitučnej terapie (náhrada omamnej látky pomaly a dlhodobo pôsobiacimi analógmi s ich následným zrušením; napr. program tzv. metadónovej substitučnej terapie pre závislých od heroínu)
ü liečba špecifickými antagonistami (naloxón a naltrexón) alebo senzibilizačnými látkami (teturam)
ü neurochirurgické metódy kryodeštrukcie cingulárneho gyru a hipokampu
47. Druhy farmakoterapie. Deontologické problémy farmakoterapie.
Farmakoterapia (FT) - súbor liečebných metód založených na užívaní liekov. Hlavné typy FT:
1.etiotropná PT - korekcia a odstránenie príčiny ochorenia (AB pri infekčných ochoreniach)
2.patogenetická FT - vplyv na mechanizmus rozvoja ochorenia (ACE inhibítory pri hypertenzii)
3.symptomatická FT - odstránenie príznakov ochorenia, ak nie je možné ovplyvniť jeho príčinu alebo patogenézu (NSAID na chrípku)
4.Substitučná FT - užívanie liekov pri nedostatku prirodzených biologicky aktívnych látok (inzulín pri cukrovke)
5. profylaktická FT (vakcíny, séra, kyselina acetylsalicylová na ischemickú chorobu srdca)
Postoj spoločnosti k drogám na súčasné štádium : 1) túžba získať dávky bez rizika 2) nádej na zázrak, vízie 3) nepochopenie rizika užívania drog 4) rozhorčenie a „spravodlivé rozhorčenie“, unáhlené hodnotenia liekov 5) túžba získať nové lieky
Postoj lekára k drogám: terapeutický optimizmus (spoliehanie sa na lieky ako silnú zložku terapie), terapeutický nihilizmus (popieranie nových liekov, dodržiavanie určitých liekov, nedôvera k novým liekom)
Compliance (adherencia) pacienta k liečbe 1) pochopenie pokynov lekára a cieľov liečby 2) snaha presne dodržiavať predpisy lekára.
V súčasnosti je na svete asi 100 000 liekov, viac ako 4 000 je registrovaných v Bieloruskej republike, z toho asi 300 životne dôležitých liekov. Štúdium farmakológie pomáha neutopiť sa v mori drog.
48. Základné princípy liečby a prevencie otravy liekmi. Antidotová terapia.
Klasifikácia toxických látok (OM):
1. Tým, že patrí do určitých tried chemických zlúčenín: barbituráty, benzodiazepíny, kyanidy.
2. Podľa pôvodu: nebiologickej povahy (kyseliny, zásady, soli ťažkých kovov), toxické splodiny niektorých MB (botulotoxín), rastlinného pôvodu (alkaloidy, glykozidy), živočíšneho pôvodu (hadí a včelí jed)
3. Podľa stupňa toxicity: a) extrémne toxické (DL50< 1 мг/кг) б) высоко токсические (1-50) в) сильно токсические (50-500) г) умеренно токсические (500-5000) д) мало токсические (5000-15000) е) практически нетоксические (> 15.000)
4. Toxikologickým účinkom: a) nervovo paralytické (bronchospazmus, dýchavičnosť) b) kožné resorpčné c) celkové toxické (hypoxické kŕče, kóma, paralýza) d) dusivé e) slzné a dráždivé e) psychotropné (zhoršená duševná činnosť, vedomie )
5. V závislosti od oblasti preferenčného použitia: priemyselné jedy, pesticídy, jedy pre domácnosť, chemické bojové látky, liečivé látky.
6. V závislosti od toxicity liečiv: Zoznam A - liečivá, ktorých účel, použitie, dávkovanie a skladovanie treba vzhľadom na ich vysokú toxicitu robiť veľmi opatrne. Rovnaký zoznam zahŕňa drogy, ktoré spôsobujú drogovú závislosť; zoznam B - lieky, ktorých vymenovanie, užívanie, dávkovanie a skladovanie treba v súvislosti s možné komplikácie pri použití bez lekárskeho dozoru.
Selektívne toxický účinok liekov.
A) kardiotoxické: srdcové glykozidy, prípravky draslíka, antidepresíva
B) neurotoxické: psychofarmakologické látky, oxychinolíny, aminoglykozidy
B) hepatotoxické: tetracyklíny, chloramfenikol, erytromycín, paracetamol
D) nefrotoxické: vankomycín, aminoglykozidy, sulfónamidy
E) gastroenterotoxické: steroidné protizápalové lieky, NSAID, rezerpín
E) hematotoxické: cytostatiká, chloramfenikol, sulfónamidy, dusičnany, dusitany
G) pneumotoxické
Toxikokinetika - študuje absorpciu, distribúciu, metabolizmus a vylučovanie liekov užívaných v toxických dávkach.
Vstup toxických látok do organizmu je možný a) enterálne b) parenterálne. Rýchlosť a úplnosť absorpcie odráža rýchlosť rozvoja toxického účinku a jeho závažnosť.
Distribúcia v tele: Vd = D / Cmax - skutočný objem, v ktorom sa jedovatá látka distribuuje v tele. Vd> 5-10 l / kg - OM je ťažko tolerovaný na jeho odstránenie (antidepresíva, fenotiazíny). Vd< 1 л/кг – ОВ легче удалить из организма (теофиллин, салицилаты, фенобарбитал).
Predávkovanie- zmeny vo farmakokinetických procesoch: rozpustnosť, spojenie s bielkovinami, metabolizmus ® výrazné zvýšenie voľnej frakcie liečiv ® toxický účinok.
Kinetika prvého rádu sa so zvýšením koncentrácie liečiva transformuje na kinetiku nultého rádu.
Toxigénne štádium je detoxikačná terapia, somatogénne štádium je symptomatická terapia.
Toxikodynamika . Hlavné mechanizmy toxického účinku:
A) mediátor: priamy (podľa typu kompetitívnej blokády - FOS, psychomimetiká) a nepriamy (aktivátory alebo inhibítory enzýmov)
B) interakcia s biomolekulami a vnútrobunkovými štruktúrami (hemolytické látky)
C) metabolizmus podľa typu letálnej syntézy (etylalkohol, tiofos)
D) enzymatické (hadie jedy atď.)
Typy pôsobenia: lokálne, reflexné, resorpčné.
Klasifikácia otravy:
1. Etiopatogenetické:
a) náhodné (samoliečba, chybný príjem)
b) úmyselné (s cieľom samovraždy, vraždy, rozvinutia bezmocného stavu u obete)
2. Klinické:
a) v závislosti od rýchlosti rozvoja otravy: akútna (podanie jednorazovej dávky alebo s krátkym časovým odstupom toxickej dávky látky), subakútna (oneskorený vývoj klinického obrazu po jednorazovej dávke), chronická
b) v závislosti od prejavu hlavného syndrómu: poškodenie CVS, poškodenie DS a pod.
c) v závislosti od závažnosti stavu pacienta: ľahký, stredný, ťažký, mimoriadne ťažký
3. Nozologické: zohľadňuje názov lieku, názov skupiny látok
Všeobecný mechanizmus smrti v prípade otravy:
A) porážka CVS:
1) zníženie krvného tlaku, hypovolémia periférnych ciev, kolaps, bradya alebo tachykardia (tricyklické antidepresíva, betablokátory, blokátory vápnikových kanálov)
2) arytmie (ventrikulárna tachykardia, fibrilácia - tricyklické antidepresíva, teofylín, amfetamín)
B) poškodenie centrálneho nervového systému: stupor, kóma ® útlm dýchania (lieky, barbituráty, alkohol, hypnosedatíva)
C) kŕče, svalová hyperreaktivita a rigidita ® hypertermia, myoglobinúria, zlyhanie obličiek, hyperkaliémia
Toxikologická triáda:
1) dĺžka užívania, dávka a anamnéza látky ® .
2) posúdenie stavu vedomia podľa symptómov: dýchanie, krvný tlak, telesná teplota
3) laboratórne údaje
Základné princípy liečby:
ja Prvá pomoc: umelé dýchanie, masáž srdca, protišoková terapia, kontrola rovnováhy voda-elektrolyt
II... Oneskorené vstrebávanie a odstraňovanie nevstrebaného OM z tela:
Účel: ukončiť kontakt s OV
1. Parenterálna cesta:
a) cez pľúca:
1) zastavte inhaláciu
2) dráždivé látky (amoniak, formaldehyd) ® na upevnenie aktívnych pohybov, zahriatie, dodanie kyslíka a odpeňovače (pre amoniak je odpeňovač ocot a pre formaldehyd zriedený roztok amoniaku)
b) cez kožu: zmyť veľkým množstvom teplej vody s mydlom alebo saponátom, špecifickými protilátkami, neutralizovať a ukončiť expozíciu OM na koži (FOS: umyť vodou, odstrániť 10-15% amoniakom alebo 5- 6% roztok hydrogénuhličitanu sodného s vodou; fenolkrezol: rastlinný olej alebo etylénglykol, ale nie vazelínový olej, KMNO4: 0,5-1% roztok kyseliny askorbovej alebo rovnaké objemy 3% peroxidu vodíka a 3% roztoku kyseliny octovej, CCl4, terpentín, benzín : teplá mydlová voda)
c) pri injekcii do končatiny: turniket nad miestom vpichu
d) pri zasiahnutí očí: vyplachovať teplým fyziologickým roztokom alebo mliekom 10-20 minút, kvapkať lokálne anestetikum; v prípade kontaktu s kyselinami a zásadami ich nemožno neutralizovať. Vyžaduje sa konzultácia s oftalmológom.
2. Enterálna cesta: na uvoľnenie žalúdka z OM, na urýchlenie pasáže
a) odstránenie OM:
1) predbežný príjem vody. Neužívajte mlieko (s výnimkou žieravých jedovatých látok) a etanol (s výnimkou metanolu).
2) vracanie - indikované hlavne pri otravách veľkými tabletami alebo kapsulami, ktoré nemôžu prejsť cez sondu. Môže byť vyvolaná reflexne alebo vracaním (NaCl: 1 polievková lyžica na 1 pohár vody; sirup Ipecac: dospelí 2 polievkové lyžice, deti 2 čajové lyžičky; horčica: 1-2 čajové lyžičky na pohár vody; apomorfín: 5-10 mg / kg subkutánne, okrem detí mladších ako 5 rokov). Po požití nevyvolávať zvracanie: organické rozpúšťadlá - nebezpečenstvo vdýchnutia, saponáty - penenie, kŕčovité látky - nebezpečenstvo vdýchnutia, žieraviny - poškodenie pažeráka)
3) sonda výplach žalúdka - je núdzové a povinné opatrenie. Žalúdok sa umyje, ak od otravy neuplynulo viac ako 4-6 hodín, niekedy až 10 hodín; pri otrave kyselinou acetylsalicylovou - po 24 hodinách. Pacient je predintubovaný hadičkou s nafukovacou manžetou: v kóme bez kašľa a laryngeálneho reflexu. Žalúdok sa premyje vodou alebo soľným roztokom 30 ° C, postup trvá 4 hodiny alebo viac. Na konci oplachovania - Aktívne uhlie a síran sodný.
b) zníženie absorpcie z gastrointestinálneho traktu: aktívne uhlie vo vnútri po vyprázdnení žalúdka + síran sodný alebo horečnatý. Vlastnosti opatrení na zníženie absorpcie:
1) organické rozpúšťadlá: nevyvolávať zvracanie, výplach žalúdka po intubácii, aktívne uhlie + tekutý parafín
2) pracie prostriedky: nevyvolávať zvracanie a vyplachovať žalúdok, je potrebné podať veľa vody + odpeňovače (simetikon)
3) kyseliny a zásady: zvracanie nie je možné vyvolať, výplach žalúdka cez hadičku namazanú rastlinným olejom po podaní narkotického analgetika je jedinou indikáciou na podávanie mlieka. Pri otravách kyselinou - antacidá, pri otravách zásadami - kyselina citrónová alebo octová.
III... Odstránenie absorbovaného OM z tela
a) forsírovaná diuréza (podmienky: dostatočný prietok krvi obličkami a glomerulárna filtrácia; vyliať-vyliať 20-25 litrov za 24 hodín)
b) peritoneálna hemodialýza
c) hemosorpcia
d) výmenná transfúzia krvi
e) nútená hyperventilácia
IV... Symptomatická liečba funkčných porúch.
Antidotá: 1) toxikotropné - viažuce, neutralizujúce a zabraňujúce absorpcii OM: pôsobiace na princípe aktívneho uhlia, pôsobiace na chemickom princípe (unitiol, penicilamín, pentacín)
2) toxikokinetika – urýchľuje biotransformáciu OM (trimedoxím bromid, tiosíran sodný, etanol, AO)
3) farmakologické - atropín, naloxón
4) imunologické antidotá
Unithiol, succimer - viaže ťažké kovy, metaloidy, srdcové glykozidy. Esmolol viaže teofylín, kofeín. Pentoát vápenatý trojsodný - tvorí komplexy s dvojmocnými a trojmocnými kovmi.
49. Receptúra a jej štruktúra. Všeobecné pravidlá vypísanie receptu. Štátna úprava pravidiel predpisovania a výdaja liekov.
Recept- ide o písomnú výzvu lekára lekárnikovi s požiadavkou na uvoľnenie lieku v určitej forme a dávke s uvedením spôsobu jeho použitia
V recepte sa rozlišujú tieto časti:
1. Inscriptio - názov, nápis. Sem sa píše dátum vystavenia receptu, priezvisko, iniciály a vek pacienta, priezvisko a iniciály lekára.
2. Invocatio - kontaktovanie lekárnika. Vyjadruje sa slovom „Recept“ (take) alebo skratkou (Rp.)
3. Designatio materiarum - označenie alebo názov liekov s uvedením ich dávok. V komplexnom receptúre sa zoznam liečivých látok vykonáva v špecifickom poradí. Prvým je hlavná liečivá látka (základ). Potom sú napísané adjuvans. Potom sú uvedené zložky, ktoré upravujú chuť, vôňu, farbu lieku (korigens). Ako posledné píšu látky, ktoré dávajú droge určitú liekovú formu (zložky).
4. Subscriptio - predpis (indikácia) lekárnikovi. Označuje liekovú formu, farmaceutické operácie potrebné na jej výrobu, počet vydaných dávok lieku.
5. Signatura - poučenie pacienta o užívaní lieku.
6. Subscriptio medici - podpis lekára, ktorý predpis vypísal, jeho osobná pečať.
Odvolanie lekára k lekárnikovi, názov liekov zahrnutých na recepte, názov liekovej formy a charakter lekárenskej prevádzky sa píše v č. latinčina... Názvy liečiv, botanické názvy rastlín sa píšu s veľkým začiatočným písmenom. Recept pre pacienta je napísaný v ruštine alebo v národných jazykoch.
Všeobecné pravidlá predpisovania:
1. Recept sa vypisuje na osobitnom tlačive v závislosti od vypisovaného lieku zreteľným rukopisom, atramentom alebo guľôčkovým perom bez opráv.
2. Recept obsahuje dátum, mesiac, rok, priezvisko, meno, priezvisko a vek pacienta, priezvisko, meno a priezvisko lekára. Potom nasleduje text receptu, v ktorom sú uvedené názvy látok obsiahnutých v recepte v genitívnom prípade s uvedením ich množstva
3. Jednotkou hmotnosti v receptoch je gram alebo JEDNOTKA.
4. Pri prekročení maximálnej dávky jedovatých a potentných látok sa to potvrdí slov
5. Recept je potvrdený podpisom a osobnou pečiatkou lekára
Bieloruská republika má štátnu reguláciu pravidiel predpisovania a vydávania liekov.
50. Pravidlá predpisovania jedovatých, omamných a silných liekov.
Zoznam A zahŕňa lieky, ktorých vymenovanie, použitie, dávkovanie a skladovanie by sa malo vzhľadom na ich vysokú toxicitu vykonávať veľmi opatrne. Rovnaký zoznam obsahuje drogy, ktoré spôsobujú drogovú závislosť.
Zoznam B zahŕňa lieky, ktorých vymenovanie, použitie, dávkovanie a skladovanie by sa malo vykonávať opatrne v súvislosti s možnými komplikáciami pri ich používaní bez lekárskeho dohľadu.
Pre jedovaté a silné lieky boli stanovené maximálne vyššie jednorazové a denné dávky. Tieto dávky sú určené pre dospelých nad 25 rokov. Pri prepočte dávok pre osoby staršie ako 60 rokov sa berie do úvahy veková citlivosť na rôzne skupiny LS. Dávky liekov, ktoré tlmia centrálny nervový systém, ako aj srdcové glykozidy a diuretiká sa znižujú o 50%, dávky iných jedovatých a silných liekov sa znižujú na 2/3 dávky pre dospelých. Dávky AB, sulfónamidov a vitamínov sú väčšinou pre všetkých rovnaké vekových skupín počnúc 25. rokom života.
1. Predpisujú sa omamné látky (zoznam A). receptový formulár Forma 2. Jedna forma – jeden liek. Musí tam byť: podpis a pečiatka ošetrujúceho lekára, podpis vedúceho lekára zdravotníckeho zariadenia, okrúhla pečiatka zdravotníckeho zariadenia.
2. Jedovaté drogy (zoznam A), silné (zoznam B) sa predpisujú na receptovom tlačive tlačiva 1. Musí tam byť podpis a osobná pečiatka lekára, pečiatka zdravotníckeho zariadenia.
51. Lieky pod kontrolou. Lieky na predpis.
Narkotické, jedovaté a silné drogy sú pod kontrolou (pozri časť 20)
A) Lieky neregistrované v Bieloruskej republike a nepovolené na oficiálne použitie
B) lieky na žiadosť pacientov a ich príbuzných bez vyšetrenia pacienta a stanovenia diagnózy
C) recepty na omamné látky na injekciu, éter anestetika, chlóretyl, pentamín, fluórtán, oxybutyrát sodný v ampulkách, oxybutyrát lítny, síran bárnatý na fluoroskopiu.
52. Farmakokinetické modely (jednokomorové a dvojkomorové), kvantitatívne zákony absorpcie a eliminácie liečiv.
![]() Jednokomorový model.
Jednokomorový model.
Celý organizmus je jedna homogénna nádoba. Predpoklady:
1) dochádza k rýchlemu dynamickému vývoju medzi obsahom liečiva v krvnom obehu a jeho koncentráciou v extravaskulárnych tkanivách
2) Liečivo sa rýchlo a rovnomerne distribuuje v celom objeme krvi
3) Eliminácia liečiv sa riadi kinetikou prvého poriadku: rýchlosť poklesu obsahu liečiva v krvi je úmerná jeho koncentrácii
Ak mechanizmy eliminácie liečiva (biotransformácia v pečeni, renálna sekrécia) nie sú nasýtené zavedením terapeutickej dávky, bude log-normálny graf zmien plazmatickej koncentrácie v čase lineárne.
Sklon lognormálna os - Kel, kde Kel je rýchlostná konštanta eliminácie a má rozmer času-1. Hodnota C0 sa získa extrapoláciou grafu na priesečník s ordinátnou osou. Plazmatická koncentrácia liečiva(Ct) kedykoľvek t po podaní do tela je:
Ln Ct = Ln C0 - kt. Eliminačná konštanta Kel, Vd a celkový klírens (CL) sú spojené výrazom: CL = k × Vd
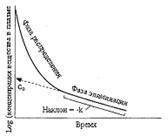 Dvojkomorový model.
Dvojkomorový model.
Často po vstupe liečiva do tela nie je možné rýchlo dosiahnuť rovnováhu medzi obsahom liečiva v krvi a jeho koncentráciou v extravaskulárnej tekutine. Potom sa predpokladá, že v súhrne tkanív a biologických tekutín tela možno rozlíšiť dve komory, ktoré sa líšia stupňom prístupnosti pre penetráciu liečiva. Centrálna komora obsahuje krv (často s intenzívne prekrvenými orgánmi - pečeň, obličky) a periférna komora - intersticiálna tekutina vnútorných orgánov a tkanív.
Výsledný graf ukazuje začiatočné Distribučná fáza (Čas potrebný na to, aby liek dosiahol rovnovážny stav medzi centrálnou a periférnou komorou a nasledujúci pomalý Vylučovacia fáza Prvá objednávka.
Hodnota C0 získaná extrapoláciou Vylučovacie fázy pred prekročením súradnice. C0 sa používa na výpočet distribučného objemu a eliminačnej konštanty. Vzorce na výpočet Ct a Cl uvedené pre jednokomorový model sa používajú aj počas eliminačnej fázy pre lieky, ktoré spĺňajú podmienky dvojkomorového modelu.
53. Selektivita a špecifickosť účinku liečiva. Terapeutické, vedľajšie a toxické účinky liečiv, ich podstata z hľadiska pojmu receptory. Terapeutická stratégia boja proti vedľajším a toxickým účinkom liekov.
Špecifickosť- je to vtedy, keď sa liek viaže na typ receptora, ktorý je preň striktne špecifický.
Selektivita- vtedy sa liek dokáže viazať na jeden alebo viacero typov receptorov presnejšie ako iné.
Je vhodnejšie použiť termín selektivita, pretože je nepravdepodobné, že by sa ktorákoľvek molekula liečiva mohla viazať len na jeden typ receptorovej molekuly, pretože počet potenciálnych receptorov u každého pacienta má astronomický význam.
Terapeutické pôsobenie - hlavný požadovaný farmakologický účinok očakávaný od daného farmakologického prípravku.
Vedľajšie účinky- tie účinky, ktoré sa vyskytujú, keď sa látky používajú v terapeutických dávkach a tvoria spektrum ich farmakologického účinku.
Toxické účinky- nežiaduce účinky prejavujúce sa u tohto lieku, keď opustí terapeutické rozmedzie.
Vzťahy medzi terapeutickými a toxickými účinkami liekov na základe analýzy mechanizmov receptor-efektor:
1) terapeutické a toxické účinky sprostredkované rovnakým mechanizmom receptor-efektor (prazosín pôsobí ako alfa-selektívny antagonista na vaskulárnych SMC receptoroch a má hypotenzívny účinok pri esenciálnej hypertenzii, ale pri vysokých dávkach môže pacient pociťovať posturálnu hypotenziu)
2) terapeutické a toxické účinky sprostredkované rovnakými receptormi, ale odlišnými tkanivami alebo rôznymi efektorovými dráhami (srdcové glykozidy sa využívajú na zvýšenie kontraktility myokardu, zároveň narúšajú funkciu gastrointestinálneho traktu, videnie v dôsledku blokády Na + / K + -ATPáza bunkovej membrány)
3) sprostredkované terapeutické a toxické účinky odlišné typy receptory (napríklad norepinefrín má hypertenzný účinok prostredníctvom a1-Ap, ale súčasne spôsobuje tachykardiu prostredníctvom b1-Ap)
Terapeutická stratégia boja proti terapeutickým a vedľajším účinkom liekov:
1.Droga sa má vždy podávať v najmenšej dávke, ktorá spôsobí prijateľný terapeutický účinok
2. Zníženie dávky jedného lieku v dôsledku vymenovania iného lieku s podobným účinkom, ale prostredníctvom rôznych receptorov a s iným profilom toxicity.
3. Selektivitu účinku liečiva možno zvýšiť riadením koncentrácie liečiva v oblasti receptorov rôznych častí tela (lokálne užívanie liečiv - inhalačné použitie salbutamolu pri bronchiálnej astme)
Informácie o čase absorpcie, distribúcie a eliminácie, teda o farmakokinetike liečivých látok, možno vyjadriť matematicky. Je to nevyhnutné pri plánovaní schém klinického použitia liekov. Na základe farmakokinetických údajov sa vyvíjajú princípy racionálneho výberu a dávkovania týchto liekov. Súčasne s týmito výpočtami je potrebné neustále klinické sledovanie účinku lieku, pretože farmakokinetické štúdie len dopĺňajú túto kontrolu a umožňujú vyvodiť objektívnejšie závery.
Eliminácia väčšiny liečivých látok prebieha v súlade s exponenciálnou kinetikou, a to tak, že za každý rovnaký časový úsek zmizne z tela konštantná časť z celkového množstva podanej liečivej látky. Vo väčšine prípadov sa rýchlosť, akou liečivo zmizne z tela, odráža v zodpovedajúcej rýchlosti poklesu plazmatických hladín liečiva.
Koncentrácia liečiv v biologických tekutinách sa stanovuje kvapalinovou alebo plynovo-kvapalinovou chromatografiou, rádioimunoanalýzou alebo enzymatickou analýzou, polarografiou alebo spektrofotometriou. Opakované stanovenie koncentrácie liečiva v krvi počas liečby sa nazýva TERAPEUTICKÉ MONITOROVANIE. Na tento účel sa niekedy používajú sliny, čo je ultrafiltrát krvi bez bielkovín.
Na základe získaných hodnôt sa vykreslí graf, na vodorovnej osi je vyznačený čas odberu vzoriek a na zvislej osi je koncentrácia liečiva v biologickej vzorke (najčastejšie v krvnej plazme) v príslušných jednotkách. Výsledná krivka charakterizuje farmakokinetické procesy vyskytujúce sa s liečivom. Takže po jednej intravenóznej injekcii koncentrácia liečiva v plazme klesá exponenciálne. Rýchlosť exponenciálneho procesu možno charakterizovať pomocou rýchlostnej konštanty (K), ktorá odráža zmenu koncentrácie za jednotku času alebo počas periódy semi-exponenciálneho procesu (označuje sa ako T 1/2 alebo t / 2). Toto obdobie sa rovná času, ktorý je potrebný na dokončenie procesu o 50 %.
Elimináciu liečiv z tela možno posudzovať podľa polčasu alebo polčasu, polčasu, polčasu, ktorý je definovaný ako čas, za ktorý sa koncentrácia liečiva v krvi zníži o 50 % podaného množstva. liečiva alebo elimináciu 50 % biologicky dostupného množstva liečiva.
Pojem "POLOLIMINAČNÉ OBDOBIE" je úspešnejší ako "POLELIMINAČNÉ OBDOBIE", keďže liečivá sa nielen vylučujú, ale aj biotransformujú. Polčas eliminácie možno určiť z grafu koncentrácie a času meraním časového intervalu, v ktorom sa akákoľvek koncentrácia látky na krivke znížila o polovicu.
Prakticky je dôležité mať na pamäti, že v jednom polčase rozpadu
50 % liečiva sa vylúči z tela, 75 % počas dvoch období, 90 % počas troch období, 94 % počas štyroch období.
Keďže úplná eliminácia exponenciálneho typu si vyžaduje čas dlhší ako štyri (4) polčasy, potom pri opätovnom podávaní lieku v kratších intervaloch je zaznamenaná jeho kumulácia (akumulácia). Odhaduje sa, že na dosiahnutie plató koncentrácie, t.j. konštantnej koncentrácie liečiva v plazme, sú potrebné približne štyri obdobia biologického polčasu liečiva.
Je dôležité, že zníženie eliminácie liečiva vedie k predĺženiu biologického polčasu a predĺženiu účinku liečiva.
Pri niektorých liekoch môže byť farmakologický účinok dlhší, ako by naznačoval t/2. V tomto ohľade sa lieky, ako je rastový hormón, anaprilín, môžu podávať v intervaloch dlhších, ako je ich T/2.
Aby sa predišlo nebezpečnému zvýšeniu plazmatickej hladiny lieku u pacientov so zníženou elimináciou v prípade poruchy funkcie pečene, obličiek alebo kardiovaskulárneho systému, jeho udržiavacie dávky by sa mali znížiť buď znížením každej dávky, alebo proporcionálnym predĺžením intervalov medzi podaním k predĺženiu ich biologického polčasu....
BIOLOGICKÁ DOSTUPNOSŤ LIEKOV
Aby sa dosiahol terapeutický účinok, musí byť liečivá látka dodaná do tých orgánov alebo tkanív, v ktorých sa uskutočňuje jej špecifický účinok (v biofáze). Pri intravaskulárnej injekcii liek okamžite a úplne vstúpi do krvného obehu. Pri iných spôsoboch podania (orálne, intramuskulárne, subkutánne atď.) musí liek pred vstupom do krvného obehu prejsť cez množstvo biologických bunkových membrán (žalúdočná sliznica, pečeňové bunky, svaly atď.) a až potom niektorá časť dostane sa do systémového obehu. Účinok liečiva do značnej miery závisí od toho, koľko z podanej dávky liečiva sa dostane do systémového obehu. Tento indikátor charakterizuje biologickú dostupnosť činidla (F). Biologická dostupnosť liečiva teda v podstate odráža jeho koncentráciu na receptoroch, to znamená v krvi a telesných tkanivách po absorpcii. Prirodzene, biologická dostupnosť toho istého činidla bude u každého pacienta odlišná. Je zrejmé, že pri intravenóznom podaní liečiva je jeho biologická dostupnosť približne 100 % a pri iných spôsoboch podávania biologická dostupnosť takmer nikdy nedosahuje 100 %.
Rozlišujte medzi ABSOLÚTNYMI A RELATÍVNYMI BIOLOGICKÝMI DOSTUPNOSŤAMI. Absolútna biologická dostupnosť je pomer absorbovaného liečiva počas extravaskulárneho podania vo vzťahu k jeho množstvu po intravenóznom podaní.
Dôležitým ukazovateľom je RELATÍVNA BIODOSTUPNOSŤ, ktorá určuje relatívny stupeň absorpcie liečiva z testovaného liečiva a z referenčných liečiv. Inými slovami, relatívna biologická dostupnosť sa určuje pre rôzne série liekov, pre lieky pri výmene
výrobná technológia, pre lieky vyrábané rôznymi výrobcami, pre rôzne liekové formy. Na stanovenie relatívnej biologickej dostupnosti možno použiť údaje o hladine liečivej látky v krvi alebo o jej vylučovaní močom po jednorazovom alebo viacnásobnom podaní. Tento pojem je dôležitý pri vzájomnom porovnaní 2 liekov.
Porovnávacia biologická dostupnosť tých istých liekov vyrobených rôznymi spoločnosťami (príklad: kokarboxináza poľského pôvodu a vyrobená v Dnepropetrovsku) sa určuje porovnaním chemických, biologických a terapeutických ekvivalencií.
CHEMICKÁ EKVIVALENCIA je náhoda nielen v liekoch chemický vzorec liečiv, ale aj koincidencie izomérie, priestorovej konfigurácie atómov v molekule liečiva.
BIOLOGICKÁ EKVIVALENCIA znamená rovnakú, rovnakú koncentráciu účinnej látky v krvi pri užívaní lieku od rôznych spoločností.
Nakoniec, TERAPEUTICKÁ EKVIVALENCIA znamená rovnaký, ekvivalentný terapeutický účinok.
Ak sú uvedené 3 charakteristiky rovnaké, hovorí sa, že lieky majú rovnakú biologickú dostupnosť (biologickú dostupnosť). V súčasnosti existuje veľa príkladov, že podobné lieky sú biologicky neekvivalentné v dôsledku rozdielov v biologickej dostupnosti. Praktický lekár by na to mal pamätať najmä pri prechode pacienta z jedného lieku na podobný liek od inej spoločnosti.
Samozrejme, na všetky tieto otázky môže odpovedať iba nová veda – a to KLINICKÁ FARMAKOLÓGIA. Je to nezávislá veda s vlastným predmetom a výskumnými cieľmi. Prečo vynikla ako samostatný subjekt? V prvom rade preto, že, ako sa ukázalo, nie všetko sa dá študovať v pokuse na zvieratách. Napríklad duševné procesy, ktoré sú vysoko charakteristické len pre ľudí.
Rýchly rozvoj farmaceutického priemyslu viedol k vytvoreniu obrovského množstva liekov. Objavila sa lavína drog, ktorá vytvorila akúsi liečivú džungľu. Súčasná situácia veľmi sťažuje výber správneho lieku aj v jednej skupine liekov, bráni lekárovi orientovať sa v lieku, ktorý je pre konkrétneho pacienta optimálny. Na všetky tieto otázky pomáha odpovedať klinická farmakológia.
Ako príklad môžeme uviesť možnosť výberu lieku na kolagenózy (ochorenia spojivového tkaniva, reumatoidná artritída, reumatizmus, systémový lupus erythematosus atď.). S jedným
strany - kyselina acetylsalicylová (aspirín), ale zároveň existujú aj iné moderné nenarkotické analgetiká, ktoré majú v porovnaní s aspirínom množstvo výhod: naproxén, piroxikam atď.
Čo je lepšie, ktorý liek bude pre daného pacienta vhodnejší, ktorý má najvýraznejší terapeutický účinok? Na tieto otázky pomáha odpovedať klinická farmakológia.
Hlavné úlohy klinického farmakológa sú:
1) Výber liekov na liečbu špecifickej bolesti
2) Určenie pre neho najvhodnejších liekov
formy a spôsob ich aplikácie.
3) Voľba spôsobu podania lieku.
4) Sledovanie účinku lieku.
Na tento účel sú nainštalované senzory, ktoré poskytujú konštantný obraz o koncentrácii liečiva v krvi na monitore. Všetky ostatné aspekty farmakokinetiky sa skúmajú.
5) Štúdium nežiaducich reakcií a vedľajších účinkov na lieky, ich eliminácia, ako aj štúdium dôsledkov liekových interakcií u daného pacienta.
6) Prenos nahromadených vedomostí prostredníctvom školenia.
7) Organizácia laboratória a informačné služby a poradenstvo v oblasti plánovania výskumu (WHO, 1971).
FARMAKODYNAMIKA (PD) je odbor farmakológie, ktorý študuje
1) mechanizmy účinku (to znamená podstata procesov interakcie s tkanivovými, bunkovými alebo subcelulárnymi receptormi - špecifickými alebo nešpecifickými) 1.
1 02) farmakologické účinky (t. j. obsah a zmeny účinku lieku v závislosti od veku, pohlavia pacienta, povahy a priebehu ochorenia, sprievodnej patológie), ako aj 3) lokalizácie lieku akcie. Stručne povedané, PD možno definovať ako odvetvie farmakológie, ktoré študuje účinok liekov na organizmus.
Mechanizmus účinku lieku sa zvyčajne študuje na pokusoch na zvieratách, pretože u zvierat a ľudí sú takmer vždy rovnaké. Znalosť mechanizmu účinku lieku umožňuje lekárovi inteligentne vybrať liek potrebný na liečbu.
Existuje veľa mechanizmov účinku liekov, ale všetky môžu byť podmienene znížené na 2 skupiny.
Prvá skupina mechanizmov je spojená s tými prípadmi, keď lieky pôsobia na špecifické receptory – to znamená, že ide o MECHANIZMY RECEPTOROV.
Druhá skupina mechanizmov je spojená s liečivami, ktoré pre svoje fyzikálno-chemické vlastnosti nepôsobia cez receptory. Tu možno v prvom rade naznačiť účinok liečiv na špecifické enzýmy, ich fyzikálno-chemický účinok na bunkové membrány a priamu chemickú interakciu s bunkovými látkami.
Príkladom nereceptorových mechanizmov je
prípad s liekmi na anestéziu, povedzme s fluorotánom. Je výborným rozpúšťadlom pre tuky, preto pôsobí predovšetkým na membrány nervových buniek, pričom vyvoláva farmakologický efekt – anestéziu.
Pozrime sa na hlavné, najčastejšie nájdené receptory a mechanizmy účinku liekov.
Z farmakologického hľadiska sú receptory funkčné biochemické makromolekulárne membránové štruktúry, ktoré sú selektívne citlivé na pôsobenie určitých chemických zlúčenín a v našom prípade na pôsobenie liečiv. Výskum v posledných rokoch ukázali, že farmakologické receptory sú proteíny alebo enzýmy (G-proteíny sú jeden peptidový reťazec 7 domén) - to je ich zásadný rozdiel od morfologických receptorov.
Selektívna citlivosť liečiva na receptor znamená skutočnosť, že liečivo sa môže po prvé viazať na receptor, to znamená, že má k nemu afinitu alebo afinitu. Inými slovami, afinita alebo afinita sa týka schopnosti liečiva viazať sa na receptor.
Afinita alebo afinita odráža kinetické konštanty, ktoré viažu liečivo, receptor a odpoveď na molekulárnej úrovni. Interakcia liečivých látok s receptorom vedie k vzniku množstva biochemických a fyziologických zmien v tele, ktoré sa prejavujú jedným alebo druhým účinkom.
Druhou charakteristikou liečivej látky je jej schopnosť vyvolať farmakologickú odpoveď, účinok po interakcii s receptorom. Táto schopnosť sa označuje ako vnútorná aktivita lieku alebo jeho účinnosť. Biologická odpoveď je do určitej miery regulovaná zmenou počtu receptorov a ich citlivosti.
V priebehu evolúcie sa vytvorili receptory, ktoré sú citlivé na rôzne endogénne regulátory. Podľa teórie receptorov je mechanizmom účinku liekov zmena rýchlosti fungovania špecifických systémov tela, keď na receptory pôsobia prirodzené mediátory alebo exogénne látky.
Lieky, ktorých účinok je spojený s priamou excitáciou alebo zvýšením funkčných schopností (schopností) receptorov, sa nazývajú AGONISTY a látky, ktoré interferujú s účinkom špecifických agonistov, sa nazývajú ANTAGONISTY. Inými slovami, ak má liek obe charakteristiky (to znamená afinitu aj vnútornú aktivitu), potom je agonistom. Preto je agonista látka s vysokou afinitou k receptoru a vysokou vnútornou aktivitou. Ak má látka schopnosť len sa viazať na receptor (teda má afinitu), no zároveň nie je schopná vyvolať farmakologické účinky, potom spôsobí blokádu receptora a nazýva sa antagonista.
Lieky, ktoré majú rovnakú afinitu k receptoru ako agonista alebo slabšiu, ale menej výraznú vnútornú
sa nazývajú čiastočné agonisty alebo agonisty-antagonisty. Tieto lieky, používané súčasne s agonistami, znižujú účinok agonistov v dôsledku ich schopnosti obsadiť receptor.
Príklad: atropín – má vyššiu aktivitu ako acetylcholín (endogénny mediátor). Atropín interaguje s receptormi, ale keďže nemá žiadnu vnútornú aktivitu, nespôsobí fyziologický účinok. Vzhľadom na väčšiu afinitu k receptoru v porovnaní s acetylcholínom bude interferovať s pôsobením agonistu, menovite acetylcholínu, a preto bude jeho antagonistom.
Liečivé látky môžu pôsobiť podobne ako endogénne mediátory alebo naopak. Ak liečivá látka pôsobí ako mediátor (acetylcholín, norepinefrín atď.), nazýva sa MIMETIKA. Mim - koreň "mim", pantomíma, mimika. Preto cholinomimetikum, adrenergný agonista.
Liek, ktorý bráni interakcii mediátora s receptorom, sa nazýva blokátor (anticholínergný, adrenergný blokátor, blokátor histamínu atď.).
V literatúre sa môžete stretnúť s pojmom „lytic“ (lýza – rozpúšťanie, fyzikálny proces). Termín je dosť starý, ale niekedy sa používa (anticholinergikum, adrenolytikum). Pojmy „lytický“ a „blokátor“ sa teda používajú zameniteľne.
V lekárskej praxi sa stále viac používa súčasné vymenovanie niekoľkých liekov. Zároveň sa môžu vzájomne ovplyvňovať, meniť závažnosť a charakter hlavného účinku, jeho trvanie alebo oslabovať vedľajšie a toxické účinky. V tejto súvislosti je osobitná časť farmakodynamiky venovaná INTERAKCII LIEKOV, ktorá je klasifikovaná nasledovne. Rozlišujte FARMAKOLOGICKÚ interakciu a FARMACEUTICKÚ interakciu.
Farmaceutické interakcie sú spojené s farmaceutickou nekompatibilitou liekov počas ich výroby alebo skladovania, ako aj pri zmiešaní v jednej injekčnej striekačke. V tomto prípade sa predtým existujúca farmakologická aktivita liekov znižuje alebo zmizne a niekedy sa objavia aj nové toxické vlastnosti.
Farmakologická interakcia liekov je spojená so zmenami v ich farmakokinetike, farmakodynamike alebo na základe chemických a fyzikálno-chemických interakcií v prostrediach organizmu. V tomto prípade môžu lieky navzájom interagovať v ktorejkoľvek fáze ich prechodu cez telo pacienta: počas absorpcie, vo fáze transportu, v procese metabolizmu, ako aj pri vylučovaní (farmakokinetická interakcia).
Farmakodynamická interakcia odzrkadľuje zmenu spôsobenú každým liekom samostatne procesy spojené s realizáciou účinku. Inými slovami, farmakodynamický typ interakcie je založený na zvláštnostiach zmien v mechanizmoch a lokalizácii účinku použitých liekov, ich hlavných účinkoch. Ak interakcia prebieha na úrovni receptorov, tak sa to týka najmä agonistov a antagonistov rôznych typov receptorov. V tomto prípade môže jedna liečivá látka zosilniť alebo oslabiť účinok inej. Ak liečivá ve
Látky pôsobia vo vzťahu k účinku jednosmerne – ide o synergické liečivá (syn – spolu, ergo – fungujú). Synergizmus je teda sprevádzaný zvýšením konečného efektu. Zvyčajne tieto lieky pôsobia na rovnaké receptory. Existujú 2 varianty synergie:
1) Účinky sú rovnaké na princípe jednoduchého súčtu. Zhrnuté (alebo aditívum, - lat. - additio - sčítanie). Účinok sa pozoruje jednoduchým sčítaním účinkov každej zo zložiek. Napríklad takto interagujú lieky na anestéziu (oxid dusný + fluorotán). Variant aditívneho účinku je podobný pri súčasnom použití aspirínu a analgínu. Prečo to potrebujete vedieť? Ak je pacient nútený užívať aspirín dlhší čas, je potrebné vziať do úvahy, že aspirín pôsobí ulcerogénne, to znamená, že spôsobuje ulceráciu gastrointestinálnej sliznice a Analgin má taký nežiaduci účinok, ako je inhibícia hematopoézy. S prihliadnutím na aditívny analgetický účinok je možné znížiť bez zásadného rizika jeho vzniku, výrazne znížiť dávkovanie oboch liekov, ktoré pacient užíva.
2) Druhou verziou synergie je zosilnenie alebo zosilnenie účinku. Táto možnosť nastáva vtedy, keď po zavedení dvoch látok celkový účinok prevýši súčet účinkov oboch činidiel. Príkladom je interakcia antipsychotík (aminazín) a anestetík, interakcia antibiotík a antimikrobiálnych sulfonylamidov.
Niekedy sa rozlišuje tretí (3) variant synergizmu - senzibilizácia. Senzibilizácia - keď jeden liek v minimálnej dávke zosilňuje účinok druhého v ich kombinácii (použitie malých dávok inzulínu v kombinácii s KCl zvyšuje úroveň prieniku draslíka do buniek).
Okrem synergie je tu fenomén antagonizmu. Schopnosť jednej látky znížiť účinok inej do tej či onej miery sa nazýva ANTAGONIZMUS, to znamená, že v tomto prípade jeden liek bráni účinku druhého.
Existujú fyzikálne, chemické a fyziologické antagonizmy. Tento typ interakcie sa najčastejšie používa v prípade predávkovania alebo akútnej otravy liekmi. Príkladom FYZIKÁLNEHO antagonizmu môže byť schopnosť adsorpčných činidiel brániť vstrebávaniu látok z tráviaceho traktu (aktívne uhlie, ktoré adsorbuje jed na svojom povrchu; cholestyramín).
Ilustráciou CHEMICKEJ interakcie môže byť tvorba komplexónov (ióny niektorých ťažkých kovov - ortuť, olovo - viažu penicilamín, EDTA), alebo takto interaguje žalúdočná kyselina chlorovodíková a hydrogénuhličitan sodný (zásady).
FYZIOLOGICKÝ antagonizmus je spojený s liekovými interakciami na úrovni receptorov, ktorých povaha bola už spomenutá vyššie.
Analogicky k synergizmu sa rozlišuje PRIAMY (keď obidve liečivé zlúčeniny pôsobia na rovnaké receptory) a NEPRIAME (odlišná lokalizácia účinku liečiva) antagonizmus. Na druhej strane, priamy antagonizmus je KONKURENČNÝ a NIE
KONKURENCIESCHOPNÝ. Pri kompetitívnom antagonizme sa liek dostáva do kompetitívneho vzťahu s prirodzenými regulátormi (mediátormi) pre väzbové miesta v špecifických receptoroch. Blokáda receptora spôsobená kompetitívnym antagonistom môže byť uvoľnená vysokými dávkami agonistu alebo prirodzeného mediátora.
Nekompetitívny antagonizmus je situácia, keď liek nemôže vytesniť prirodzený mediátor z receptora, ale vytvára s ním kovalentné väzby (mediátor).
BODY INTERAKCIE LIEKOV Hlavný
hmota receptorov sa nachádza na vonkajšej a vnútri membrány bunky a jej organely. Medzi najčastejšie body liekovej interakcie patria: 1) mediátory a hormonálne receptory; 2) ATP-fáza Na/K pumpy, Ca, K a Na - intramembránové kanály.
Ten opäť dokazuje, že lieky pôsobia na dostupné kľúčové mechanizmy biologických reakcií, teda na fylogeneticky determinované procesy, a nie vytváraním nejakých nových reakcií.
K interakcii liečiv s receptorom dochádza na úrovni chemických alebo fyzikálno-chemických procesov. Povaha reakcie, jej sila, reverzibilita a trvanie sú najčastejšie spôsobené vlastnosťami spojenia lieku s receptorom. Sila väzby závisí od vzdialenosti elektrostatickej interakcie medzi dvoma atómami. Povaha interakcie je spravidla zložitá, môže zahŕňať rôzne druhy komunikácia, ktorá je určená komplementaritou lieku a receptora, mierou ich vzájomnej konvergencie.
Najslabšie spojenia sú van der Waals (určujú špecifickosť interakcie látok s reaktívnymi systémami). Vo väčšine prípadov vznikajú iónové väzby medzi liečivom a receptorom (reverzibilné).
TYPY ÚČINKU LIEKOV
1) LOKÁLNY ÚČINOK - pôsobenie látky, ku ktorému dochádza v mieste jej aplikácie. Príklad: použitie lokálnych anestetík – zavedenie roztoku dikaínu do spojovkovej dutiny. Použitie 1% roztoku novokaínu počas extrakcie
zub. Tento termín (lokálne pôsobenie) je trochu svojvoľný, pretože skutočne lokálny účinok sa pozoruje veľmi zriedkavo, pretože látky môžu byť čiastočne absorbované alebo majú reflexný účinok.
2) REFLEXNÉ PÔSOBENIE - je to vtedy, keď liek pôsobí na dráhy reflexu, to znamená, že ovplyvňuje extero- alebo interoreceptory a účinok sa prejaví zmenou stavu buď zodpovedajúcich nervových centier alebo výkonných orgánov. Takže použitie horčicových náplastí na patológiu dýchacieho systému reflexne zlepšuje ich trofizmus (éterický horčičný olej stimuluje exteroreceptory kože). Liek cytiton (respiračné analeptikum) pôsobí vzrušujúco na chemoreceptory karotického glomerulu a reflexnou stimuláciou centra dýchania zvyšuje objem a frekvenciu dýchania. Ďalším príkladom je použitie amoniaku pri mdlobách (amoniak), ktorý sa reflexne zlepšuje
cerebrálny obeh a tonické vitálne centrá.
3) RESORPTÍVNE PÔSOBENIE - je to vtedy, keď sa účinok látky rozvinie po jej absorpcii (resorpcia - absorpcia; latinsky - resorbeo - absorbujem), vstupom do celkového krvného obehu a potom do tkanív. Resorpčný účinok závisí od spôsobu podania liečiva a jeho schopnosti prenikať cez biologické bariéry. Ak látka interaguje len s funkčne jednobodovými receptormi určitej lokalizácie a neovplyvňuje iné receptory, pôsobenie takejto látky sa nazýva SELEKČNÉ. Takže niektoré kurariformné látky (svalové relaxanciá) celkom selektívne blokujú cholinergné receptory koncových platničiek, čo spôsobuje relaxáciu kostrového svalstva. Účinok lieku prazosín je spojený so selektívnym blokovaním postsynaptických alfa-on adrenergných receptorov, čo v konečnom dôsledku vedie k zníženiu krvného tlaku. Základom selektivity účinku liečiv (selektivita) je afinita (afinita) látky k receptoru, ktorá je určená prítomnosťou určitých funkčných skupín v molekule týchto látok a všeobecnou štruktúrnou organizáciou látky. , čo je najvhodnejšie pre interakciu s týmito receptormi, teda ÚPLNOSŤ.
VŠEOBECNÁ CHARAKTERISTIKA ÚČINKU DROG NA ORGANIZMUS
Napriek množstvu liekov, všetko obrovské
nimi spôsobené v tele, majú určitú spoločnú a
jednotnosť. Na základe konceptu reakčnej rýchlosti existuje 5
typy zmien
spôsobené farmakologickými látkami (N.V. Vershinin):
1) tónovanie (zvýšenie funkcie na normálnu);
2) vzrušenie (zvýšená funkcia nad normu);
3) upokojujúci účinok (sedatívum), to znamená zníženie zvýšenej funkcie na normálnu;
4) útlak (zníženie funkcie pod normál);
5) paralýza (ukončenie funkcie). Množstvo tonika a košíka
prebúdzací efekt sa nazýva prebúdzacia akcia.
HLAVNÉ ÚČINKY LIEKOV
V prvom rade sa rozlišuje:
1) fyziologické účinky, keď lieky spôsobujú zmeny, ako je zvýšenie alebo zníženie krvného tlaku, srdcovej frekvencie atď.;
2) biochemické (zvýšené hladiny enzýmov v krvi, glukózy
Shl atď.). Okrem toho existujú ZÁKLADNÉ (alebo hlavné) a
SEKUNDÁRNE (malé) účinky liekov. ZÁKLADNÉ EF
SKUTOČNOSŤ je tá, z ktorej vychádza lekár pri svojich výpočtoch pri liečbe tohto (!) pacienta (analgetiká - pre analgetický účinok, antihypertenzíva - na zníženie krvného tlaku atď.).
DÔLEŽITÉ, alebo nie hlavné účinky, dodatočné, inak také, ktoré sú tomuto lieku vlastné, ale ktorých vývoj u tohto pacienta nie je potrebný (nenarkotické analgetiká - okrem analgetického účinku spôsobujú aj antipyretický účinok, atď.). Vedľajšie účinky môžu zahŕňať VÝHODY a NEŽIADUCE (alebo VEDĽAJŠIE) účinky.
Príklad. Atropín - uvoľňuje hladké vnútorné svaly
orgánov. Zároveň však zlepšuje vedenie v AV uzle srdca (so srdcovou blokádou), zväčšuje priemer zrenice atď. Všetky tieto účinky je potrebné posudzovať individuálne v každom konkrétnom prípade.
FAKTORY OVPLYVŇUJÚCE HODNOTU ÚČINKU DROG
1) Najprv si musíte pamätať na farmakokinetické faktory, ktoré sú vlastné každému lieku. To už bolo spomenuté vyššie, len pripomeniem, že hovoríme o jeho rýchlosti vstrebávania alebo vstrebávania, biotransformácie, vylučovania (liek, liek).
2) Druhá skupina faktorov je fyziologická.
a) Vek. Každý naozaj dobre vie, že citlivosť pacienta na lieky sa vekom mení. Vynikli aj v tomto smere:
perinatálna farmakológia;
Pediatrická farmakológia;
geriatrická farmakológia;
reprodukčná farmakológia;
b) Hmotnosť pacienta. Je známe, že čím väčšia hmotnosť, tým vyššia
dávka. Preto sa lieky dávkujú v (mg / kg).
c) Pohlavie. Odhalená rozdielna citlivosť u mužov a žien
určité látky, napríklad nikotín, alkohol atď.,
čo sa vysvetľuje rozdielom v metabolizme, rozdielom v špecifických
hmotnosť telesného tuku atď.
c) Stav organizmu. Účinok liekov na organizmus po su
sociálnej fyzická aktivita bude iný ako bez neho.
e) Biologické rytmy (denné, mesačné, sezónne, ročné
vye, a teraz už aj obyvateľov) majú najvážnejšie
vplyv na pôsobenie liečiv v organizme. 3) Patologické fakty
ry (napríklad úroveň hormonálnej aktivity). Takže s ba
toxické dávky morfínu sú ľahšie tolerované, ale zvyšuje sa citlivosť myokardu na adrenalín. 1 0 Účinok srdcových glykozidov na krvný obeh sa prejavuje iba na pozadí srdcového zlyhania. Účinok liekov sa výrazne mení pri hypo- a hypertermii, pri infekčných ochoreniach, pri zmene funkčného stavu centrálneho nervového systému a pod.).
4) Genetické faktory. Je známe, že absencia enzýmu glukózo-6-fosfátdehydrogenázy (G-6-FDG) v talasénii znemožňuje predpisovať antimalariká, ako je primachín. Nedostatok enzýmu butyrylcholínesterázy v krvi, ktorý sa vyskytuje u jedného z 2500 ľudí, je príčinou predĺženej svalovej relaxácie po podaní ditilínu.
5) Poddajnosť pacientov alebo placebo efekt. V tomto smere dosahuje antianginózny účinok napríklad placebo liekov 40 % a až 81 % placebo efektu vzniká injekčnou cestou podania lieku. To je pravdepodobne dôvod, prečo je používanie vitamínových prípravkov, tonikov, trankvilizérov z veľkej časti spôsobené týmto účinkom.
6) Dávka lieku. Účinok liekov je do značnej miery určený ich dávkou. Dávka sa vzťahuje na množstvo liečivej látky
jednorazová dávka (zvyčajne označovaná ako jednorazová dávka). Dávka lieku závisí nielen od účinnosti liečby, ale aj od bezpečnosti pacienta. Na konci 18. storočia William Withering napísal: „Jed v malých dávkach – najlepší liek; užitočný liek v príliš veľkej dávke je jed.“ O to správnejšie je to v dnešnej dobe, keď sa do lekárskej praxe zaviedli mimoriadne účinné lieky, ktorých dávky sa merajú v zlomkoch miligramu.
Uveďte dávku v gramoch alebo zlomkoch gramu. Pre presnejšie dávkovanie liekov sa ich množstvo vypočíta na 1 kg telesnej hmotnosti (alebo na 1 m2 plochy tela), napríklad 1 mg / kg; 1 μg / kg atď. Lekár sa musí orientovať nielen v dávke vypočítanej na jednorazovú dávku (pro dosi), ale aj v dennej dávke (pro die).
Minimálne dávky, pri ktorých lieky spôsobujú počiatočný biologický (terapeutický) účinok, sa nazývajú prahové alebo minimálne účinné (terapeutické) dávky. V praktické lekárstvo najčastejšie sa používajú priemerné terapeutické dávky, pri ktorých liečivá poskytujú potrebný optimálny farmakoterapeutický účinok. Ak pri ich predpisovaní pacientovi nie je účinok dostatočne výrazný, dávka sa zvýši na najvyššiu terapeutickú dávku. Vyššie terapeutické dávky môžu byť jednorazové a denné. Najvyššia jednotlivá dávka je maximálne množstvo liečiva, ktoré možno podať jednorazovo bez poškodenia pacienta. Tieto dávky sa používajú zriedkavo, v extrémnych prípadoch (v naliehavých, núdzových situáciách). Priemerné terapeutické dávky sú zvyčajne 1/3-1/2 najvyššej jednotlivej dávky.
Najvyššie terapeutické dávky jedovatých a silných látok sú uvedené v Štátnom liekopise ZSSR. V niektorých prípadoch, napríklad pri použití chemoterapeutických činidiel, je dávka liečiva indikovaná pre priebeh liečby (kurzová dávka). Ak je potrebné rýchlo vytvoriť vysokú koncentráciu liečiva v tele (sepsa, kardiovaskulárne zlyhanie), použite prvú dávku, takzvanú nárazovú dávku, ktorá prevyšuje všetky nasledujúce. Existujú aj toxické (nebezpečné účinky) a smrteľné dávky.
Pre lekára je dôležité poznať ešte jednu charakteristiku – a to koncept šírky terapeutického pôsobenia lieku. Pod šírkou terapeutického účinku sa rozumie vzdialenosť, rozsah od minimálnej terapeutickej dávky po minimálnu toxickú dávku. Prirodzene, čím väčšia je táto vzdialenosť, tým je tento liek bezpečnejší.
1/20 dávky x vek dieťaťa.
Pre kvantitatívne charakteristiky a pri hodnotení účinnosti nového farmakologického činidla sa spravidla používajú dve štandardné porovnania - buď s placebom alebo s analogénom.
gický typ akcie, ktorý je jedným z najúčinnejších prostriedkov v tejto skupine.
Placebo (dummy) je indiferentná látka v liekovej forme, ktorá napodobňuje určité farmakologické alebo liečivo. Použitie placeba je nevyhnutné za prítomnosti: a) vplyvu presumptivity, vplyvu osobnosti, očakávaní a zaujatosti zo strany pacienta alebo výskumníka; b) spontánne zmeny priebehu ochorenia, symptómov, ako aj javov nesúvisiacich s liečbou.
Placebo je latinský výraz, ktorý znamená „môžem ťa potešiť“.
Placebo efekt je účinok spôsobený nie špecifickými farmakodynamickými vlastnosťami lieku pre danú patológiu, ale SKUTOČNOSŤOU UŽÍVANIA liekov, ktoré ovplyvňujú psychologicky. Placebo liečivá sú zvyčajne farmakologicky inertné a obsahujú neaktívne látky ako škrob alebo laktózu. Placebá sa používajú v klinických štúdiách na zistenie účinku sugescie zo strany pacienta aj lekára, najmä ak sa majú skúmať lieky určené na liečbu bronchiálnej astmy, hypertenzie, anginy pectoris, ochorenia koronárnych artérií. V takýchto prípadoch by sa placebo prípravok nemal líšiť farbou ani inými fyzikálnymi vlastnosťami (vôňa, chuť, tvar) od aktívneho prípravku. Placebo je účinnejšie, keď sú o ňom lekár aj pacient nedostatočne informovaní.
PRÍKLAD. Pri ischemickej chorobe srdca (ICHS), ak je jednej skupine pacientov s ICHS predpísané aktívne liečivo a druhé - placebo, potom u 40% pacientov v druhej skupine sa záchvaty angíny zastaví.
Najvýraznejší placebo efekt (až 81 %) sa pozoruje pri injekčnom spôsobe jeho podania. Lektvary a pilulky sú menej účinné.
Pojem FARMAKOTERAPIA (FT) sa často používa v literatúre o expozícii pacienta liekom. Farmakoterapia je časť farmakológie, ktorá študuje liekovú terapiu pacienta.
Existujú nasledujúce typy farmakoterapie:
1) ETIOTROPNÁ - ideálna forma farmakoterapie. Tento typ FT je zameraný na odstránenie príčiny ochorenia. Príkladom etiotropnej PT môže byť liečba infekčných pacientov antimikrobiálnymi látkami (benzylpenicilín pri streptokokovej pneumónii), použitie antidot pri liečbe pacientov s toxickými
látok. 2) PATOGENETICKÁ FARMAKOTERAPIA - riadená
eliminovať resp
potlačenie mechanizmov vývoja ochorenia. Väčšina v súčasnosti používaných liekov patrí špecificky do skupiny liekov patogenetickej FT. Antihypertenzíva, srdcové glykozidy, antiarytmiká, protizápalové, psychotropné a mnohé ďalšie lieky majú terapeutický účinok tým, že potláčajú zodpovedajúce mechanizmy rozvoja ochorenia.
3) SYMPTOMATICKÁ TERAPIA – zameraná na odstránenie resp
obmedzenie jednotlivých prejavov ochorenia. Symptomatické lieky zahŕňajú lieky proti bolesti, ktoré neovplyvňujú príčinu alebo mechanizmus ochorenia. Dobrým príkladom symptomatických liekov sú aj antitusiká. Niekedy tieto prostriedky (eliminácia syndróm bolesti s infarktom myokardu) môže mať významný vplyv na priebeh hlavného patologického procesu a zároveň zohrávať úlohu prostriedkov patogenetickej terapie.
4) SUBSTITUČNÁ FARMAKOTERAPIA sa využíva pri nedostatku prirodzených živín. Prostriedky substitučnej terapie zahŕňajú enzýmové preparáty (pankreatín, panzinorm atď.), hormonálne lieky (inzulín pri diabetes mellitus, tyreoidín pri myxedémoch), vitamínové preparáty (vitamín D napr. pri krivici). Lieky substitučnej terapie bez odstránenia príčin ochorenia môžu zabezpečiť normálnu existenciu tela po mnoho rokov. Nie je náhoda, že taká závažná patológia ako cukrovka- je medzi Američanmi považovaný za zvláštny životný štýl.
5) PREVENTÍVNA TERAPIA sa vykonáva na prevenciu chorôb. Medzi profylaktické lieky patria niektoré antivírusové látky (napríklad počas chrípkovej epidémie – remantadín), dezinfekčné prostriedky a množstvo ďalších. Za profylaktickú FT možno považovať aj užívanie liekov proti tuberkulóze, ako je izonizid. Vakcíny sú dobrým príkladom preventívnej liečby.
CHEMOTERAPIU treba odlíšiť od farmakoterapie. Ak sa FT zaoberá dvoma účastníkmi patologického procesu, a to liekom a makroorganizmom, potom počas chemoterapie sú už 3 účastníci: liek, makroorganizmus (pacient) a pôvodca ochorenia.
Keď už hovoríme o dávkach, primárne sme poukázali na alopatické dávky, na rozdiel od homeopatických. Preto pár slov o HOMEOPATII. Pojem "homeopatia" je odvodený z dvoch gréckych slov: homois - podobný a pathos - utrpenie, choroba. Doslova sa homeopatia prekladá ako podobná, podobná choroba. Zakladateľ homeopatie, nemecký vedec Samuel Hahnemann, vo svojom slávna kniha"Organon lekárskeho umenia alebo základná teória homeopatickej liečby" späť v začiatkom XIX storočia (1810) načrtol základné princípy tejto vedy. Existuje niekoľko princípov, ale 2 z nich sú základné:
1) Toto je zákon podobnosti, ktorý hovorí, že liečba chorôb sa musí vykonávať podobnými, podobnými prostriedkami. Podľa tohto princípu Hahnemann radí „napodobňovať prírodu, ktorá niekedy vylieči chronické ochorenie prostredníctvom inej sprievodnej choroby“. Preto „proti chorobe, ktorá sa má vyliečiť (hlavne chronickej), treba použiť takú liečivú látku, ktorá je schopná vyvolať inú, najpodobnejšiu umelú chorobu, a tá prvá sa vylieči. Similia
similibus (podobné podobnému). Napríklad žltačku treba liečiť žltou atď.
2) Druhou zásadou je liečiť super malými dávkami. Riedenie liekov používaných homeopatmi sa počíta v niekoľkých rádoch, niekedy ich dosahujú desiatky: 10 v piatom; 10 v desiatom; 10 na osemnástu alebo väčšiu mocninu (tj milión
a viac ako zlomok gramov). Na vysvetlenie účinku použitia le
sacharidové látky v
vysoké riedenia Hahnemann predložil špekulatívny koncept: "Malé dávky sa vyznačujú zvláštnou duchovnou silou, väčšou aktivitou, schopnosťou preniknúť do postihnutých orgánov a tkanív."
Nie je známe, čo so zvláštnou duchovnou silou, ale vedecký život v poslednom desaťročí predložil veľmi silný dôkaz o platnosti Hahnemannovho tvrdenia. Napríklad experimenty Francúza Jacquesa Bekvenisteho, ktoré vykonal s riedením látok 10 na osemdesiatu mocninu, ukázali, že molekuly vody majú „pamäť“ na prítomnosť danej látky, čo spôsobuje určitý fyziologický účinok. Ak sa táto skutočnosť zaznamenaná v blízkej budúcnosti potvrdí, teda ak sa zistí, či sú molekuly vody zdrojom informácií, určite budeme na základni. najväčší objav, schopný vysvetliť terapeutickú účinnosť homeopatických liekov.
Ďalej zvážte časť týkajúcu sa FARMAKOLOGICKÝCH ASPEKTOV TOXICKÉHO ÚČINKU DROG, konkrétne TOXIKOLÓGIE DROG. Toxikológia liekov je oblasť farmakológie, ktorá študuje toxické účinky týchto liekov. Teraz je však správnejšie hovoriť o nežiaducich reakciách ľudského tela na drogy. Táto skutočnosť je známa už dlho, nahromadilo sa množstvo faktografického materiálu, čo naznačuje, že pri užívaní takmer všetkých liekov sa môžu vyskytnúť nežiaduce reakcie rôzneho stupňa.
Existuje mnoho klasifikácií vedľajších účinkov liekov a komplikácií farmakoterapie, hoci žiadna nie je dokonalá. Zároveň na základe patogenetického princípu možno všetky nežiaduce účinky alebo reakcie rozdeliť do 2 typov:
1) nežiaduce reakcie spojené s
a) predávkovanie drogami
b) otravy;
2) toxické reakcie spojené s farmakologickými vlastnosťami liečiv.
K predávkovaniu zvyčajne dochádza pri použití vysokých dávok liekov. Obzvlášť často dochádza k predávkovaniu pri užívaní liekov s malou šírkou terapeutického účinku. Napríklad pri užívaní aminoglykozidových antibiotík (streptomycín, kanamycín, neomycín) je ťažké vyhnúť sa toxicite. Tieto lieky spôsobujú vestibulárne poruchy a hluchotu, keď sa liečia dávkami, ktoré nie sú oveľa vyššie ako terapeutické. Pri niektorých liekoch je jednoducho nemožné vyhnúť sa toxickým komplikáciám (antineoplastiká, cytotoxické lieky), ktoré poškodzujú všetky rýchlo sa deliace bunky a
Inertný mozog nezmizne a súčasne účinne ovplyvňuje rast nádorových buniek.
Okrem toho môže byť predávkovanie spojené nielen s použitím vysokých dávok, ale aj s fenoménom kumulácie (srdcové glykozidy).
Otrava môže byť náhodná alebo úmyselná. K úmyselnej otrave zvyčajne dochádza so samovražedným cieľom (samovražda). V regióne Omsk sú najčastejšie vo všeobecnej štruktúre otravy otravy kauterizačnými kvapalinami, na druhom mieste sú otravy drogami. Ide predovšetkým o otravu tabletkami na spanie, trankvilizérmi, FOS, alkoholom, oxidom uhoľnatým.
Napriek rozdielom v etiologických faktoroch sú opatrenia pomoci v štádiách lekárskej pomoci v zásade podobné.
Tieto zásady sú nasledovné:
1) BOJUJTE S NEOPAČOVANÝM JEDOM Z GASTROINTESTINÁLNEHO TRAKTU. Najčastejšie sa to vyžaduje pri orálnej otrave jedom. Najčastejšia akútna otrava je spôsobená požitím látok. Povinným a naliehavým opatrením v tomto smere je výplach žalúdka sondou aj 10-12 hodín po otrave. Ak je pacient pri vedomí, vykoná sa výplach žalúdka s použitím veľkého množstva vody a následné vyvolanie zvracania. Zvracanie sa vyvoláva mechanicky. V bezvedomí sa pacientovi vykoná výplach žalúdka cez hadičku. Je potrebné zamerať úsilie na adsorpciu jedu v žalúdku, na ktorý sa používa aktívne uhlie (1 polievková lyžica vo vnútri alebo 20-30 tabliet súčasne, pred a po výplachu žalúdka). Žalúdok sa po 3-4 hodinách niekoľkokrát premyje, kým sa úplne nezbaví látky.
Zvracanie je kontraindikované v nasledujúcich prípadoch:
S kómou;
V prípade otravy žieravými kvapalinami;
V prípade otravy petrolejom, benzínom (možnosť hydrokarbonátovej pneumónie s nekrózou pľúcneho tkaniva a pod.).
Ak je obeťou malé dieťa, potom je lepšie použiť na umývanie soľné roztoky v malých objemoch (100-150 ml).
Najlepšie je odstrániť jed z čriev pomocou slaných laxatív. Preto sa na konci výplachu môže do žalúdka zaviesť 100-150 ml 30% roztoku síranu sodného a ešte lepšie síranu horečnatého. Slané laxatíva sú najsilnejšie, rýchlo pôsobiace laxatíva v črevách. Ich pôsobenie podlieha zákonom osmózy, teda sú krátke obdobiečasom sa pôsobenie jedu ukončí.
Je dobré podávať adstringenty (roztoky trieslovín, čaj, vtáčia čerešňa), ako aj obaľujúce (mlieko, vaječný bielok, rastlinný olej).
V prípade kontaktu pokožky s jedom je potrebné pokožku dôkladne opláchnuť, najlepšie korkovou vodou. Ak sa toxické látky dostanú cez pľúca, ich vdychovanie by sa malo zastaviť odstránením obete z otrávenej atmosféry.
Pri subkutánnej injekcii toxickej látky možno jej absorpciu z miesta vpichu spomaliť injekciami roztoku adrenalínu
okolo miesta vpichu, ako aj ochladzovanie tejto oblasti (ľad na koži v mieste vpichu).
2) Druhým princípom pomoci pri akútnej otrave je ovplyvnenie vstrebaného jedu, jeho ODSTRÁNENIE Z TELA.
Aby sa toxická látka z tela čo najskôr odstránila, používa sa predovšetkým nútená diuréza. Podstata tejto metódy spočíva v kombinácii zvýšenej vodnej záťaže so zavedením aktívnych, silných diuretík. Telo sa zaplaví pitím veľkého množstva tekutín pacientovi alebo intravenóznou injekciou rôznych roztokov (roztoky krvnej náhrady, glukózy atď.). Z diuretík sa najčastejšie používa FUROSEMID (lasix) alebo MANNIT. Metódou nútenej diurézy tak trochu „umyjeme“ tkanivá pacienta, čím ich zbavíme toxických látok. Táto metóda dokáže odstrániť iba voľné látky, ktoré nie sú spojené s bielkovinami a krvnými lipidmi. Pozornosť by sa mala venovať rovnováhe elektrolytov, ktorá pri použití túto metódu môže byť narušená v dôsledku eliminácie značného množstva iónov z tela.
Pri akútnom kardiovaskulárnom zlyhaní, závažnej renálnej dysfunkcii a riziku rozvoja mozgového alebo pľúcneho edému je forsírovaná diuréza kontraindikovaná.
Okrem forsírovanej diurézy sa používa hemodialýza a peritoneálna dialýza, kedy krv (hemodialýza, alebo umelá oblička) prechádza cez semipermeabilnú membránu, zbavuje sa toxických látok, alebo sa vykonáva „premývanie“ peritoneálnej dutiny roztokom elektrolytu. .
MIMOTELOVÉ METÓDY DETOXIKÁCIE. Úspešnou metódou detoxikácie, ktorá sa rozšírila, je metóda HEMOSORPCIE (lymfosorpcie). V tomto prípade sú toxické látky v krvi adsorbované na špeciálnych sorbentoch (granulovaný uhlík obalený krvnými bielkovinami, alo slezina). Táto metóda umožňuje úspešnú detoxikáciu organizmu v prípade otravy neuroleptikami, trankvilizérmi, FOS atď. Metóda hemosorpcie odstraňuje látky, ktoré sa zle odstraňujú hemodialýzou a peritoneálnou dialýzou.
NÁHRADA KRVI sa používa, keď sa krvácanie kombinuje s transfúziou krvi darcu.
3) Treťou zásadou boja proti akútnej otrave je ZNEŠKODŇOVANIE PRISATÉHO JEDU zavedením ANTAGONISTOV a ANTIDOT.
Antagonisty sú široko používané pri akútnej otrave. Napríklad atropín na otravu anticholínesterázou, FOS; nalorfín - v prípade otravy morfínom a pod. Farmakologické antagonisty zvyčajne kompetitívne interagujú s rovnakými receptormi ako látky, ktoré otravu spôsobili. V tomto smere veľmi zaujímavo vyzerá tvorba ŠPECIFICKÝCH PROTILÁTOK (monoklonálnych) vo vzťahu k látkam, ktoré sú obzvlášť často príčinou akútnej otravy (monoklonálne protilátky proti srdcovým glykozidom).
Na špecifickú liečbu pacientov s otravou chemikáliami je účinná TERAPIA ANTIDOTE. ANTIDOTÁ sú činidlá používané na špecifické viazanie jedu, neutrálne
lízanie, inaktivácia jedov, či už chemickou alebo fyzikálnou interakciou.
Takže v prípade otravy ťažkými kovmi sa používajú zlúčeniny, ktoré s nimi tvoria netoxické komplexy (napríklad unitiol na otravu arzénom, D-penicilamín, desferal na otravu prípravkami železa atď.).
4) Štvrtou zásadou je vykonávanie SYMPTOMATICKEJ TERAPIE. Predovšetkým veľký význam symptomatická terapia sa získava v prípade otravy látkami, ktoré nemajú špeciálne antidotá.
Symptomatická terapia podporuje vitálne funkcie: OBEH a DÝCHANIE. Používajú srdcové glykozidy, vazotoniká, prostriedky zlepšujúce mikrocirkuláciu, oxygenoterapiu a stimulanty dýchania. Kŕče sa eliminujú injekciami sibazonu. S edémom mozgu sa uskutočňuje dehydratačná terapia (furosemid, manitol). užívajte analgetiká, upravte acidobázický stav krvi. Pri zástave dýchania je pacient preložený na umelú ventiláciu pľúc s komplexom resuscitačných opatrení.
Ďalej sa zameriame na DRUHÝ TYP NEŽIADUCICH ÚČINKOV, teda nežiaducich reakcií spojených s farmakologickými vlastnosťami liečiv. Nežiaduce účinky liekov sa prejavujú u 10 – 20 % ambulantných pacientov a 0,5 – 5 % pacientov potrebuje hospitalizáciu na nápravu liekových porúch. Tieto nežiaduce, z hľadiska patogenézy, reakcie môžu byť: a) PRIAMY a b) spojené so ZMENENOU CITLIVOSŤOU organizmu pacienta.
Pozrime sa na PRIAMY TOXICKÉ REAKCIE. Nazývajú sa priame, pretože drogy priamo, priamo toxické pre funkčný systém. Napríklad antibiotiká zo série aminoglykozidov (streptomycín, kanamycín, gentamicín) vykazujú NEUROTOXICITU, toxický účinok na sluchový orgán (ototoxicita) a vestibulárny aparát. Okrem toho túto triedu antibiotiká majú toxicitu vo vzťahu k behaviorálnym reakciám, prejavujú sa letargiou, apatiou, letargiou, ospalosťou.
Lieky môžu mať PRIAMY GLATOTOXICKÉ REAKCIE. Napríklad fluorotan (anestetické činidlo) pri opakovanom použití v krátkom čase môže mať výrazný toxický účinok až po akútnu žltú dystrofiu pečene.
Priame toxické účinky môžu byť realizované NEFROTOXICITOU. Tento účinok majú mycínové antibiotiká-aminoglykozidy. Pri predpisovaní liekov tejto série potrebuje pacient neustála kontrola na stav močových testov (bielkoviny, krv v moči a pod.).
Ďalším priamym toxickým účinkom je ULTSEROGÉNNY (ulcerózny). Napríklad vymenovanie salicylátov, glukokortikoidov, antihypertenzívum rezerpínu - vedie k ulcerácii žalúdočnej sliznice, čo sa musí brať do úvahy pri predpisovaní týchto tried liekov, najmä u pacientov, ktorí už trpia vredovou chorobou.
Priame toxické účinky možno vyjadriť v EMBRYOTOXICITE. Dovoľte mi pripomenúť, že nepriaznivé
účinok liekov, ktorý nie je spojený s porušením organogenézy, ku ktorému dochádza pred 12. týždňom tehotenstva. A toxický účinok liekov je viac neskoré obdobie tehotenstvo sa nazýva FETOTOXICKÉ. Na tento účinok je potrebné pamätať pri predpisovaní liekov pre tehotné ženy, pri vykonávaní farmakoterapie pre ne iba na prísne indikácie.
Príklady: 1) vymenovanie streptomycínu tehotným ženám môže viesť k hluchote plodu (poškodenie VIII páru hlavových nervov); 2) tetracyklíny nepriaznivo ovplyvňujú vývoj kostí u plodu; 3) u matky trpiacej na morfium môže byť novorodenec aj fyzicky závislý na morfiu.
Lieky môžu mať TERATOGENICitu, teda taký škodlivý vplyv na diferenciáciu tkanív a buniek, čo vedie k narodeniu detí s rôznymi anomáliami. Napríklad použitie talidomidu, ktorý má výrazný teratogénny účinok, ako sedatívum a hypnotikum, viedlo k pôrodu v krajinách západná Európa niekoľko tisíc detí s rôznymi deformáciami (fotomélia - plutvovité končatiny; amelia - absencia končatín; tvárové hemangióny, gastrointestinálne anomálie).
Na štúdium teratogénneho účinku látok sa skúma účinok liekov na zvieratá, hoci neexistuje priama súvislosť s účinkom liekov na zvieratá a ľudí. Napríklad v tom istom talidomide bola teratogenita v experimente na myšiach zistená pri dávke 250-500 mg / kg telesnej hmotnosti, zatiaľ čo u ľudí sa rovnala 1-2 mg / kg.
Najnebezpečnejší z hľadiska teratogénneho pôsobenia je prvý trimester (najmä obdobie 3-8 týždňov tehotenstva), teda obdobie organogenézy. Počas týchto období je obzvlášť ľahké spôsobiť závažnú anomáliu vo vývoji embrya.
Pri vytváraní nových liekov treba mať na pamäti aj možnosť takých závažných negatívnych účinkov, akými sú CHEMICKÁ MUTAGENCIA a KARCINOGENITA. MUTAGENCIA je schopnosť látok spôsobiť trvalé poškodenie zárodočnej bunky, ale najmä jej genetického aparátu, čo sa prejaví zmenou genotypu potomka. KARCINOGENITA je schopnosť látok vyvolať vývoj zhubných nádorov. Estrogény prispievajú k rozvoju rakoviny prsníka u žien vo fertilnom veku.
Mutagénne a teratogénne účinky sa môžu objaviť po mesiacoch alebo dokonca rokoch, čo sťažuje identifikáciu ich skutočnej aktivity. Teratogenita je vlastná antineoplastickým liekom, kortikosteroidom, androgénom, alkoholu. Cyklofosfamid a niektoré hormonálne činidlá majú karcinogénny účinok.
Nežiaduce reakcie pri užívaní drog môžu byť vyjadrené rozvojom DROGOVEJ ZÁVISLOSTI alebo globálnejšie DROGOVOU ZÁVISLOsťou. Existuje niekoľko hlavných príznakov závislosti.
1) Ide o prítomnosť DUŠEVNEJ ZÁVISLOSTI, teda takého stavu, keď sa u pacienta vyvinie neodolateľná duševná príťažlivosť k opakovanému podávaniu liečivej látky, napr.
liek.
2) FYZICKÁ ZÁVISLOSŤ - tento pojem označuje prítomnosť ťažkého telesného ochorenia u pacienta bez opätovného podania lieku, najmä lieku. Pri náhlom prerušení podávania lieku, ktorý spôsobil drogovú závislosť, vzniká fenomén DEPRIVÁCIE alebo ABSTINENCIE. Objavuje sa strach, úzkosť, melanchólia, nespavosť. Možno vzniká motorický nepokoj, agresivita. Mnohé fyziologické funkcie sú narušené. V závažných prípadoch môžu byť abstinenčné príznaky smrteľné.
3) Rozvoj TOLERANCIE, teda závislosti. Iné druhy
Nežiaduce účinky spôsobené vlastnosťami samotných liečiv sú poruchy spojené s posunmi v imunobiologickom systéme pacienta pri užívaní vysoko aktívnych liečiv. Napríklad použitie širokospektrálnych antibiotík sa môže prejaviť zmenou normálnej bakteriálnej flóry tela (črevá), realizovanej rozvojom superinfekcie, dysbiózy, kandidózy. Najčastejšie sa na týchto procesoch podieľajú pľúca a črevá.
Liečba kortikosteroidmi a imunosupresívna liečba oslabuje imunitný systém, čo má za následok zvýšené riziko vzniku infekčných ochorení, predovšetkým oportúnneho charakteru (pneumocystóza, cytomegalovírus a pod.).
Táto podskupina reakcií má 2 typy:
1) ALERGICKÉ REAKCIE;
2) Idiosynkrázia. Treba povedať, že negatívne vplyvy
súvisiaci s
chemické reakcie sú v lekárskej praxi veľmi bežné. Ich frekvencia sa neustále zvyšuje. Vznikajú bez ohľadu na dávku podaného liečiva a na ich vzniku sa podieľajú imunitné mechanizmy. Alergické reakcie môžu byť 2 typov: PRECITLIVOSŤ OKAMŽITÉHO TYPU, GNT – spojená s tvorbou protilátok triedy IgE a IgG4) a typu SLOW (hromadenie senzibilizovaných T-lymfocytov a makrofágov).
Klinický obraz je veľmi rôznorodý: žihľavka, kožné vyrážky, angioedém, sérová choroba, bronchiálna astma, horúčka, hepatitída atď. Ale hlavná vec je možnosť rozvoja anafylaktického šoku. Ak si rozvoj alergických reakcií vyžaduje aspoň dva kontakty pacienta s liečivou látkou, potom je vznik IDIOSYNKRÁZIE - intolerancie liečivých látok pri prvom kontakte s xenobiotikom vždy spojený s nejakým druhom GENETICKÉHO VADU, ktorý sa zvyčajne prejavuje tzv. absencia alebo extrémne nízka aktivita enzýmu. Napríklad užívanie antimalarika primachinu u osôb s genetickou enzymopatiou (nedostatok akt. G-6-FDG) spôsobuje tvorbu chinónu, ktorý pôsobí hemolyticky. V prítomnosti tejto fermentopatie je nebezpečné predpisovať lieky, ktoré sú oxidačnými činidlami, pretože to môže viesť k hemolýze
erytrocyty, lieková hemolytická anémia (aspirín, chloramfenikol, chinidín, primachín, furadonín).
PÁR SLOV O TVORBE NOVÝCH DROG, HODNOTENÍ DROG A ICH NÁZVOV. Pokrok farmakológie je charakterizovaný neustálym hľadaním a tvorbou nových liekov. Tvorba liekov začína výskumom chemikov a farmakológov, ktorých tvorivá spolupráca je pri objavovaní nových liekov absolútne nevyhnutná. Hľadanie nových fondov sa zároveň vyvíja viacerými smermi.
Hlavným spôsobom je CHEMICKÁ syntéza liečiv, ktorá môže byť realizovaná formou RIADENEJ syntézy alebo má EMPIRICKÚ cestu. Ak je riadená syntéza spojená s reprodukciou biogénnych látok (inzulín, adrenalín, noradrenalín), tvorbou antimetabolitov (PABA-sulfónamidy), modifikáciou molekúl zlúčenín so známou biologickou aktivitou (zmena v štruktúre acetylcholínu - gongliobacter hygronia) atď., potom empirická cesta pozostáva buď z náhodných nálezov, alebo hľadania pomocou skríningu, teda preosievania rôznych chemických zlúčenín na farmakologickú aktivitu.
Jedným z príkladov empirických zistení môže byť prípad obštrukcie hypoglykemického účinku pri použití sulfónamidov, čo následne viedlo k vytvoreniu syntetických sulfónamidových perforovaných antidiabetík (butamid, chlórpropamid).
Veľmi prácny je aj ďalší variant empirického spôsobu tvorby drog, SCREENINGOVÁ METÓDA. Je to však nevyhnutné, najmä ak sa skúma nová trieda chemických zlúčenín, ktorých vlastnosti na základe ich štruktúry je ťažké predpovedať (neefektívny spôsob). A tu v súčasnosti zohráva obrovskú úlohu informatizácia vedeckého výskumu.
V súčasnosti sa liečivá získavajú najmä cielenou chemickou syntézou, ktorá sa môže uskutočniť a) podobnosťou (zavedenie ďalších reťazcov, radikálov) b) komplementaritou, teda zhodou s akýmikoľvek receptormi tkanív a orgánov.
V arzenáli drog sa okrem syntetických drog napr. významné miesto sú obsadené prípravkami a jednotlivými látkami z liečivých surovín rastlinného alebo živočíšneho pôvodu, ako aj z rôznych minerálov. Ide predovšetkým o galenické, novogalenické lieky, alkaloidy, glykozidy. Takže morfín, kodeín, papaverín sa získavajú z ópia, rezerpín sa získava z hadovitého hada a srdcové glykozidy - digitoxín, digoxín - sa získavajú z náprstníka; z radu žliaz s vnútornou sekréciou hovädzieho dobytka – hormóny, imunoaktívne lieky (inzulín, tyreoidín, taktivín atď.).
Niektoré lieky sú odpadové produkty húb a mikroorganizmov. Príkladom sú antibiotiká. Ako základ pre ich syntézu, ako aj následné chemické premeny a výrobu polosyntetických a syntetických liečiv často slúžia liečivé látky rastlinného, živočíšneho, mikrobiálneho, hubového pôvodu.
Tempo vývoja liekov užívaním naberá na obrátkach
vývoj metód genetického inžinierstva (inzulín atď.).
Nové liečivo, ktoré prešlo všetkými týmito „sitami“ (štúdium farmakologickej aktivity, farmakodynamiky, farmakokinetiky, štúdium vedľajších účinkov, toxicity atď.), je povolené na klinické skúšky. Využíva metódu „slepej kontroly“, placebo efekt, metódu dvojitej „slepej kontroly“, kedy ani lekár, ani pacient nevie, kedy sa toto placebo používa. To vie len špeciálna komisia. Klinické skúšky sa vykonávajú na ľuďoch av mnohých krajinách na dobrovoľníkoch. Tu je, samozrejme, veľa právnych, deontologických, morálne aspekty problémy, ktoré si vyžadujú ich jasné vypracovanie, úpravu a schválenie zákonov v tomto smere.
NOMENKLATÚRA LIEKOV
Mnohé lieky s jednou účinnou látkou môžu byť pomenované podľa ich chemická štruktúra... Ale kvôli veľkej zložitosti ich zapamätania a nepohodlnosti ich používania sa chemické názvy v lekárskej praxi nepoužívajú.
V súčasnosti sa na označenie liekov používajú 2 typy názvov:
1) NEPATENTOVANÉ medzinárodné, ktoré sú schválené oficiálnymi zdravotníckymi orgánmi a používajú sa v národných a medzinárodných liekopisoch;
2) KOMERČNÉ alebo obchodné značky, ktoré sú obchodným majetkom farmaceutických spoločností. Navyše, jeden a ten istý liek môže mať mnoho mien. Sedatívum diazenam má obchodné názvy "seduxen", "sibazon", "relanium" atď. Niektoré lieky majú viac ako 100 názvov (napríklad vitamín B12). Zvyčajne má liek na obale obchodný názov aj medzinárodný nechránený názov.
Uprednostňuje sa generické predpisovanie liekov, čo znižuje možnosť vzniku lekárske chyby... Tieto lieky sú lacnejšie ako značkové lieky. Okrem toho predpisovanie liekov pod ich generickým názvom umožňuje lekárni poskytnúť pacientovi liek od akejkoľvek spoločnosti, ktorá tento liek vyrába.
Pre lekárov je najvýhodnejšia klasifikácia liekov, ktorá vychádza z NOSOLOGICKÉHO PRINCÍPU (napríklad lieky na liečbu bronchiálnej astmy, infarktu myokardu, antidiabetiká a pod.). Najlepšie klasifikácie však zohľadňujú také charakteristiky liekov, ako je lokalizácia účinku, farmakologický účinok a terapeutické použitie. Jednou z takýchto klasifikácií, ktorá je najdokonalejšia, je klasifikácia akademika M. D. Mashkovského, podľa ktorej je prezentovaná aj jeho známa referenčná kniha.
Blokátor H1-histamínových receptorov prvej generácie. Účinok na centrálny nervový systém je spôsobený blokádou H3-histamínových receptorov v mozgu a inhibíciou centrálnych cholinergných štruktúr. Uvoľňuje kŕče hladkého svalstva (priame pôsobenie), znižuje priepustnosť kapilár, predchádza a oslabuje alergické reakcie, pôsobí lokálne anesteticky, antiemeticky, sedatívne, stredne blokuje cholinergné receptory autonómnych ganglií, pôsobí hypnoticky.
Indikácie - anafylaktické a anafylaktoidné reakcie (v kombinovanej terapii); - Quinckeho edém;
Sérová choroba; - iné akútne alergické stavy (v kombinovanej liečbe av prípadoch, keď nie je možné použiť tabletovú formu).
Vedľajšie účinky
Zo strany nervový systém: ospalosť, slabosť, znížená rýchlosť psychomotorických reakcií, zhoršená koordinácia pohybov, závraty, triaška, podráždenosť, eufória, nepokoj (najmä u detí), nespavosť.
Zo strany dýchací systém: suchosť sliznice úst, nosa, priedušiek (zvýšená viskozita spúta).
Zo strany hematopoézy: hemolytická anémia, trombocytopénia, agranulocytóza.
Zo strany kardiovaskulárneho systému: zníženie krvného tlaku, tachykardia, extrasystol.
Z močového systému: porucha močenia.
Alergické reakcie: žihľavka, fotosenzitivita, kožná vyrážka, svrbenie.
Loratadin (klaritín)
farmakologický účinok
Antialergický liek, selektívny blokátor periférnych histamínových H 1 receptorov. Loratadín je tricyklická zlúčenina s výrazným antihistamínovým účinkom. Má rýchly a dlhotrvajúci antialergický účinok.
Loratadín nepreniká do BBB a neovplyvňuje centrálny nervový systém. Nemá klinicky významný anticholinergný alebo sedatívny účinok, t.j. pri použití v odporúčaných dávkach nespôsobuje ospalosť a neovplyvňuje rýchlosť psychomotorických reakcií. Užívanie Claritinu nepredĺži QT interval na EKG. Pri dlhodobej liečbe nenastali žiadne klinicky významné zmeny vitálnych funkcií, údajov z fyzikálneho vyšetrenia, laboratórnych výsledkov alebo EKG.
Loratadín nemá žiadnu významnú selektivitu pre histamínové H2 receptory. Neinhibuje spätné vychytávanie norepinefrínu a má malý alebo žiadny vplyv na kardiovaskulárny systém alebo funkciu kardiostimulátora
Vedľajšie účinky
Z nervového systému: u detí vo veku 2 až 12 rokov - bolesť hlavy (2,7 %), nervozita (2,3 %), únava (1 %); u dospelých - bolesť hlavy (0,6%), ospalosť (1,2%), nespavosť (0,1%).
u dospelých - zvýšená chuť do jedla (0,5%).
V období po uvedení lieku na trh
Z nervového systému: veľmi zriedka (< 1/10 000) - головокружение, утомляемость.
Z tráviaceho systému: veľmi zriedka (< 1/10 000) - сухость во рту, желудочно-кишечные расстройства (тошнота, гастрит), нарушение функции печени.
Alergické reakcie: veľmi zriedka (< 1/10 000) - сыпь, анафилаксия.
Na strane kardiovaskulárneho systému: veľmi zriedka (< 1/10 000) - сердцебиение, тахикардия.
Zo strany kože: veľmi zriedka (< 1/10 000) - алопеция.
Indikácie
sezónna (senná nádcha) a celoročná alergická nádcha a alergická konjunktivitída (na odstránenie príznakov spojených s týmito ochoreniami - kýchanie, svrbenie nosovej sliznice, rinorea, pocit pálenia a svrbenia v očiach, slzenie); - chronická idiopatická žihľavka; - kožné ochorenia alergického pôvodu...
33. Prostriedky, ktoré eliminujú všeobecné prejavy alergických reakcií, ako je anafylaktický šok. Epinefrín, Eufillin, prednizolón. Hlavné farmakologické účinky, účel predpisovania každého lieku a nežiaduce účinky.
PROTIALERGICKÉ LIEKY(antialergiká; syn. desenzibilizátory) - lieky, ktoré zabraňujú alebo oslabujú prejavy alergických reakcií. Jedným z možných spôsobov prevencie a liečby alergických reakcií je metóda tzv. špecifická hyposenzibilizácia, teda zníženie citlivosti organizmu na akýkoľvek antigén opakovaným podávaním samotného antigénu v nízkych dávkach, ktoré nespôsobujú prejavy alergie. V tomto prípade telo postupne stráca citlivosť na injekčne podaný antigén.
Adrenalín
Farmakologický účinok Adrenomimetikum, má priamy stimulačný účinok na α- a β-adrenergné receptory. Pôsobením epinefrínu (adrenalínu) v dôsledku stimulácie α-adrenergných receptorov dochádza k zvýšeniu obsahu intracelulárneho vápnika v hladkých svaloch. zvyšuje aktivitu fosfolipázy C (prostredníctvom stimulácie G-proteínu) a tvorbu inozitoltrifosfátu a diacylglycerolu. Má výrazný vplyv na kardiovaskulárny systém. Zvyšuje srdcovú frekvenciu a silu, mŕtvicu a srdcový výdaj. Zlepšuje AV vodivosť, zvyšuje automatizáciu. Zvyšuje potrebu kyslíka v myokarde. Spôsobuje vazokonstrikciu brušných orgánov, kože, slizníc, v menšej miere - kostrových svalov. Zvyšuje krvný tlak (hlavne systolický), epinefrín (adrenalín) uvoľňuje hladké svalstvo priedušiek, znižuje tonus a motilitu tráviaceho traktu, rozširuje zrenice a pomáha znižovať vnútroočný tlak. Spôsobuje hyperglykémiu a zvyšuje hladinu voľných mastných kyselín v plazme. Indikácie Alergické reakcie okamžitého typu (vrátane žihľavky, angioedému, anafylaktického šoku), ktoré sa vyvíjajú s použitím liekov, sér, krvných transfúzií, jedla, bodnutia hmyzom alebo iných alergénov. Bronchiálna astma (zmiernenie záchvatu), bronchospazmus počas anestézie. S cieľom zastaviť krvácanie. Vedľajší účinok Zo strany kardiovaskulárneho systému: angina pectoris, bradykardia alebo tachykardia, palpitácie, zvýšenie alebo zníženie krvného tlaku; pri použití vo vysokých dávkach - ventrikulárne arytmie; zriedkavo - arytmia, bolesť na hrudníku. Z nervového systému: bolesť hlavy, úzkosť, tras, závraty, nervozita, únava, psychoneurotické poruchy
Euphyllin
farmakologický účinok
Bronchodilatátor, derivát xantínu; inhibuje fosfodiesterázu, zvyšuje akumuláciu cyklického adenozínmonofosfátu v tkanivách, blokuje adenozínové (purínové) receptory; znižuje tok iónov vápnika cez kanály bunkových membrán, znižuje kontraktilnú aktivitu hladkých svalov. Uvoľňuje svaly priedušiek, zvyšuje mukociliárny klírens, stimuluje kontrakciu bránice, zlepšuje funkciu dýchacích a medzirebrových svalov, stimuluje dýchacie centrum, zvyšuje jeho citlivosť na oxid uhličitý a zlepšuje alveolárnu ventiláciu, čo v konečnom dôsledku vedie k zníženiu v závažnosti a frekvencii epizód apnoe. Normalizáciou funkcie dýchania prispieva k nasýteniu krvi kyslíkom a zníženiu koncentrácie oxidu uhličitého. Pôsobí stimulačne na činnosť srdca, zvyšuje silu a počet srdcových kontrakcií, zvyšuje koronárne prekrvenie a potrebu kyslíka myokardom. Znižuje tonus krvných ciev (hlavne ciev mozgu, kože a obličiek). Má periférny venodilatačný účinok, znižuje odpor pľúcnych ciev, znižuje tlak v „malom“ okruhu krvného obehu. Zvyšuje prietok krvi obličkami, má mierny diuretický účinok. Rozširuje extrahepatálny žlčový trakt. Inhibuje agregáciu krvných doštičiek (inhibuje aktivačný faktor krvných doštičiek a PgE2 alfa), zvyšuje odolnosť erytrocytov voči deformácii (zlepšuje reologické vlastnosti krvi), znižuje tvorbu trombov a normalizuje mikrocirkuláciu. Má tokolytický účinok, zvyšuje kyslosť žalúdočnej šťavy. Pri použití vo veľkých dávkach má enileptogénny účinok.
Vedľajšie účinky
Z nervového systému: závrat, bolesť hlavy, nespavosť, nepokoj, úzkosť, podráždenosť, triaška.
Na strane kardiovaskulárneho systému: palpitácie, tachykardia (vrátane plodu, keď ho užíva tehotná žena v treťom trimestri), arytmie, kardialgia, zníženie krvného tlaku, zvýšenie frekvencie záchvatov angíny pectoris.
Z tráviaceho systému: gastralgia, nevoľnosť, vracanie, gastroezofageálny reflux, pálenie záhy, exacerbácia vredovej choroby žalúdka, hnačka, pri dlhodobom používaní - znížená chuť do jedla.
Alergické reakcie: kožná vyrážka, svrbenie, horúčka.
Ostatné: bolesť na hrudníku, tachypnoe, návaly horúčavy, albuminúria, hematúria, hypoglykémia, zvýšené vylučovanie moču, zvýšené potenie.
Indikácie
Broncho-obštrukčný syndróm akéhokoľvek pôvodu: bronchiálna astma (liek voľby u pacientov s fyzickou námahou a ako doplnkový liek pri iných formách), chronická obštrukčná choroba pľúc, pľúcny emfyzém, chronická obštrukčná bronchitída, pľúcna hypertenzia, pľúcne srdce, spánok apnoe.
Prednison
farmakologický účinok
Syntetický GCS. Má výrazný protizápalový účinok. Liek inhibuje rozvoj symptómov zápalu. Inhibuje hromadenie makrofágov, leukocytov a iných buniek v oblasti zápalu. Inhibuje fagocytózu, uvoľňovanie mikrozomálnych enzýmov, ako aj syntézu a uvoľňovanie zápalových mediátorov. Spôsobuje zníženie kapilárnej permeability, inhibíciu migrácie leukocytov.
Zvyšuje syntézu lipomodulínu, inhibítora fosfolipázy A2, ktorý uvoľňuje kyselinu arachidónovú z fosfolipidových membrán a zároveň inhibuje jej syntézu.
Mechanizmus imunosupresívneho účinku prednizolónu nie je úplne objasnený. Liek znižuje počet T-lymfocytov, monocytov a acidofilných granulocytov, ako aj väzbu imunoglobulínov na receptory na povrchu bunky, inhibuje syntézu alebo uvoľňovanie interleukínov znížením blastogenézy T-lymfocytov; znižuje skorú imunologickú odpoveď. Inhibuje tiež penetráciu imunologických komplexov cez membrány a znižuje koncentráciu zložiek komplementu a imunoglobulínov.
Prednizolón pôsobí na distálne obličkové tubuly, zvyšuje reabsorpciu sodíka a vody, ako aj zvyšuje vylučovanie iónov draslíka a vodíka.
Prednizolón inhibuje sekréciu ACTH hypofýzou, čo vedie k zníženiu produkcie kortikosteroidov a androgénov kôrou nadobličiek. Po dlhšom užívaní lieku vo vysokých dávkach je možné do roka obnoviť funkciu nadobličiek a v niektorých prípadoch dochádza k pretrvávajúcemu útlmu ich funkcie. Prednizolón zvyšuje katabolizmus bielkovín a indukuje enzýmy zapojené do metabolizmu aminokyselín. Inhibuje syntézu a zvyšuje katabolizmus bielkovín v lymfatickom, spojivovom a svalovom tkanive. Pri dlhodobom používaní je možný rozvoj atrofie týchto tkanív (ako aj kože).
Zvyšuje koncentráciu glukózy v krvi indukciou enzýmov glukoneogenézy v pečeni, stimuluje katabolizmus proteínov (čím sa zvyšuje množstvo aminokyselín pre glukoneogenézu) a znižuje spotrebu glukózy v periférnych tkanivách. To vedie k akumulácii glykogénu v pečeni, zvýšeniu koncentrácie glukózy v krvi a zvýšeniu inzulínovej rezistencie.
Indikácie
Endokrinologické ochorenia:
Nedostatočnosť kôry nadobličiek: primárna (Addisonova choroba) a sekundárna; - adrenogenitálny syndróm (vrodená adrenálna hyperplázia); - akútna nedostatočnosť kôry nadobličiek;
Pred chirurgickými zákrokmi a v prípade závažných ochorení a zranení u pacientov s nedostatočnosťou nadobličiek; - subakútna tyroiditída.
Závažné alergické ochorenia rezistentné na inú liečbu: - kontaktná dermatitída; - atopická dermatitída; - sérová choroba; - reakcie z precitlivenosti na lieky;
Pretrvávajúca alebo sezónna alergická rinitída; - anafylaktické reakcie; - angioedém.
Reumatické ochorenia:
Reumatoidná artritída, juvenilná reumatoidná artritída (v prípadoch rezistentných na inú liečbu);
Dermatologické ochorenia: - exfoliatívna dermatitída - herpetiformná bulózna dermatitída;
Závažná seboroická dermatitída - Závažný multiformný erytém (Stevensov-Johnsonov syndróm);
Vedľajšie účinky
Pri krátkodobom užívaní prednizónu (ako iných kortikosteroidov) sú vedľajšie účinky zriedkavé. Pri dlhodobom používaní prednizolónu sa môžu vyvinúť nasledujúce vedľajšie účinky.
Na strane rovnováhy voda-elektrolyt: zadržiavanie sodíka a tekutín v tele, hypokaliémia.
Z pohybového aparátu: svalová slabosť, steroidná myopatia, strata svalovej hmoty, osteoporóza, kompresívna zlomenina chrbtice.
Z tráviaceho systému: steroidný vred s možnou perforáciou a krvácaním, pankreatitída, plynatosť, ulcerózna ezofagitída, poruchy trávenia, nevoľnosť, zvýšená chuť do jedla.
Dermatologické reakcie: atrofia kože, strie, akné, oneskorené hojenie rán, stenčenie kože, petechie, hematómy, erytém, zvýšené potenie, alergická dermatitída, žihľavka, angioedém.
Zo strany centrálneho nervového systému a periférneho nervového systému: zvýšený intrakraniálny tlak so syndrómom kongestívnej bradavky zrakového nervu (vyskytuje sa najčastejšie u detí, po príliš rýchlom znížení dávky, príznaky - bolesť hlavy, zhoršenie zrakovej ostrosti, dvojité videnie); kŕče, závraty, bolesti hlavy, poruchy spánku.
Z endokrinného stavu: sekundárna adrenálna a hypotalamo-hypofyzárna nedostatočnosť (najmä počas stresových situácií: choroba, úraz, operácia); Cushingov syndróm.
Ostatné: anafylaktické reakcie, reakcie z precitlivenosti; obliterujúca arteritída, prírastok hmotnosti, mdloby.
1. Podstata farmakológie ako vedy. Sekcie a odbory modernej farmakológie. Hlavné pojmy a pojmy farmakológie sú farmakologická aktivita, pôsobenie, účinnosť chemikálií.
Farmakológia- veda o liekoch vo všetkých aspektoch - teoretický základ terapie:
a) veda o interakcii chemikálií so živými systémami
b) náuka o riadení životne dôležitých procesov tela pomocou chemikálií
Rozvoj farmakológie ide dvoma hlavnými smermi: základným výskumom na objasnenie princípov a mechanizmov pôsobenia liekov a ich vývoja účinné lieky ako základ pre liečbu chorôb.
Farmakológia sa delí na:
1. Všeobecné- študuje všeobecné zákonitosti vzájomného pôsobenia liečivých látok so živými organizmami.
Súkromné- považuje za špecifické farmakologické skupiny a jednotlivé lieky
2. Experimentálna (základná) farmakológia- experimentálne skúma účinok drog.
Klinická farmakológia- štúdie klinickej účinnosti a bezpečnosti
užívanie liekov u pacientov, optimalizuje liečebný program pacienta, pričom zohľadňuje
jeho stav.
Toxikológia- študuje toxický účinok rôznych látok na orgány (vrátane
a liečivé).
Časti modernej farmakológie:
1) farmakodynamiky- študuje a) vplyv liekov na ľudský organizmus, b) vzájomné pôsobenie rôznych liekov v organizme pri ich predpisovaní, c) vplyv veku a rôznych chorôb na účinok liekov
2) farmakokinetika- študuje absorpciu, distribúciu, metabolizmus a vylučovanie liekov (t. j. ako telo pacienta reaguje na lieky)
3) farmakogenetika- študuje úlohu genetických faktorov pri vytváraní farmakologickej odpovede organizmu na lieky
4) farmakoekonomika- zhodnotí výsledky užívania a náklady na lieky pre rozhodnutie o ich následnom praktickom použití
5) farmakoepidemiológia- študuje užívanie drog a ich účinky na úrovni populácie alebo veľkých skupín ľudí s cieľom zabezpečiť užívanie najúčinnejších a najbezpečnejších liekov
Základné pojmy a pojmy:
Farmakologická (biologická) aktivita- vlastnosť látky spôsobovať zmeny v biosystéme (ľudskom tele). Farmakologické látky = biologicky aktívne látky (BAS)
farmakologický účinok- vplyv drog na objekt a jeho ciele
Farmakologický účinok- výsledok pôsobenia látky v organizme (úprava fyziologických, biochemických procesov, morfologických štruktúr) - kvantitatívna, nie však kvalitatívna zmena stavu biosystémov (buniek, tkanív, orgánov).
Účinnosť liekov- schopnosť liekov vyvolať v organizme určité farmakologické účinky nevyhnutné v tomto prípade. Posúdené na základe „podstatných dôkazov“ – adekvátne dobre kontrolované štúdie a klinické štúdie vykonávané odborníkmi s primeraným vedeckým vzdelaním a skúsenosťami vo výskume liekov tohto typu (FDA)
2. Zdroje a štádiá tvorby drog. Lieky – generiká, placebo – účinky Vymedzenie pojmov liek, liek, liek a lieková forma.
Zdroje tvorby drog:
a) prírodné suroviny: rastliny, živočíchy, minerály, odpadové produkty mikroorganizmov (srdcové glykozidy, bravčový inzulín, AB)
b) modifikované prírodné biologicky aktívne látky
c) produkty chemickej syntézy (metódy: farmakologický skríning, molekulárny dizajn, reprodukcia biogénnych amínov, cielená modifikácia molekúl s už známou aktivitou, syntéza farmakologicky aktívnych metabolitov, náhodné nálezy ("serendipitická" metóda))
d) produkty genetického inžinierstva (rekombinantný inzulín, interferóny)
Etapy výroby lieku:
1. Syntéza liečiv v chemickom laboratóriu
2. Predklinické hodnotenie aktivity a nežiaducich účinkov liečiv MZ a iných organizmov
3. Klinické skúšky liekov Farmakologický výbor skúma dokumentáciu po ukončení každej fázy. Liek možno vysadiť v ktorejkoľvek fáze. (I. fáza - hodnotenie tolerancie na zdravých dobrovoľníkoch vo veku 20-25 rokov, II. fáza - na chorých dobrovoľníkoch s menej ako 100 ľuďmi trpiacimi špecifickým ochorením, III. fáza - multicentrické klinické skúšky na veľkých skupinách ľudí (do 1000 osôb) , Fáza IV - monitorovanie liekov počas 5 rokov po jeho oficiálnom povolení (vykonané dňa Vysoké číslo pacientov (najmenej 1 000 – 5 000 ľudí). Po ukončení III. fázy klinických skúšok dokumentácia opäť prejde Farmakologickému výboru (objem celej dokumentácie môže byť až 1 milión strán) a do 1-2 rokov je zaregistrovaná v Štátny register lieky a produkty lekárske účely... Až potom má farmaceutický koncern právo začať priemyselnú výrobu lieku a jeho distribúciu prostredníctvom siete lekární.
Generický liek je generický liek, ktorý je úpravou pôvodného lieku, na ktorý vypršal patent. Môže sa líšiť od pôvodného lieku v zložení pomocných látok. Nevyhnutná požiadavka na predaj generík – dôkazmi podložená farmaceutická, biologická a terapeutická rovnocennosť s materským liekom. Generické lieky sú vždy lacnejšie ako ich značkové náprotivky, pretože spoločnosť nemíňa peniaze na 10-15 ročný výskum liekov, ale používa hotové dáta
Placebo- akákoľvek zložka terapie, ktorá nemá žiadny špecifický biologický účinok na ochorenie, ktoré je predmetom liečby.
Používa sa na účely kontroly pri hodnotení účinku liekov a v prospech pacienta bez akýchkoľvek farmakologických látok v dôsledku iba psychického vplyvu (t.j. placebo efekt).
Všetky typy liečby majú psychologickú zložku alebo uspokojujúcu ( placebo efekt) alebo znepokojujúce ( nocebo efekt). Príklad placebo efektu: rýchle zlepšenie stavu pacienta s vírusovou infekciou pri užívaní antibiotík. Prínos placebo efektu súvisí s psychologickým dopadom na pacienta. Maximálny bude len pri jeho používaní. v kombinácii s liečebnými metódami ktoré majú výrazný špecifický účinok. Drahé látky ako placebo tiež pomáhajú dosiahnuť väčšiu odozvu.
Indikácie pre použitie placeba:
1) slabé duševné poruchy
2) psychologická podpora pre pacienta s nevyliečiteľnou chronickou chorobou alebo s podozrením na zložitú diagnózu
Medicína- akákoľvek látka alebo produkt používaný na úpravu alebo vyšetrenie fyziologických systémov alebo patologických stavov v prospech príjemcu (podľa WHO, 1966); jednotlivé látky, zmesi látok alebo kompozície neznámeho zloženia s preukázanými liečivými vlastnosťami.
Liečivá látka- jednotlivá chemická zlúčenina používaná ako liečivo.
Lieková forma- vhodná forma na praktické použitie, podávaná liečivu na dosiahnutie požadovaného terapeutického alebo profylaktického účinku.
Liečivo- liek v určitej liekovej forme schválený orgánom štátnej správy.
Napríklad: liekom je antibiotikum ampicilín, liekom je trihydrát ampicilínu, ktorý môže byť vo forme tabliet alebo kapsúl. Liečivo sú tablety ampicilín trihydrát po 0,25 g.
Cesty podávania liečiva do organizmu a ich charakteristika. Presystémová eliminácia liekov.
a. enterálny spôsob podania: perorálne, sublingválne, bukálne, rektálne, sondou b. parenterálny spôsob podania: intravenózne, subkutánne, intramuskulárne, ... 2. Na lokálnu expozíciu: kožné (epikutárne), na sliznice, do dutiny (brušnej, pleurálnej, kĺbovej), do tkaniva ...Transport liečiv cez biologické bariéry a jeho odrody. Hlavné faktory ovplyvňujúce transport liečiv v tele.
1) Filtrácia (difúzia vody) - pasívny pohyb molekúl látok po koncentračnom gradiente cez póry vyplnené vodou v membráne každého ... 2) Pasívna difúzia (difúzia lipidov) - hlavný mechanizmus prenosu liečiva, ... 3 ) Transport pomocou špecifických nosičov - prenos liečiva pomocou nosičov zabudovaných v membráne (častejšie ...Transport liečivých látok s premenlivou ionizáciou cez membrány (Henderson-Hasselbalchova ionizačná rovnica). Princípy riadenia prenosu.
Všetky lieky sú slabé kyseliny alebo slabé zásady, ktoré majú svoje vlastné hodnoty ionizačnej konštanty (pK). Ak sa hodnota pH média rovná hodnote pK liečiva, potom 50 % jeho molekúl bude v ionizovanom stave a 50 % v neionizovanom stave a médium pre liečivo bude neutrálne.
V kyslom prostredí (pH menšie ako pK), kde je nadbytok protónov, bude slabá kyselina v nedisociovanej forme (R-COOH), t.j. bude spojená s protónom - protónovaná. Táto forma kyseliny je bez náboja a je ľahko rozpustná v lipidoch. Ak sa pH posunie na alkalickú stranu (tj pH sa stane vyšším ako pK), potom kyselina začne disociovať a strácať protón, prechádzajúc do neprotónovanej formy, ktorá má náboj a je slabo rozpustná v lipidoch. .
V alkalickom prostredí, kde je nedostatok protónov, bude slabá zásada v nedisociovanej forme (R-NH 2), t.j. bude neprotonovaný a bez náboja. Táto forma bázy je vysoko rozpustná v tukoch a rýchlo sa vstrebáva. V kyslom prostredí je nadbytok protónov a slabá zásada sa začne disociovať, pričom viaže protóny a vytvára protónovanú nabitú formu zásady. Táto forma je slabo rozpustná v lipidoch a slabo absorbovaná.
teda absorpcia slabých kyselín prebieha najmä v kyslom prostredí a slabých zásad v alkalickom prostredí.
Vlastnosti metabolizmu slabých kyselín (SC):
1) žalúdok: SA v kyslom obsahu žalúdka nie je ionizovaný a v alkalickom prostredí tenkého čreva sa disociuje a molekuly SA získajú náboj. Preto bude absorpcia slabých kyselín najintenzívnejšia v žalúdku.
2) v krvi je médium dostatočne zásadité a absorbované molekuly SC sa premenia na ionizovanú formu. Filter renálneho glomerulu umožňuje prechod ionizovaných aj neionizovaných molekúl, preto sa napriek náboju molekuly SC vylúči do primárneho moču
3) ak je moč alkalický, potom kyselina zostane v ionizovanej forme, nebude sa môcť reabsorbovať späť do krvného obehu a bude sa vylučovať močom; Ak je moč kyslý, potom liek prejde do neionizovanej formy, ktorá sa ľahko reabsorbuje späť do krvi.
Vlastnosti metabolizmu slabých zásad: oproti SC (v čreve sa lepšie vstrebáva, v alkalickom moči sa reabsorbuje)
to., pre urýchlenie vylučovania slabej kyseliny z tela je potrebné alkalizovať moč a pre urýchlenie vylučovania slabej zásady okysleť (detoxikácia podľa Popova).
Kvantitatívna závislosť procesu ionizácie liečiva pri rôznych hodnotách pH média umožňuje získať rovnicu Henderson-Hasselbach:
Kde pKa zodpovedá hodnote pH, pri ktorej sú koncentrácie ionizovaných a neionizovaných foriem v rovnováhe .
Henderson-Hasselbachova rovnica umožňuje odhadnúť stupeň ionizácie liečiva pri danej hodnote pH a predpovedať pravdepodobnosť jeho prieniku cez bunkovú membránu.
(1)Pre zriedenú kyselinu A,
HA ↔ H + + A -, kde HA je koncentrácia neionizovanej (protónovanej) formy kyseliny a A - je koncentrácia ionizovanej (neprotónovanej) formy.
(2) Pre slabá základňa, B,
BH + ↔ H + + B, kde BH + je koncentrácia protónovanej formy bázy, B je koncentrácia neprotónovanej formy
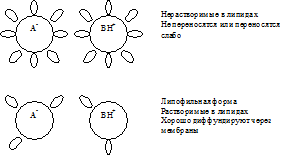
Pri znalosti pH média a pKa látky je možné z vypočítaného logaritmu určiť stupeň ionizácie liečiva, a teda stupeň jeho absorpcie z gastrointestinálneho traktu, reabsorpcie alebo vylučovania obličkami pri rôznych hodnoty pH moču atď.
Princípy riadenia dopravy.
Na urýchlenie absorpcie
Ø slabé kyseliny (ASA) – pH žalúdočnej šťavy musí byť kyslé;
Ø slabý základ – pH žalúdočnej šťavy by malo byť neutrálne.
Pre urýchlenie výberu
Ø slabé kyseliny – moč je alkalický;
Ø slabé zásady – okysľujú moč.
Prenos liečiv v tele. Difúzia vody a difúzia v lipidoch (Fickov zákon). Aktívna doprava.
Prenos liečiv v tele sa môže uskutočniť difúziou vody a lipidov, aktívnym transportom, endocytózou a pinocytózou.
Vlastnosti prenosu liečiv v tele difúziou vody:
1. Epitelové vrstvy (sliznice tráviaceho traktu, ústna dutina a pod.) - difúzia vody len veľmi malých molekúl (metanol, ióny lítia a pod.)
2. Kapiláry (okrem mozgových) - filtrácia látok s molekulovou hmotnosťou do 20-30 tis.. Áno.
3. Kapiláry mozgu - v zásade nemajú vodné póry, s výnimkou oblastí hypofýzy, epifýzy, komory IV zóny, plexus choroideus, eminencia mediánu
4. Placenta – nemá žiadne vodné póry (hoci táto otázka je kontroverzná).
5. Väzba liečiv na krvné bielkoviny bráni ich výstupu z krvného obehu, a tým aj difúzii vody
6. Difúzia vo vode závisí od veľkosti molekúl liečiva a vodných pórov
Vlastnosti lipidovej difúzie:
1. Hlavný mechanizmus prenosu liečiva cez bunkové membrány
2. Určená lipofilitou difúznej látky (t. j. distribučným koeficientom olej/voda) a koncentračným gradientom, môže byť obmedzená veľmi nízkou rozpustnosťou látky vo vode (ktorá zabraňuje prenikaniu liečiva do vodnej fázy). membrán)
3. Nepolárne zlúčeniny ľahko difundujú, ióny ťažko difundujú.
Akákoľvek difúzia (voda aj lipidy) sa riadi Fickovým zákonom difúzie:
Rýchlosť difúzie - počet molekúl liečiva prenášaných za jednotku času; С 1 - koncentrácia látky mimo membrány; С 2 - koncentrácia látky zvnútra membrány.
Dôsledok Fickovho zákona:
1) filtrácia liečiva je tým vyššia, čím väčšia je jeho koncentrácia v mieste vpichu (S absorbovaného povrchu v čreve je väčšie ako v žalúdku, preto je absorpcia liečiva do čreva rýchlejšia)
2) čím vyššia je koncentrácia liečiva v mieste vpichu, tým vyššia je filtrácia liečiva
3) filtrácia liečiv je tým vyššia, čím menšia je hrúbka biologickej membrány, ktorá sa má prekonať (hrúbka bariéry v pľúcnych alveolách je oveľa menšia ako hrúbka kože, preto je rýchlosť absorpcie vyššia v pľúca)
Aktívna doprava- prenos liečiv bez ohľadu na koncentračný gradient s využitím energie ATP je charakteristický pre hydrofilné polárne molekuly, množstvo anorganických iónov, cukrov, aminokyselín, pyrimidínov.
Charakterizované: a) selektivita pre určité zlúčeniny b) možnosť konkurencie dvoch látok pre jeden transportný mechanizmus c) saturácia pri vysokých koncentráciách látky d) možnosť transportu proti koncentračnému gradientu e) spotreba energie.
7. Centrálnym postulátom farmakokinetiky je koncentrácia liečiva v krvi – hlavný parameter na kontrolu terapeutického účinku. Problémy riešené na základe poznania tohto postulátu.
Centrálny postulát (dogma) farmakokinetiky: koncentrácia liečiva v krvnej plazme určuje (kvantifikuje) farmakologický účinok.
Vo väčšine prípadov je rýchlosť absorpcie, distribúcie, metabolizmu a vylučovania liečiv úmerná ich koncentrácii v krvnej plazme (podriaďuje sa zákonu hromadného pôsobenia), takže je možné:
1) určiť polčas rozpadu (pre lieky s kinetikou prvého rádu)
2) vysvetliť trvanie niektorých toxických účinkov liekov (pre lieky vo vysokých dávkach s kinetikou nasýtenia)
[C] plazma → [C] na cieľ → účinok
Určený zákonmi je určený z-us farmakodynamiky
Distribúcia
Ciele: naučiť sa kontrolovať koncentráciu lieku v krvi.
Farmakokinetické modely (jednokomorové a dvojkomorové), kvantitatívne zákony absorpcie a eliminácie liečiva.
Celý organizmus je jedna homogénna nádoba. Predpoklady: 1) dochádza k rýchlemu dynamickému vývoju medzi obsahom liečiva v ... 2) liečivo je rýchlo a rovnomerne distribuované v objeme krviDistribúcia liekov v tele. Oddiely, ligandy. Hlavné determinanty distribúcie.
Distribučné kompartmenty: 1. Extracelulárny priestor (plazma, medzibunková tekutina) 2. Bunky (cytoplazma, membrána organel)Eliminačná konštanta, jej podstata, rozmer, vzťah s ostatnými farmakokinetickými parametrami.
Konštanta rýchlosti eliminácie(k el, min -1) - ukazuje, aká časť liečiv sa z tela vylúči za jednotku času Þ Kel = A out / A total, kde A out je množstvo uvoľnených liečiv v jednotkách. čas, A celkový - celkové množstvo liekov v tele.
Hodnota k el sa zvyčajne zistí vyriešením farmakokinetickej rovnice popisujúcej proces eliminácie liečiva z krvi, preto sa k el nazýva modelový kinetický index. K el priamo nesúvisí s plánovaním dávkovacieho režimu, ale jeho hodnota sa používa na výpočet iných farmakokinetických parametrov.
Eliminačná konštanta je priamo úmerná klírensu a nepriamo úmerná distribučnému objemu (z definície klírensu): Kel = CL / Vd; = hodina -1 / min -1 = zlomok za hodinu.
Polčas rozpadu liečiv, jeho podstata, rozmer, vzťah s ostatnými farmakokinetickými parametrami.
Polovičné eliminačné obdobie(t ½, min) je čas potrebný na zníženie koncentrácie liečiva v krvi presne o polovicu. V tomto prípade nezáleží na tom, akým spôsobom sa dosiahne zníženie koncentrácie - pomocou biotransformácie, vylučovania alebo vďaka kombinácii oboch procesov.
Polčas je určený vzorcom:
![]()
Polčas je najdôležitejším farmakokinetickým parametrom, ktorý umožňuje:
b) určiť čas úplného vylúčenia liečiva
c) predpovedať koncentráciu liečiv kedykoľvek (pre liečivá s kinetikou prvého rádu)
Klírens ako hlavný farmakokinetický parameter na riadenie dávkovacieho režimu. Jeho podstata, rozmer a vzťah s ostatnými farmakokinetickými parametrami.
Odbavenie(Cl, ml / min) - objem krvi, ktorý sa vyčistí z liekov za jednotku času.
Pretože plazma (krv) je „viditeľná“ časť distribučného objemu, potom je klírens podielom distribučného objemu, z ktorého sa liek uvoľní za jednotku času. Ak označíme celkové množstvo liečiva v organizme cez A celkovo a suma, ktorá bola pridelená po A von, potom:
Na druhej strane z definície distribučného objemu vyplýva, že celkové množstvo liečiva v organizme je A celkom = Vd´Cter/plazma... Nahradením tejto hodnoty do vzorca vôle dostaneme:
![]() .
.
Klírens je teda pomer rýchlosti eliminácie liečiva k jeho koncentrácii v krvnej plazme.
V tejto forme sa klírensový vzorec používa na výpočet udržiavacej dávky lieku ( D p), teda dávka lieku, ktorá by mala kompenzovať stratu lieku a udržiavať jeho hladinu na konštantnej úrovni:
Rýchlosť podávania = rýchlosť eliminácie = Cl'C ter (dávka / min)
D p = rýchlosť infúzie 't (t je interval medzi užitím lieku)
Svetlá výška je aditívna, t.j. vylučovanie látky z tela môže nastať za účasti procesov v obličkách, pľúcach, pečeni a iných orgánoch: Cl systémový = Cl obličkový. + Cl pečeň + Cl ostatné.
Povolenie viazané s polčasom rozpadu lieku a distribučným objemom: t1/2 = 0,7* Vd/Cl.
Dávka. Druhy dávok. Jednotky dávkovania lieku. Ciele dávkovania liečiva, spôsoby a možnosti podávania, interval podávania.
Účinok liekov na telo je do značnej miery určený ich dávkou.
Dávka- množstvo látky zavedenej do tela naraz; vyjadrené v hmotnosti, objeme alebo konvenčných (biologických) jednotkách.
Typy dávok:
a) jednorazová dávka - množstvo látky na dávku
b) denná dávka - množstvo liečiva predpísané za deň v jednej alebo viacerých dávkach
c) kurzová dávka - celkové množstvo liečiva na priebeh liečby
d) terapeutické dávky - dávky, v ktorých sa liek používa na terapeutické alebo profylaktické účely (prahové, resp. minimálne účinné, priemerné terapeutické a vyššie terapeutické dávky).
e) toxické a smrteľné dávky - dávky liekov, pri ktorých začínajú mať výrazné toxické účinky alebo spôsobujú smrť organizmu.
f) nasycovacia (úvodná) dávka - počet vstreknutých liečiv, ktorý vyplní celý distribučný objem organizmu v efektívnej (terapeutickej) koncentrácii: VD = (Css * Vd) / F
g) udržiavacia dávka - systematicky podávané množstvo liečiva, ktoré kompenzuje stratu liečiva s klírensom: PD = (Css * Cl * DT) / F
Farmaceutické dávkové jednotky:
1) v gramoch alebo zlomkoch gramu liečiva
2) počet liekov na 1 kg telesná hmotnosť (napríklad 1 mg/kg) alebo na jednotku plochy tela (napríklad 1 mg/m2)
Ciele dávkovania liekov:
1) určiť množstvo liekov potrebné na dosiahnutie požadovaného terapeutického účinku s určitým trvaním
2) vyhnúť sa javom intoxikácie a vedľajším účinkom pri zavádzaní liekov
Spôsoby podávania liekov: 1) enterálne 2) parenterálne (pozri časť 5)
Možnosti podávania liekov:
a) kontinuálne (dlhodobou intravaskulárnou infúziou liečiv kvapkaním alebo prostredníctvom automatických dávkovačov). Pri kontinuálnom podávaní liekov sa jeho koncentrácia v organizme plynule mení a nepodlieha výraznejším výkyvom.
b) prerušované podávanie (injekčnými alebo neinjekčnými metódami) - podávanie liečiva v pravidelných intervaloch (dávkovacie intervaly). Pri prerušovanom podávaní liekov jeho koncentrácia v organizme neustále kolíše. Po užití určitej dávky najskôr stúpa a potom postupne klesá, pričom pred ďalším podaním lieku dosahuje minimálne hodnoty. Kolísanie koncentrácie je tým výraznejšie, čím väčšia je podaná dávka liečiva a interval medzi injekciami.
Interval vstrekovania- interval medzi podávanými dávkami zabezpečujúci udržanie terapeutickej koncentrácie látky v krvi.
15. Podávanie liekov konštantnou rýchlosťou. Kinetika koncentrácie liečiva v krvi. Stacionárna koncentrácia liečiva v krvi (C ss), čas na jej dosiahnutie, jej výpočet a riadenie.
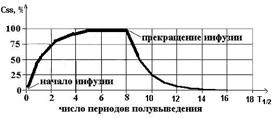 Zvláštnosťou zavádzania liekov konštantnou rýchlosťou je hladká zmena jeho koncentrácie v krvi po podaní, pričom:
Zvláštnosťou zavádzania liekov konštantnou rýchlosťou je hladká zmena jeho koncentrácie v krvi po podaní, pričom:
1) čas na dosiahnutie ustálenej koncentrácie liečiva je 4-5t ½ a nezávisí od rýchlosti infúzie (veľkosti podanej dávky)
2) so zvýšením rýchlosti infúzie (podanej dávky) sa hodnota C SS tiež zvyšuje proporcionálne
3) eliminácia lieku z tela po ukončení infúzie trvá 4-5 t ½.
Сss - rovnovážna stacionárna koncentrácia- koncentrácia liečiv dosiahnutá pri rýchlosti podávania rovnajúcej sa rýchlosti vylučovania, preto:
![]() (z definície povolenia)
(z definície povolenia)
Pre každý nasledujúci polčas sa koncentrácia liečiva zvyšuje o polovicu zostávajúcej koncentrácie. Všetky lieky, ktoré dodržiavajú zákon o eliminácii prvého poriadku, sú dosiahne Css za 4-5 polčasov.
Prístupy k riadeniu úrovne Css: zmeniť podanú dávku lieku alebo interval podávania
16. Prerušované podávanie liekov. Kinetika koncentrácie liečiva v krvi, rozsah terapeutických a toxických koncentrácií. Výpočet stacionárnej koncentrácie (C ss), hranice jej kolísania a jej kontrola. Primeraný diskrétny interval dávkovania.
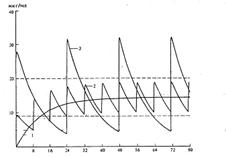 Kolísanie koncentrácie liečiv v krvnej plazme: 1 - s konštantným intravenóznym kvapkaním; 2 - s čiastočným zavedením rovnakej dennej dávky s intervalom 8 hodín; 3 - so zavedením dennej dávky s intervalom 24 hodín.
Kolísanie koncentrácie liečiv v krvnej plazme: 1 - s konštantným intravenóznym kvapkaním; 2 - s čiastočným zavedením rovnakej dennej dávky s intervalom 8 hodín; 3 - so zavedením dennej dávky s intervalom 24 hodín.
Prerušované podávanie lieku- zavedenie určitého množstva liekov v určitých intervaloch.
Rovnovážna koncentrácia v rovnovážnom stave sa dosiahne po 4-5 polovičných eliminačných periódach, čas na jej dosiahnutie nezávisí od dávky (na začiatku, keď je hladina koncentrácie liečiva nízka, je nízka aj rýchlosť jeho eliminácie; s narastajúcim množstvom látky v organizme sa zvyšuje aj rýchlosť jej vylučovania, preto skôr či neskoro príde okamih, keď zvýšená rýchlosť vylučovania vyrovná podanú dávku liečiva a ďalšie zvyšovanie koncentrácie sa zastaví)
Css je priamo úmerná dávke liečiva a nepriamo úmerná intervalu medzi injekciami a klírensom liečiva.
Hranice swingu CSS: ![]() ; C ss min = C ss max × (1 - e-mail). Kolísanie koncentrácie liečiva je úmerné T/t 1/2.
; C ss min = C ss max × (1 - e-mail). Kolísanie koncentrácie liečiva je úmerné T/t 1/2.
Terapeutický rozsah (bezpečnostná chodba, terapeutické okienko)- Toto je rozsah koncentrácií od minimálnej terapeutickej po spôsobenie prvých príznakov vedľajších účinkov.
Toxický rozsah- rozsah koncentrácie od najvyššej terapeutickej po smrteľnú.
Adekvátne podávanie oddelených dávok: spôsob podávania, pri ktorom kolísanie koncentrácie liečiva v krvi spadá do terapeutického rozsahu. Na určenie adekvátneho režimu podávania lieku je potrebné vypočítať. Rozdiel medzi Css max a Css min by nemal presiahnuť 2Css.
Kontrola fluktuácií CSS:
Rozsah kolísania Css je priamo úmerný dávke liečiva a nepriamo úmerný intervalu jeho podávania.
1. Zmeňte dávku liekov: so zvyšovaním dávky liečiva sa úmerne zvyšuje rozsah kolísania jeho Css
2. Zmeňte interval podávania lieku: s predlžovaním intervalu podávania lieku úmerne klesá rozsah kolísania jeho Css
Súčasne zmeňte dávku a interval podávania
Úvodná (nasycovacia) dávka. Terapeutický význam, výpočet podľa farmakokinetických parametrov, podmienky a obmedzenia jeho použitia.
Úvodná (nasycovacia) dávka- dávka podaná naraz a vypĺňajúca celý distribučný objem v aktuálnej terapeutickej koncentrácii. VD = (Css * Vd) / F; = mg/l, = l/kg
Terapeutický význam: úvodná dávka rýchlo poskytuje účinnú terapeutickú koncentráciu liečiva v krvi, čo umožňuje napríklad rýchlo zastaviť záchvat astmy, arytmie atď.
Úvodná dávka sa môže podať len vtedy, keď proces distribúcie látky sa ignoruje
Obmedzenie používania VD: ak je liek distribuovaný oveľa pomalšie ako jeho vstup do krvného obehu, podanie celej nárazovej dávky naraz (najmä intravenózne) vytvorí koncentráciu výrazne vyššiu ako je terapeutická a spôsobí výskyt toxických účinkov. Podmienka používania VD: preto zavedenie nárazových dávok by mala byť vždy pomalá alebo zlomková.
Udržiavacie dávky, ich terapeutický význam a výpočet pre optimálny dávkovací režim.
Terapeutický zmysel: PD kompenzuje straty klírensom počas intervalu medzi injekciami lieku. Výpočet optimálneho dávkovania liekov (pre rýchlu úľavu od záchvatu): ... 1. Výpočet VD: VD = (Css * Vd) / FIndividuálne, vekové a pohlavné rozdiely vo farmakokinetike liekov. Opravy pre výpočet jednotlivých hodnôt pre objem distribúcie liekov.
2. Pohlavné rozdiely v pôsobení drog. Ženy sa vyznačujú nižšou telesnou hmotnosťou ako muži, preto by veľkosť dávok liekov pre nich mala ... 3. Patologické stavy organizmu a účinok liekov a) ochorenie pečene: F lieky v dôsledku invalidizácie prvého- prejsť metabolizmom, zlomok neviazaných liekov v dôsledku nedostatku ...Renálny klírens liečiv, mechanizmy, ich kvantitatívne a kvalitatívne charakteristiky.
Mechanizmy renálneho klírensu a ich charakteristiky: 1. Filtrácia: liečivá uvoľnené len filtráciou (inzulín) budú mať klírens, ... Určené: obličkovým prekrvením, neviazanou frakciou lieku a filtračnou kapacitou obličiek.Faktory ovplyvňujúce renálny klírens liekov. Závislosť klírensu od fyzikálno-chemických vlastností liečiv.
a) glomerulárna filtrácia b) rýchlosť prietoku krvi obličkami c) maximálna rýchlosť sekrécieHepatálny klírens liečiv, jeho determinanty a obmedzenia. Enterohepatálny liekový cyklus.
1) metabolizmus (biotransformácia) oxidáciou, redukciou, alkyláciou, hydrolýzou, konjugáciou atď. Hlavná stratégia metabolizmu xenobiotík: nepolárne látky ® polárne ... 2) sekrécia (vylučovanie netransformovaných látok do žlče)Korekcia liekovej terapie na poškodenie pečene a iné patologické stavy.
Pre úpravu dávkovacieho režimu v prípade ochorenia obličiek pozri odsek 26 vyššie, pre všeobecné zásady korekcie pozri odsek 25. Korekcia dávkovacieho režimu pod kontrolou celkového klírensu liečiva: Korekcia dávky: Dind. = Dtypická × Clind./Cltypická.Korekcia dávkovacieho režimu pod kontrolou zvyškovej funkcie obličiek.
Poznáme: a) reziduálnu funkciu obličiek, ktorá je určená klírensom kreatinínu v danom ... b) celkový klírens daného liečiva (CLP / celkový) a podiel renálneho klírensu liečiva na celkovom klírenseIndividuálna stratégia liekovej terapie.
Uznanie dôležitej úlohy koncentrácie ako prepojenia medzi farmakokinetikou a farmakodynamikou prispieva k vytvoreniu stratégie cieľovej koncentrácie – optimalizovať dávku u daného pacienta na základe merania koncentrácie liečiva. Pozostáva z nasledujúcich etáp:
1. Voľba cieľovej koncentrácie
2. Vypočítajte Vd a Cl na základe typických hodnôt a vykonajte úpravy pre faktory, ako je telesná hmotnosť a funkcia obličiek.
3. Zadanie nasycovacej dávky alebo udržiavacej dávky vypočítanej s prihliadnutím na hodnoty TC, Vd a Cl.
4. Registrácia reakcie pacienta a stanovenie koncentrácie liečiva
5. Revízia V d a Cl na základe výsledkov meraní koncentrácie.
6. Opakujte kroky 3-6, aby ste upravili udržiavaciu dávku potrebnú na optimálnu odpoveď na liek.
Biotransformácia liečiv, jej biologický význam, hlavné smerovanie a vplyv na aktivitu liečiv. Hlavné fázy metabolických premien liečiv v tele.
Biotransformácia liečiv - chemické premeny liečiv v organizme.
Biologický význam biotransformácie liečiv: vytvorenie substrátu, ktorý je vhodný na následnú likvidáciu (ako energetický alebo plastový materiál) alebo na urýchlenie vylučovania liečiv z tela.
Hlavný smer metabolických premien liečiv: nepolárne liečivá → polárne (hydrofilné) metabolity vylučované močom.
Existujú dve fázy metabolických reakcií liekov:
1) metabolická premena (nesyntetické reakcie, fáza 1) - premena látok v dôsledku mikrozomálnej a extramikrozomálnej oxidácie, redukcie a hydrolýzy
2) konjugácia (syntetické reakcie, fáza 2) - biosyntetický proces sprevádzaný pridaním množstva chemických skupín alebo molekúl endogénnych zlúčenín k liečivu alebo jeho metabolitom a) tvorbou glukuronidov b) glycerolestermi c) sulfoestermi d ) acetylácia e) metylácia
Vplyv biotransformácie na farmakologickú aktivitu liečiv:
1) biotransformačné metabolity najčastejšie nemajú farmakologickú aktivitu alebo je ich aktivita v porovnaní s pôvodnou látkou znížená
2) v niektorých prípadoch si metabolity môžu zachovať aktivitu a dokonca prekročiť aktivitu materskej látky (kodeín sa metabolizuje na farmakologicky aktívnejší morfín)
3) niekedy pri biotransformácii vznikajú toxické látky (metabolity izoniazidu, lidokaínu)
4) niekedy v priebehu biotransformácie vznikajú metabolity s opačnými farmakologickými vlastnosťami (metabolity neselektívnych agonistov b 2 - adrenergné receptory majú vlastnosti blokátorov týchto receptorov)
5) mnohé látky sú proliečivá, ktoré spočiatku nevykazujú farmakologické účinky, ale v priebehu biotransformácie sa premieňajú na biologicky aktívne látky (neaktívna L-dopa, prenikajúca do BBB, sa v mozgu mení na aktívny dopamín, pričom žiadne systémové účinky dopamínu).
Klinický význam biotransformácie liečiva. Faktory ovplyvňujúce ich btotransformáciu. Metabolické liekové interakcie.
Vplyv rôznych faktorov na biotransformáciu liečiv: a) funkčný stav pečene: pri jej ochoreniach býva klírens liečiv ... b) vplyv faktorov prostredia: fajčenie podporuje indukciu cytochrómu P450, ako napr. výsledkom je metabolizmus liečiv v ...Spôsoby a mechanizmy vylučovania liečiv z tela. Možnosti kontroly eliminácie liečiva.
Spôsoby a mechanizmy vylučovania liečiva: eliminácia liekov pečeňou a obličkami a niektorými ďalšími orgánmi:
a) obličkami filtráciou, sekréciou, reabsorpciou
b) pečeňou biotransformáciou, vylučovaním žlčou
c) cez pľúca, sliny, pot, mlieko atď. sekréciou, vyparovaním
Možnosti riadenia procesov vysadenia lieku:
1. kontrola pH: v alkalickom moči sa zvyšuje vylučovanie kyslých zlúčenín, v kyslom moči vylučovanie zásaditých zlúčenín.
2.užívanie choleretických liekov (cholenzým, alochol)
3.hemodialýza, peritoneálna dialýza, hemosorpcia, lymfosorpcia
4. Nútená diuréza (IV NaCl alebo glukóza na vodnú záťaž + furosemid alebo manitol)
5.výplach žalúdka, použitie klystírov
Pojem receptorov vo farmakológii, molekulárna podstata receptorov, signalizačné mechanizmy účinku liečiva (typy transmembránovej signalizácie a sekundárnych poslov).
Receptory - molekulárne zložky bunky alebo organizmu, ktoré interagujú s liečivami a vyvolávajú množstvo biochemických dejov vedúcich k rozvoju farmakologického účinku.
Koncept receptorov vo farmakológii:
1. Receptory určujú kvantitatívne vzorce účinku lieku
2. Receptory sú zodpovedné za selektivitu účinku liečiva
3. Receptory sprostredkúvajú pôsobenie farmakologických antagonistov
Koncept receptorov je základom pre cielené používanie liekov, ktoré ovplyvňujú regulačné, biochemické procesy a komunikáciu.
Molekulárna povaha receptorov:
1.regulačné proteíny, sprostredkovatelia pôsobenia rôznych chemických signálov: neurotransmitery, hormóny, autokoidy
2.enzýmy a transmembránové proteínové nosiče (Na +, K + ATPáza)
3. štrukturálne proteíny (tubulín, cytoskeletálne proteíny, bunkový povrch)
4.jadrové proteíny a nukleové kyseliny
Signálne mechanizmy účinku lieku:
1) penetrácia ligandov rozpustných v lipidoch cez membránu a ich účinok na intracelulárne receptory.
2) signálna molekula sa viaže na extracelulárnu doménu transmembránového proteínu a aktivuje enzymatickú aktivitu svojej cytoplazmatickej domény.
3) signálna molekula sa viaže na iónový kanál a reguluje jeho otvorenie.
4) signálna molekula sa viaže na receptor na bunkovom povrchu, ktorý je spojený s efektorovým enzýmom prostredníctvom G-proteínu. G-proteín aktivuje sekundárneho posla.
Typy transmembránovej signalizácie:
a) cez 1-TMS receptory s aktivitou tyrozínkinázy a bez nej
b) prostredníctvom 7-TMS receptorov spojených s G-proteínom
c) cez iónové kanály (závislé od ligandu, od napätia, medzerové kontakty)
Sekundárni sprostredkovatelia: cAMP, ióny Ca2 +, DAG, IF3.
Fyzikálno-chemické a chemické mechanizmy účinku liečivých látok.
Hlavné farmakologické účinky: 1) narkotické 2) celkové depresívne 3) paralyzujúce 4) lokálne dráždivé 5) membranolytické pôsobenie. Chemická povaha látok: chemicky inertné uhľovodíky, étery, alkoholy, ... Mechanizmus účinku - vratná deštrukcia membrán.Selektivita a špecifickosť účinku liečiva. Terapeutické, vedľajšie a toxické účinky liečiv, ich podstata z hľadiska pojmu receptory. Terapeutická stratégia boja proti vedľajším a toxickým účinkom liekov.
Špecifickosť-Väzba liečiv na prísne špecifický typ receptora.
Selektivita- je schopný viazať lieky na jeden alebo viac typov receptorov presnejšie ako iné.
Je vhodnejšie použiť termín selektivita, pretože je nepravdepodobné, že by sa molekula liečiva mohla viazať len na jeden typ molekuly receptora, pretože počet potenciálnych receptorov u každého pacienta je astronomický.
Terapeutické pôsobenie- hlavný požadovaný farmakologický účinok očakávaný od daného farmakologického prípravku.
Vedľajšie účinky- tie účinky, ktoré sa vyskytujú, keď sa látky používajú v terapeutických dávkach a tvoria spektrum ich farmakologického účinku.
Toxické účinky- nežiaduce účinky prejavujúce sa u tohto lieku, keď opustí terapeutické rozmedzie.
Vzťahy medzi terapeutickými a toxickými účinkami liekov na základe analýzy mechanizmov receptor-efektor:
1) terapeutické a toxické účinky sprostredkované rovnakým mechanizmom receptor-efektor (prazosín pôsobí ako alfa-selektívny antagonista na vaskulárnych SMC receptoroch a má hypotenzívny účinok pri esenciálnej hypertenzii, ale pri vysokých dávkach môže pacient pociťovať posturálnu hypotenziu)
2) terapeutické a toxické účinky sprostredkované rovnakými receptormi, ale odlišnými tkanivami alebo rôznymi efektorovými dráhami (srdcové glykozidy sa využívajú na zvýšenie kontraktility myokardu, zároveň narúšajú funkciu gastrointestinálneho traktu, videnie v dôsledku blokády Na + / K + -ATPáza bunkovej membrány)
3) terapeutické a toxické účinky sprostredkované rôznymi typmi receptorov (napríklad norepinefrín má hypertenzný účinok prostredníctvom 1-Ar, ale súčasne spôsobuje tachykardiu prostredníctvom b1-Ar)
Terapeutická stratégia boja proti terapeutickým a vedľajším účinkom liekov:
1.Droga sa má vždy podávať v najmenšej dávke, ktorá spôsobí prijateľný terapeutický účinok
2. Zníženie dávky jedného lieku v dôsledku vymenovania iného lieku s podobným účinkom, ale prostredníctvom rôznych receptorov a s iným profilom toxicity.
3. Selektivitu účinku liečiva možno zvýšiť riadením koncentrácie liečiva v oblasti receptorov rôznych častí tela (lokálne užívanie liečiv - inhalačné použitie salbutamolu pri bronchiálnej astme)
32. Pojmy a pojmy kvantitatívnej farmakológie: účinok, účinnosť, aktivita, agonista (úplný, čiastočný), antagonista. Klinický rozdiel medzi pojmami aktivita a účinnosť liekov.
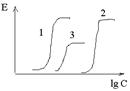 Účinok (odpoveď)- kvantitatívny výťažok reakcie interakcie bunky, orgánu, systému alebo organizmu s farmakologickým činidlom.
Účinok (odpoveď)- kvantitatívny výťažok reakcie interakcie bunky, orgánu, systému alebo organizmu s farmakologickým činidlom.
Efektívnosť- miera reakcie pozdĺž osi účinku - veľkosť odpovede biologického systému na farmakologický účinok; je to schopnosť lieku poskytnúť mu maximálny možný účinok... Tie. v skutočnosti ide o maximálnu veľkosť účinku, ktorú možno dosiahnuť podaním daného lieku. Číselne charakterizovaný hodnotou E max. Čím vyššia je E max, tým vyššia je účinnosť lieku.
Aktivita- miera citlivosti na liečivá pozdĺž koncentračnej osi, charakterizuje afinitu (afinitu ligandu k receptoru), ukazuje, aká dávka (koncentrácia) liečiva je schopná vyvolať vývoj štandardného účinku rovnajúceho sa 50 % maximálne možné pre tento liek. Číselne charakterizované hodnotou EC50 alebo ED50. Čím vyššia je aktivita lieku, tým nižšia je jeho dávka potrebná na reprodukciu terapeutického účinku.
Účinnosť: 1 = 2 > 3
Aktivita: 1> 3> 2
V klinickej praxi je dôležitejšie poznať účinnosť, ako aktivitu, pretože nás skôr zaujíma schopnosť liekov vyvolať v organizme určitý účinok.
Agonista- ligand, ktorý sa viaže na receptor a spôsobuje biologickú odpoveď, aktiváciu fyziologického systému. Úplný agonista- maximálna odozva, čiastočné- spôsobiť menšiu reakciu, aj keď sú obsadené všetky receptory.
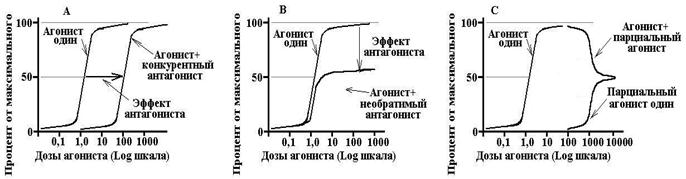 Antagonista- ligandy, ktoré obsadzujú receptory alebo ich menia tak, že strácajú schopnosť interakcie s inými ligandami, ale samy nespôsobujú biologickú reakciu (blokujú pôsobenie agonistov).
Antagonista- ligandy, ktoré obsadzujú receptory alebo ich menia tak, že strácajú schopnosť interakcie s inými ligandami, ale samy nespôsobujú biologickú reakciu (blokujú pôsobenie agonistov).
Konkurenčné antagonisty- interagujú s receptormi reverzibilne a tak súťažia s agonistami. Zvýšenie koncentrácie agonistu môže úplne eliminovať účinok antagonistu. Kompetitívny antagonista posúva krivku dávka-odozva pre agonistu, zvyšuje EC50, neovplyvňuje E max.
Nekonkurenčné antagonisty- ireverzibilne menia afinitu receptorov k agonistovi, často nedochádza k väzbe s aktívnym miestom receptora, zvýšenie koncentrácie agonistu neeliminuje účinok antagonistu. Nekompetitívny antagonista znižuje Emax, nemení EC50 a krivka dávka-účinok je stlačená okolo vertikálnej osi.
33. Kvantitatívne vzorce pôsobenia drogy. Zákon znižovania odozvy biologických systémov. Clarkov model a jeho dôsledky. Celkový pohľad na koncentráciu závislosti - účinok v normálnych a lognormálnych súradniciach.
Model Clark-Ariens:
1. Interakcia medzi ligandom (L) a receptorom (R) je reverzibilná.
2. Všetky receptory pre daný ligand sú ekvivalentné a nezávislé (ich saturácia neovplyvňuje ostatné receptory).
3. Účinok je priamo úmerný počtu obsadených receptorov.
4. Ligand existuje v dvoch stavoch: voľný a viazaný na receptor.
A), kde Kd je rovnovážna konštanta, Ke je vnútorná aktivita.
B) Pretože so zvýšením počtu ligandov v určitom časovom bode budú obsadené všetky receptory, potom je maximálny možný počet vytvorených komplexov ligand-receptor opísaný vzorcom:
= [R] × (1)
Účinok je určený pravdepodobnosťou aktivácie receptora po naviazaní na ligand, t.j. jeho vnútornú aktivitu (Ke), preto E = Ke ×. V tomto prípade je účinok maximálny pri Ke = 1 a minimálny a Ke = 0. Prirodzene, maximálny účinok je opísaný pomerom Emax = Ke ×, kde je celkový počet receptorov pre daný ligand
Účinok tiež závisí od koncentrácie ligandu na [C] receptoroch
Z vyššie uvedených vzťahov vyplýva, že EC 50 = Kd
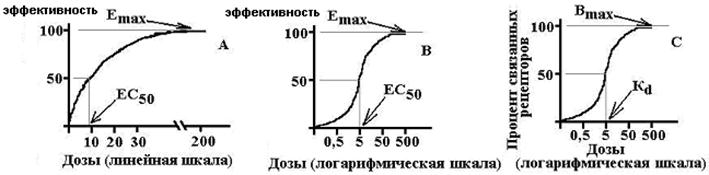
E max je maximálny účinok, B max je maximálny počet naviazaných receptorov, EC 50 je koncentrácia liečiva, pri ktorej nastáva účinok rovnajúci sa polovici maxima, K d je konštanta disociácie látky z receptora, pri. na ktoré je viazaných 50 % receptorov.
Zákon klesajúcej odozvy zodpovedá parabolická závislosť „koncentrácia – účinnosť“. Reakcia na nízke dávky liekov sa zvyčajne zvyšuje priamo úmerne s dávkou... Keď sa však dávka zvyšuje, zvýšenie odpovede sa znižuje a nakoniec možno dosiahnuť dávku, pri ktorej už nedochádza k ďalšiemu zvýšeniu odpovede (v dôsledku obsadenia všetkých receptorov pre daný ligand).
Postupné a kvantové hodnotenie účinku, podstaty a klinických aplikácií. Kvantifikácia aktivity a účinnosti liečiv v experimentálnej a klinickej praxi.
Všetky farmakologické účinky možno zhruba rozdeliť do dvoch kategórií:
a) postupné (kontinuálne, integrálne) efekty- také účinky liekov, ktoré možno kvantitatívne merať (účinok antihypertenzív - podľa hladiny krvného tlaku). Je opísaná postupná „krivka účinku od dávky“ (pozri str. 33), na základe ktorej je možné hodnotiť: 1) individuálnu citlivosť na lieky; 2) lieková aktivita; 3) maximálna účinnosť lieku.
b) kvantové efekty- také účinky drog, ktoré sú diskrétnou veličinou, kvalitatívnym znakom, t.j. popísané len niekoľkými možnosťami stavov (bolesť hlavy po užití analgetika, buď tam alebo nie). Je popísaná kvantová krivka dávka-účinok, kde je zaznamenaná závislosť prejavu účinku v populácii od hodnoty podanej dávky lieku. Graf dávka-účinok má kupolovitý tvar a je identický s Gaussovou normálnou distribučnou krivkou. Na základe kvantovej krivky je možné: 1) odhadnúť populačnú citlivosť na drogy; 2) zaznamenať prítomnosť účinku pri danej dávke; 3) zvoľte priemernú terapeutickú dávku.
Rozdiely medzi postupnými a kvantovými charakteristikami dávka-účinok:
Kvantitatívne hodnotenie aktivity a účinnosti liekov je založené na konštrukcii kriviek dávka-účinok a ich následnom hodnotení (pozri odsek 32).
Druhy účinku lieku. Zmeny v účinku liekov pri ich opakovaní.
1. Podľa lokalizácie: · lokálne - pôsobenie, ktoré sa vyskytuje v mieste aplikácie lieku (zvyčajne kožné a ... · resorpčné - to je účinok, ktorý má liek, keď sa absorbuje do krvného obehu alebo priamo vstrekne do .. .Závislosť účinku liekov od veku, pohlavia a individuálnych schopností tela. Význam cirkadiánnych rytmov.
· Deti - oblasť farmakológie, ktorá študuje charakteristiky účinku liekov na detský organizmus, sa nazýva pediatrická farmakológia. ... · starší ľudia - farmakokinetika...Variabilita a variabilita účinku liečiva. Hypo- a hyperreaktivita, tolerancia a tachyfylaxia, hypersenzitivita a idiosynkrázia. Dôvody variability účinku lieku a racionálna stratégia terapie.
Variabilita účinku liečiva – odráža rozdielnosť farmakologických účinkov jedného liečiva u rôznych jedincov.
Variabilita účinku liečiva – odráža schopnosť liečiva mať účinok, ktorý sa líši od jeho typických farmakologických účinkov.
Varianty variability a variability účinku lieku:
1. Hyporeaktivita- zníženie účinku danej dávky liekov v porovnaní s účinkom, ktorý sa pozoruje u väčšiny pacientov.
2. Hyperreaktivita- zvýšenie účinku danej dávky liekov v porovnaní s účinkom, ktorý sa pozoruje u väčšiny pacientov.
3. Tolerancia- zníženie reakcie tela na opakované injekcie liekov; aby sa obnovila reakcia na lieky, musí sa podávať vo väčších a väčších dávkach.
4. Tachyfylaxia- stav, pri ktorom časté podávanie liekov vyvoláva vznik tolerancie po niekoľkých hodinách, avšak pri dostatočne zriedkavom podávaní liekov je jeho účinok plne zachovaný. Rozvoj tachyfylaxie je zvyčajne spojený s vyčerpaním efektorových systémov.
5. Precitlivenosť- vznik alergickej alebo inej imunitnej reakcie na opakované podávanie liekov.
6. Idiosynkrázia- zvrátená reakcia organizmu na lieky spojená s genetickými charakteristikami metabolizmu liekov alebo individuálnou imunologickou reaktivitou.
Hlavné dôvody variability účinku lieku:
1) zmena koncentrácie látky v receptorovej zóne - v dôsledku rozdielov v rýchlosti absorpcie, jej distribúcie, metabolizmu, eliminácie
2) odchýlky v koncentrácii endogénneho ligandu - receptora - propranololu (β-blokátora) spomaľujú srdcovú frekvenciu u ľudí so zvýšenou hladinou katecholamínov v krvi, ale neovplyvňujú srdcovú frekvenciu na pozadí u športovcov.
3) zmeny v hustote alebo funkcii receptorov.
4) zmeny v reakčných zložkách umiestnených distálne od receptora.
Stratégia racionálnej terapie: spočíva v tom, že na vymenovanie lieku a na to, aby mal očakávaný účinok, je potrebné vziať do úvahy individuálne faktory tela (vek, pohlavie atď.), rytmy človeka, prítomnosť chronických ochorení a iné abnormality. Je tiež potrebné predvídať vývoj necharakteristických vplyvov, berúc do úvahy všetky možné možnosti variabilita účinku lieku.
Hodnotenie bezpečnosti lieku. Terapeutický index a štandardné bezpečnostné rozpätia.
Na vytvorenie a implementáciu nového lieku sa vynakladajú obrovské prostriedky - od 100 do 350 miliónov dolárov a viac. Tieto náklady zahŕňajú prácu vynaloženú na ... Aby prešli všetky stupne hodnotenia lieku, musia zodpovedať hlavnému ... Hodnotenie bezpečnosti nových liekov sa vykonáva v 2 etapách:Farmakokinetické liekové interakcie (príklady).
Farmakokinetická interakcia liečiv je typ farmakologickej interakcie, t.j. vzájomné pôsobenie liekov, ktoré sa prejaví až vtedy, keď sa spolu dostanú do ľudského tela.
Farmakokinetická interakcia nastáva v štádiu absorpcie, distribúcie a ukladania, metabolizmu a vylučovania.
1. Počas fázy nasávania- tento typ interakcie môže viesť k zvýšeniu alebo zníženiu ich absorpcie. Dá sa tomu vyhnúť, ak interval medzi liekmi trvá najmenej 4 hodiny.
Keď sa liek podáva per os, jeho absorpcia je určená:
· pH média- neionizované lieky sa vstrebávajú v gastrointestinálnom trakte lepšie ako ionizované, preto zvýšenie pH žalúdočnej šťavy zvyšuje vstrebávanie slabých zásad a znižuje vstrebávanie slabých kyselín. Príklad: antacidá, blokátory H 2 -histamínových receptorov inhibujú vstrebávanie ketokonazolu atď. antifungálne lieky, nepriame antikoagulanciá, kyselina acetylsalicylová, barbituráty (takmer úplne zabraňujú ich hypnotickému účinku); zvýšenie pH média zlepšuje absorpciu glibutidu, urýchľuje rozpúšťanie obalu enterosolventných látok.
· priama interakcia v tráviacom trakte- tvorba chelátových komplexov a zlúčenín, ktoré sa nevstrebávajú v gastrointestinálnom trakte. NS Príklady: aktívne uhlie tvorí s liekmi nerozpustné zlúčeniny, ktoré bránia ich absorpcii v prípade otravy; tetracyklíny interagujú s vápnikom, hliníkom, železom, horčíkom za vzniku chelátových komplexov, preto ich absorpcia klesá pri použití antacíd, bizmutových prípravkov; fluorochinolóny + antacidá alebo sukralfát = znížená účinnosť antibiotickej liečby.
· gastrointestinálna motilita- môže spôsobiť zrýchlenie alebo spomalenie absorpcie liečiva. Príklady: prokinetiká (metoklopromid) urýchľujú vstrebávanie rýchlo absorbovaných liekov (etanol, paracetamol, tetracyklín) a spomaľujú tie, ktoré sa vstrebávajú pomaly (digoxín, cimetidín); laxatíva znižujú absorpciu a biologickú dostupnosť liekov; pri užívaní anticholinergík, blokátorov H 2 -histamínových receptorov (predĺženie doby prechodu liečiv gastrointestinálnym traktom) zvyšuje biologickú dostupnosť a vstrebávanie srdcových glykozidov, prípravkov železa, čo môže viesť k prejavom toxických účinkov.
· črevnú mikroflóru- priamo sa podieľa na vstrebávaní liekov, preto sa každá dysbióza prejavuje poruchami vstrebávania liekov. Príklady: digoxín + erytromycín = zvýšenie koncentrácie digoxínu v krvi a rozvoj nežiaducich účinkov; perorálne kontraceptíva + širokospektrálne AB = znížený antikoncepčný účinok
· poškodenie črevného CO- inhibuje vstrebávanie niektorých liekov. Príklady: cytostatiká (cyklofosfamid) inhibujú absorpciu digoxínu; zhoršená absorpcia prípravkov železa, kyanokobalamínu, kyseliny listovej.
V štádiu distribúcie a vkladu
· Konkurenčné vytesnenie z väzby s albumínom krvnej plazmy – ak je liek spojený s proteínmi menej ako 90 %, potom vytesnenie z väzby s ním nevedie k ... · vytesnenie z väzby s proteínmi v tkanivách: chinidín vytesňuje digoxín + ... 3. V štádiu metabolizmu - lieky môžu zvyšovať alebo znižovať aktivitu enzýmových systémov zapojených do metabolizmu liekov (...V štádiu liahnutia
· Zmeny tubulárnej sekrécie - chinidín + digoxín = zvýšená koncentrácia digoxínu v krvi a rozvoj toxických účinkov (chinidín ... · zmeny tubulárnej reabsorpcie - iba reabsorpcia je ...Vedľajšie a toxické účinky liečivých látok. Teratogénne, embryotoxické, mutagénne účinky liekov. Lekárske a sociálne aspekty boja proti drogovej závislosti, drogovej závislosti a alkoholizmu. Koncept zneužívania návykových látok.
Vedľajšie účinky- tie účinky, ktoré sa vyskytujú, keď sa látky používajú v terapeutických dávkach a tvoria spektrum ich farmakologického účinku, môžu byť primárne a sekundárne:
a) primárne vedľajšie účinky - ako priamy dôsledok účinku tohto lieku na špecifický substrát (hyposalivácia pri použití atropínu na odstránenie bradyarytmie)
b) sekundárne vedľajšie účinky – nepriame účinky (AB, potlačenie normálnej mikroflóry, môže viesť k superinfekcii)
Toxické účinky- nežiaduce účinky prejavujúce sa u tohto lieku, keď opustí terapeutické rozmedzie (predávkovanie liekom)
Selektivita účinku liečiva závisí od jeho dávky. Čím vyššia je dávka lieku, tým je menej selektívny.
Teratogénne pôsobenie- schopnosť liekov pri podávaní tehotnej žene spôsobiť anatomické anomálie vývoja plodu (talidomid: fokomélia, antiblastómy: mnohopočetné defekty)
Embryotoxický účinok- nepriaznivý účinok, ktorý nie je spojený s porušením organogenézy v prvých troch mesiacoch tehotenstva. Neskôr sa objaví fetotoxický účinok.
Mutagénny účinok liekov- poškodenie zárodočnej bunky a jej genetického aparátu liečivami, ktoré sa prejavuje zmenou genotypu potomstva (adrenalín, cytostatiká).
Karcinogénny účinok liekov- schopnosť niektorých liekov vyvolať karcinogenézu.
1) Drogová závislosť- stav mysle a / alebo fyzický stav, ktorý je dôsledkom účinku drogy na telo a je charakterizovaný špecifickými behaviorálnymi reakciami, je ťažké prekonať túžbu znovu užívať drogy, aby sa dosiahol špeciálny mentálny efekt alebo aby sa predišlo nepohodliu pri absencii liekov v tele. Drogová závislosť je charakterizovaná:
a) psychická závislosť- rozvoj emocionálneho stresu, keď prestanete užívať drogy. Človek sa cíti prázdny, upadá do depresie, prežíva pocit strachu, úzkosti, jeho správanie sa stáva agresívnym. Všetky tieto psychopatologické symptómy vznikajú na pozadí myšlienok o potrebe vstreknúť si drogu, ktorá spôsobila závislosť. Túžba brať drogy sa môže pohybovať od jednoduchej túžby až po vášnivý smäd po drogách, ktorý absorbuje všetky ostatné potreby a mení sa na zmysel života človeka. Verí sa, že psychická závislosť sa vyvinie, keď si človek uvedomí, že optimálnu pohodu môže dosiahnuť iba zavedením drog. Základom psychickej závislosti je viera človeka v pôsobenie drogy (prípady rozvoja psychickej závislosti na placebe sú popísané v literatúre).
b) fyzická závislosť- porušenie normálneho fyziologického stavu tela, ktoré si vyžaduje neustálu prítomnosť liekov v ňom na udržanie stavu fyziologickej rovnováhy. Vysadenie lieku spôsobuje rozvoj špecifického komplexu symptómov - abstinenčného syndrómu - komplexu duševných a neurovegetatívnych porúch vo forme dysfunkcie v opačnom smere, ako je charakteristické pre pôsobenie (morfín tlmí bolesť, tlmí dýchacie centrum, zužuje zreničky, spôsobuje zápchu, s abstinenčnými príznakmi sa u pacienta objavia neznesiteľné bolesti, časté hlučné dýchanie, zreničky sú rozšírené a vzniká pretrvávajúca hnačka)
v) tolerancie... Tolerancia liekov, ktoré spôsobujú drogovú závislosť, je často prierezová, t.j. vzniká nielen danej chemickej zlúčenine, ale všetkým štruktúrne podobným zlúčeninám. Napríklad u pacientov s drogovou závislosťou od morfínu vzniká tolerancia nielen naň, ale aj na iné opioidné analgetiká.
Pre rozvoj drogovej závislosti nie je prítomnosť všetkých 3 kritérií nevyhnutnou podmienkou.
Opioidy, barbituráty, alkohol spôsobujú silnú fyzickú a psychickú závislosť a toleranciu. Anxiolytiká (diazepam, alprazolam) spôsobujú prevažne psychickú závislosť.
2) Závislosť (drogová závislosť)- Ide o mimoriadne ťažkú formu drogovej závislosti, nutkavé užívanie drog, charakterizované neustále sa zvyšujúcim, neodolateľným nutkaním podávať si tento liek, zvyšujúc jeho dávku. Kompulzívnosť túžby znamená, že potreba podať liek dominuje nad všetkými ostatnými (aj životne dôležitými) potrebami pacienta. Z hľadiska tejto definície je túžba po morfíne drogovou závislosťou, zatiaľ čo túžba po nikotíne je drogová závislosť.
3) Závislý na medicíne- charakterizuje menej intenzívnu túžbu po liekoch, keď odmietnutie liekov vyvoláva len pocit mierneho nepohodlia, bez rozvoja fyzickej závislosti alebo detailného obrazu psychickej závislosti. To. závislosť zahŕňa tú časť drogovej závislosti, ktorá nezodpovedá definícii závislosti. Napríklad už spomínaná drogová závislosť na nikotíne je formou závislosti.
4) Drogová závislosť- neoprávnené užívanie drog v takých dávkach a takými spôsobmi, ktoré sa líšia od uznávaných medicínskych alebo spoločenských štandardov v danej kultúre a v danom čase. To. zneužívanie drog zahŕňa iba sociálne aspekty užívania drog. Príkladom zneužívania je užívanie anabolických steroidov v športe alebo na zlepšenie postavy mladými mužmi.
5) Alkoholizmus- chronické požívanie alkoholu (etylalkoholu), ktoré v dnešnej dobe vedie k poškodeniu mnohých orgánov (pečeň, gastrointestinálny trakt, centrálny nervový systém, kardiovaskulárny systém, imunitný systém) a sprevádzané psycho-fyzickou závislosťou.
6) Zneužívanie látok- chronické zneužívanie rôznych drog (vrátane drog, alkoholu, halucinogénov), prejavujúce sa rôznymi duševnými a somatickými poruchami, poruchami správania a sociálnou degradáciou.
Liečba drogovej závislostiťažká a nevďačná úloha. Doteraz nebola vytvorená účinná metóda, ktorá by zabezpečila úspešnosť liečby u viac ako 30 – 40 % pacientov. Dosiahnutie akýchkoľvek badateľných výsledkov je možné len pri plnej spolupráci úsilia pacienta, lekára a sociálneho prostredia, v ktorom sa chorý človek nachádza (princíp dobrovoľnosti a individuality). Moderné techniky sú založené na nasledujúcich princípoch:
Psychoterapeutické a ergoterapeutické metódy;
Skupinová liečba a rehabilitácia (spoločnosť anonymných alkoholikov, drogovo závislých)
Postupné alebo náhle vysadenie lieku počas detoxikačnej terapie
Substitučná terapia (náhrada omamnej látky pomaly a dlhodobo pôsobiacimi analógmi s ich následným zrušením, napr. program tzv. metadónovej substitučnej terapie pre závislých od heroínu)
Liečba špecifickými antagonistami (naloxón a naltrexón) alebo senzibilizačnými látkami (teturam)
Neurochirurgické metódy kryodeštrukcie cingulárneho gyrusu a hipokampu
42. Farmaceutické liekové interakcie. Upozornenia a opatrenia pre fluidnú terapiu.
Farmaceutické interakcie - typ interakcie spojenej s fyzikálno-chemickou reakciou medzi liečivami počas výroby lieku, ešte pred zavedením týchto látok do ľudského tela
a) typické chyby vedúce k farmaceutickej inkompatibilite: vypisovanie zložitých receptov, nesprávne skladovanie, neberie sa do úvahy možnosť adsorpcie liečiv na povrchu plastov (organické dusičnany)
b) problémy s infúznou terapiou: miešanie rozpustných solí, derivátov nerozpustných slabých kyselín alebo zásad vedie k ich zrážaniu; v tekutých liekových formách sa hydrolyzujú srdcové glykozidy a alkaloidy, ničí sa AB; pH média (alkaloidy sa vyzrážajú v alkalickom prostredí)
c) odporúčania: 1) Všetky zmesi je lepšie pripravovať ex tempore 2) Najspoľahlivejšie je riešenie s jedným liečivom 3) Všetky roztoky sa musia pred použitím skontrolovať na suspenzie 4) K interakcii môže dôjsť bez viditeľných zmien roztokov 5) Lieky nemôžu pridávať do krvi a roztokov AK 6) Pri absencii špeciálnych pokynov je potrebné prípravky rozpustiť v 5% roztoku glukózy (pH 3,5-6,5), izotonickom roztoku NaCl (pH 4,5-7,0).
Roztok glukózy stabilizovaný HCl je nekompatibilný s epinefrínom, benzylpenicilínom, apomorfínom, kanamycínom, vitamínom C, oleandomycínom, srdcovými glykozidmi. Srdcové glykozidy sú nekompatibilné s atropínom, papaverínom, platifilínom. AB sú inkompatibilné s heparínom, hydrokortizónom. Vitamíny skupiny B sú navzájom nekompatibilné, s vitamínmi PP, C. Vitamíny PP a C sú tiež navzájom nekompatibilné.
Nemožno miešať s inými liekmi: fenotiazid, chlórpromazín, barbituráty, prípravky vitamínu C, amfotericín B, furosemid, sulfadiazín, aminofylín, adrenomimetiká.
Druhy farmakoterapie. Deontologické problémy farmakoterapie.
1. etiotropná PT - korekcia a eliminácia príčiny ochorenia (AB pri infekčných ochoreniach) 2. patogenetická PT - vplyv na mechanizmus rozvoja ochorenia (inhibítory ... 3. symptomatická PT - eliminácia symptómov ochorenia, ak je nemožné ovplyvniť jej príčinu alebo patogenézu (NSAID...Základné princípy liečby a prevencie otravy liekmi. Antidotová terapia (príklady).
Klasifikácia toxických látok (OM):
1. Tým, že patrí do určitých tried chemických zlúčenín: barbituráty, benzodiazepíny, kyanidy.
2. Podľa pôvodu: nebiologickej povahy (kyseliny, zásady, soli ťažkých kovov), toxické splodiny niektorých MB (botulotoxín), rastlinného pôvodu (alkaloidy, glykozidy), živočíšneho pôvodu (hadí a včelí jed)
3. Podľa stupňa toxicity: a) extrémne toxické (DL50< 1 мг/кг) б) высоко токсические (1-50) в) сильно токсические (50-500) г) умеренно токсические (500-5000) д) мало токсические (5000-15000) е) практически нетоксические (> 15.000)
4. Toxikologickým účinkom: a) nervovo paralytické (bronchospazmus, dýchavičnosť) b) kožné resorpčné c) celkové toxické (hypoxické kŕče, kóma, paralýza) d) dusivé e) slzné a dráždivé e) psychotropné (zhoršená duševná činnosť, vedomie )
5. V závislosti od oblasti preferenčného použitia: priemyselné jedy, pesticídy, jedy pre domácnosť, chemické bojové látky, liečivé látky.
6. V závislosti od toxicity liečiv: Zoznam A - liečivá, ktorých účel, použitie, dávkovanie a skladovanie treba vzhľadom na ich vysokú toxicitu robiť veľmi opatrne. Rovnaký zoznam zahŕňa drogy, ktoré spôsobujú drogovú závislosť; zoznam B - lieky, ktorých vymenovanie, užívanie, dávkovanie a skladovanie by sa malo vykonávať opatrne v súvislosti s možnými komplikáciami pri ich užívaní bez lekárskeho dohľadu.
Selektívne toxický účinok liekov.
a) kardiotoxické: srdcové glykozidy, prípravky draslíka, antidepresíva
b) neurotoxické: psychofarmakologické látky, oxychinolíny, aminoglykozidy
c) hepatotoxické: tetracyklíny, chloramfenikol, erytromycín, paracetamol
d) nefrotoxické: vankomycín, aminoglykozidy, sulfónamidy
e) gastroenterotoxické: steroidné protizápalové lieky, NSAID, rezerpín
f) hematotoxické: cytostatiká, chloramfenikol, sulfónamidy, dusičnany, dusitany
g) pneumotoxické
Toxikokinetika - študuje absorpciu, distribúciu, metabolizmus a vylučovanie liekov užívaných v toxických dávkach.
Vstup toxických látok do organizmu je možný a) enterálne b) parenterálne. Rýchlosť a úplnosť absorpcie odráža rýchlosť rozvoja toxického účinku a jeho závažnosť.
Distribúcia v tele: Vd = D / Cmax - skutočný objem, v ktorom sa jedovatá látka distribuuje v tele. Vd> 5-10 l / kg - OM je ťažko tolerovaný na jeho odstránenie (antidepresíva, fenotiazíny). Vd< 1 л/кг – ОВ легче удалить из организма (теофиллин, салицилаты, фенобарбитал).
Predávkovanie- zmeny vo farmakokinetických procesoch: rozpustnosť, spojenie s bielkovinami, metabolizmus ® výrazné zvýšenie voľnej frakcie liečiv ® toxický účinok.
Kinetika prvého rádu sa so zvýšením koncentrácie liečiva transformuje na kinetiku nultého rádu.
Toxigénne štádium je detoxikačná terapia, somatogénne štádium je symptomatická terapia.
Toxikodynamika . Hlavné mechanizmy toxického účinku:
a) mediátor: priamy (podľa typu kompetitívnej blokády - FOS, psychomimetiká) a nepriamy (aktivátory alebo inhibítory enzýmov)
b) interakcia s biomolekulami a vnútrobunkovými štruktúrami (hemolytické látky)
c) metabolizmus podľa typu letálnej syntézy (etylalkohol, tiofos)
d) enzymatické (hadie jedy atď.)
Typy pôsobenia: lokálne, reflexné, resorpčné.
Klasifikácia otravy:
1. Etiopatogenetické:
a) náhodné (samoliečba, chybný príjem)
b) úmyselné (s cieľom samovraždy, vraždy, rozvinutia bezmocného stavu u obete)
2. Klinické:
a) v závislosti od rýchlosti rozvoja otravy: akútna (podanie jednorazovej dávky alebo s krátkym časovým odstupom toxickej dávky látky), subakútna (oneskorený vývoj klinického obrazu po jednorazovej dávke), chronická
b) v závislosti od prejavu hlavného syndrómu: poškodenie CVS, poškodenie DS a pod.
c) v závislosti od závažnosti stavu pacienta: ľahký, stredný, ťažký, mimoriadne ťažký
3. Nozologické: zohľadňuje názov lieku, názov skupiny látok
Všeobecný mechanizmus smrti v prípade otravy:
a) porážka CVS:
1) zníženie krvného tlaku, hypovolémia periférnych ciev, kolaps, bradykardia alebo tachykardia (tricyklické antidepresíva, betablokátory, blokátory vápnikových kanálov)
2) arytmie (ventrikulárna tachykardia, fibrilácia - tricyklické antidepresíva, teofylín, amfetamín)
b) poškodenie centrálneho nervového systému: stupor, kóma ® útlm dýchania (lieky, barbituráty, alkohol, hypnosedatíva)
c) kŕče, svalová hyperreaktivita a stuhnutosť ® hypertermia, myoglobinúria, zlyhanie obličiek, hyperkaliémia
Toxikologická triáda:
1) dĺžka užívania, dávka a anamnéza látky ® .
2) posúdenie stavu vedomia podľa symptómov: dýchanie, krvný tlak, telesná teplota
3) laboratórne údaje
Základné princípy liečby:
ja Prvá pomoc: umelé dýchanie, masáž srdca, protišoková terapia, kontrola rovnováhy voda-elektrolyt
II. Oneskorené vstrebávanie a odstraňovanie nevstrebaného OM z tela:
Účel: ukončiť kontakt s OV
1. Parenterálna cesta:
a) cez pľúca:
1) zastavte inhaláciu
2) dráždivé látky (amoniak, formaldehyd) ® na upevnenie aktívnych pohybov, zahriatie, dodanie kyslíka a odpeňovače (pre amoniak je odpeňovač ocot a pre formaldehyd zriedený roztok amoniaku)
b) cez kožu: zmyť veľkým množstvom teplej vody s mydlom alebo saponátom, špecifickými protilátkami, neutralizovať a ukončiť expozíciu OM na koži (FOS: umyť vodou, odstrániť 10-15% amoniakom alebo 5- 6% roztok hydrogénuhličitanu sodného s vodou; fenolkrezol: rastlinný olej alebo etylénglykol, ale nie vazelínový olej, KMNO 4: 0,5-1% roztok kyseliny askorbovej alebo rovnaké objemy 3% roztoku peroxidu vodíka a 3% roztoku kyseliny octovej, CCl 4, terpentín , benzín: teplá mydlová voda)
c) pri injekcii do končatiny: turniket nad miestom vpichu
d) pri zasiahnutí očí: vyplachovať teplým fyziologickým roztokom alebo mliekom 10-20 minút, kvapkať lokálne anestetikum; v prípade kontaktu s kyselinami a zásadami ich nemožno neutralizovať. Vyžaduje sa konzultácia s oftalmológom.
2. Enterálna cesta: na uvoľnenie žalúdka z OM, na urýchlenie pasáže
a) odstránenie OM:
1) predbežný príjem vody. Neužívajte mlieko (s výnimkou žieravých jedovatých látok) a etanol (s výnimkou metanolu).
2) vracanie - indikované hlavne pri otravách veľkými tabletami alebo kapsulami, ktoré nemôžu prejsť cez sondu. Môže byť vyvolaná reflexne alebo vracaním (NaCl: 1 polievková lyžica na 1 pohár vody; sirup Ipecac: dospelí 2 polievkové lyžice, deti 2 čajové lyžičky; horčica: 1-2 čajové lyžičky na pohár vody; apomorfín: 5-10 mg / kg subkutánne, okrem detí mladších ako 5 rokov). Po požití nevyvolávať zvracanie: organické rozpúšťadlá - nebezpečenstvo vdýchnutia, saponáty - penenie, kŕčovité látky - nebezpečenstvo vdýchnutia, žieraviny - poškodenie pažeráka)
3) sonda výplach žalúdka - je núdzové a povinné opatrenie. Žalúdok sa umyje, ak od otravy neuplynulo viac ako 4-6 hodín, niekedy až 10 hodín; pri otrave kyselinou acetylsalicylovou - po 24 hodinách. Pacient je predintubovaný hadičkou s nafukovacou manžetou: v kóme bez kašľa a laryngeálneho reflexu. Žalúdok sa premyje vodou alebo soľným roztokom 30 ° C, postup trvá 4 hodiny alebo viac. Na konci premývania aktívne uhlie a síran sodný.
b) zníženie absorpcie z gastrointestinálneho traktu: aktívne uhlie vo vnútri po vyprázdnení žalúdka + síran sodný alebo horečnatý. Vlastnosti opatrení na zníženie absorpcie:
1) organické rozpúšťadlá: nevyvolávať zvracanie, výplach žalúdka po intubácii, aktívne uhlie + tekutý parafín
2) pracie prostriedky: nevyvolávať zvracanie a vyplachovať žalúdok, je potrebné podať veľa vody + odpeňovače (simetikon)
3) kyseliny a zásady: zvracanie nie je možné vyvolať, výplach žalúdka cez hadičku namazanú rastlinným olejom po podaní narkotického analgetika je jedinou indikáciou na podávanie mlieka. Pri otravách kyselinou - antacidá, pri otravách zásadami - kyselina citrónová alebo octová.
III. Odstránenie absorbovaného OM z tela
a) forsírovaná diuréza (podmienky: dostatočný prietok krvi obličkami a glomerulárna filtrácia; vyliať-vyliať 20-25 litrov za 24 hodín)
b) peritoneálna hemodialýza
c) hemosorpcia
d) výmenná transfúzia krvi
e) nútená hyperventilácia
IV. Symptomatická liečba funkčných porúch.
2) toxikokinetické - urýchľujú biotransformáciu OM (trimedoxím bromid, tiosíran sodný, etanol, AO) 3) farmakologické - atropín, naloxón 4) imunologické antidotáPravidlá predpisovania jedovatých, omamných a silných liekov.
Predpisy na omamné látky (morfín, omnopon, promedol, fenamín, kokaín atď.) a tie, ktoré sa im prirovnávajú, bez ohľadu na drogy. f-sme predpísané na špeciálne... V prípade, že lek. Svadobný obsah. alkoholu, potom sa tesnenie položí. inštitúcií “Pre... V prípadoch, keď je max. dávka jedovatého alebo silného. in-in prekračovať, povinné. uveďte ich počet slovami s pridaním ...Čo urobíme s prijatým materiálom:
Ak sa ukázalo, že tento materiál je pre vás užitočný, môžete si ho uložiť na svoju stránku v sociálnych sieťach:









