Splošna farmakologija. Farmakodinamika. Dejavniki, ki vplivajo na farmakokinetiko in farmakodinamiko. Klinični pomen biotransformacije zdravil. Dejavniki, ki vplivajo na njihovo btotransformacijo. Metabolične interakcije z zdravili. Vzdrževalni odmerki, njihove terapije
1. Koncept zdravljenja kot usmerjene korekcije fizioloških motenj v telesu. Prednosti in tveganja uporabe zdravil. Razlogi za njihovo uporabo. Ocena varnosti.
farmakologija – teoretično podlago farmakoterapija.
Razlogi za uporabo drog:
1) popraviti in odpraviti vzrok bolezni
2) v primeru nezadostnih preventivnih ukrepov
3) iz zdravstvenih razlogov
4) očitna potreba na podlagi ravni znanja in izkušenj
5) prizadevanje za izboljšanje kakovosti življenja
Prednosti pri predpisovanju zdravil:
1) popravek ali odprava vzroka bolezni
2) lajšanje simptomov bolezni, če je ni mogoče zdraviti
3) nadomestitev zdravilnih snovi z naravnimi biološko aktivnimi snovmi, ki jih organizmi ne proizvajajo v zadostnih količinah
4) izvajanje preventive bolezni (cepiva ipd.)
Tveganje- verjetnost, da bo zaradi izpostavljenosti nastala škoda ali škoda; je enako razmerju med številom neželenih (averzivnih) dogodkov in velikostjo rizične skupine.
A) nesprejemljivo (škoda > korist)
B) sprejemljivo (korist > škoda)
B) nepomemben (105 - stopnja varnosti)
D) zavestno
Ocenjevanje varnosti zdravil se začne na ravni kemičnih laboratorijev, ki sintetizirajo zdravila. Predklinično oceno varnosti zdravil izvaja Ministrstvo za zdravje, FDA itd. Če je zdravilo uspešno opravljeno tej fazi, se začne njena klinična presoja, ki jo sestavljajo štiri faze: faza I - ocena tolerance na zdravih prostovoljcih, starih 20-25 let, faza II - na bolnih prostovoljcih, ki štejejo manj kot 100 ljudi z določeno boleznijo, faza III - multicentrična klinična preskušanja na velike skupine ljudi (do 1000 ljudi), IV faza - spremljanje zdravila 5 let po uradni odobritvi. Če zdravilo uspešno preide vse te faze, se šteje za varno.
2. Bistvo farmakologije kot znanosti. Sekcije in področja sodobne farmakologije. Glavni izrazi in koncepti farmakologije so farmakološka aktivnost, delovanje, učinkovitost kemikalij.
farmakologija- znanost o zdravilih v vseh pogledih - teoretična osnova terapije:
A) znanost o interakciji kemikalij z živimi sistemi
B) znanost o upravljanju vitalnih procesov telesa s pomočjo kemikalij.
Odseki sodobne farmakologije:
1) Farmakodinamika- preučuje a) vpliv zdravil na človeško telo, b) medsebojno delovanje različnih zdravil v telesu med predpisovanjem, c) vpliv starosti in različnih bolezni na učinek zdravil
2) Farmakokinetika- preučuje absorpcijo, porazdelitev, presnovo in izločanje zdravil (tj. kako se bolnikovo telo odziva na zdravila)
3) Farmakogenetika- preučuje vlogo genetskih dejavnikov pri oblikovanju farmakološkega odziva telesa na zdravila
4) Farmakoekonomija- ocenjuje rezultate uporabe in stroške zdravil za odločitev o njihovi nadaljnji praktični uporabi
5) Farmakoepidemiologija- preučuje uporabo drog in njihove učinke na ravni populacij ali velikih skupin ljudi, da zagotovi uporabo najbolj učinkovitih in varnih zdravil
Farmakološka (biološka) aktivnost- lastnost snovi, da povzroča spremembe v biosistemu (človeško telo). Farmakološke snovi = biološko aktivne snovi (BAS)
farmakološki učinek- vpliv zdravil na predmet in njegove tarče
Farmakološki učinek- rezultat delovanja snovi v telesu (sprememba fizioloških, biokemičnih procesov, morfoloških struktur) - kvantitativna, ne pa kakovostna sprememba stanja biosistemov (celice, tkiva, organi).
Učinkovitost zdravil- sposobnost zdravil, da povzročijo določene farmakološke učinke, ki so v tem primeru potrebni v telesu. Ocenjeno na podlagi "znatnih dokazov" - ustreznih dobro nadzorovanih študij in kliničnih preskušanj, ki jih izvajajo strokovnjaki z ustreznim znanstvenim usposabljanjem in izkušnjami na področju raziskav zdravil te vrste (FDA)
3. Kemična narava zdravil. Dejavniki, ki zagotavljajo terapevtski učinek zdravila- farmakološko delovanje in placebo učinki.
Obstajajo zdravila 1) rastlinska 2) živalska 3) mikrobna 4) mineralna 5) sintetična
Sintetične droge predstavljajo skoraj vsi razredi kemičnih spojin.
farmakološki učinek- vpliv mamil na predmet in njegovo tarčo.
Placebo- katero koli sestavino terapije, ki nima posebnega biološkega učinka na bolezen, ki je predmet zdravljenja.
Uporablja se z namenom nadzora pri ocenjevanju učinka zdravil in v korist bolnika brez farmakoloških učinkovin kot posledica zgolj psihičnega vpliva (tj. Placebo učinek).
Vse vrste zdravljenja imajo psihološko komponento ali zadovoljivo ( Placebo učinek) ali moteče ( Nocebo učinek). Primer placebo učinka: hitro izboljšanje pri bolniku z virusno okužbo pri uporabi antibiotikov, ki ne vplivajo na viruse.
Prednost placebo učinka je povezana s psihološkim vplivom na bolnika. Največja bo le ob uporabi. V kombinaciji z metodami zdravljenja ki imajo izrazit specifičen učinek. Drage snovi kot placebo pomaga tudi pri doseganju večjega odziva.
Indikacije za uporabo placeba:
1) šibke duševne motnje
2) psihološka podpora bolniku z neozdravljivo kronično boleznijo ali sumom, da ima težko diagnozo
4. Viri in faze nastanka zdravil. Opredelitev pojmov zdravila, zdravila, zdravila in dozirne oblike. Ime zdravil.
Viri ustvarjanja zdravil:
A) naravne surovine: rastline, živali, minerali itd. (srčni glikozidi, svinjski inzulin)
B) modificirane naravne biološko aktivne snovi
B) sintetične spojine
D) izdelki genskega inženiringa (rekombinantni insulin, interferoni)
Faze ustvarjanja zdravila:
1. Sinteza zdravil v kemijskem laboratoriju
2. Predklinična ocena delovanja in neželenih učinkov zdravil Ministrstva za zdravje in drugih organizmov
3. Klinična preskušanja zdravil (za več podrobnosti glejte razdelek 1)
Zdravilo- katera koli snov ali izdelek, ki se uporablja za spreminjanje ali raziskovanje fizioloških sistemov ali patoloških stanj v korist prejemnika (po WHO, 1966); posamezne snovi, mešanice snovi ali sestavke neznane sestave z dokazanimi zdravilnimi lastnostmi.
Zdravilna snov- posamezna kemična spojina, ki se uporablja kot zdravilo.
Odmerna oblika- priročno za praktična uporaba oblika, ki se daje zdravilu za dosego želenega terapevtskega ali profilaktičnega učinka.
Zdravilo- zdravilo v posebni dozirni obliki, ki jo odobri državni organ.
5. Poti vnosa zdravil v telo in njihove značilnosti. Presistemsko izločanje zdravil.
1. Za sistemsko delovanje
A. Enteralni način dajanja: peroralno, sublingvalno, bukalno, rektalno, cevno
B. Parenteralni način dajanja: intravensko, subkutano, intramuskularno, inhalacijsko, subarahnoidalno, transdermalno
2. Za lokalno izpostavljenost: kožna (epikutarna), na sluznicah, v votlini (abdominalna, plevralna, sklepna), v tkivu (infiltracija)
|
Pot dajanja zdravila |
dostojanstvo |
Pomanjkljivosti |
|
Oralno - peroralno |
1. Priročno in enostavno za pacienta 2. Sterilnost zdravil ni potrebna |
1. Absorpcija številnih zdravil je odvisna od vnosa hrane, funkcionalnega stanja prebavil in drugih dejavnikov, ki se v praksi komaj upoštevajo. 2. Vsa zdravila se ne absorbirajo dobro v prebavnem traktu 3. Nekatera zdravila se uničijo v želodcu (inzulin, penicilin) 4. Del zdravila ima NLR na sluznici prebavil (NSAID - manifestacije na sluznici, antacidi - zavirajo motorične sposobnosti) 5. Ni uporabno za bolnike v nezavestnem stanju in z okvarjenim požiranjem |
|
Sublingvalno in bukalno |
1. Priročen in hiter uvod 2. Hitra absorpcija zdravil 3. Zdravila niso predmet predsistemske eliminacije 4. Delovanje zdravila se lahko hitro prekine |
1. Nevšečnosti zaradi pogoste redne uporabe tablet 2. Draženje ustne sluznice, prekomerno slinjenje, olajšanje požiranja zdravil in zmanjšanje njegove učinkovitosti 3. Slab okus |
|
rektalno |
1. Polovica zdravil ni podvržena predsistemski presnovi 2. Sluznica prebavil ni razdražena 3. Priročno, kadar so drugi načini dajanja nesprejemljivi (bruhanje, potovalna slabost, dojenčki) 4. Lokalno delovanje |
1. Neprijetni psihološki trenutki za bolnika 2. Absorpcija zdravil se znatno upočasni, ko se danka ne izprazni. |
|
Intravaskularno (običajno intravensko |
1. Hiter vstop v krvni obtok (nujna stanja) 2. Hitro ustvarjanje visoke sistemske koncentracije in sposobnost obvladovanja 3. Omogoča uvedbo zdravil, ki se uničijo v prebavilih |
1. Tehnične težave pri intravaskularnem dostopu 2. Nevarnost okužbe na mestu injiciranja 3. Venska tromboza na mestu injiciranja zdravil (eritromicin) in bolečina (kalijev klorid) 4. Nekatera zdravila se adsorbirajo na stene kapalk (inzulin) |
|
Intramuskularno |
Dovolj hitra absorpcija zdravila v kri (10-30 min) |
Tveganje za lokalne zaplete |
|
Subkutano |
1. Pacient lahko po treningu samostojno injicira. 2. Dolgoročni učinek zdravil |
1. Počasna absorpcija in manifestacija učinka zdravila 2. Atrofija maščobnega tkiva na mestu injiciranja in zmanjšanje hitrosti absorpcije zdravil |
|
Vdihavanje |
1. Hiter začetek delovanja in visoka koncentracija na mestu injiciranja pri zdravljenju bolezni dihal. načine 2. Dobra obvladljivost akcije 3. Zmanjšanje toksičnih sistemskih učinkov |
1. Potreba po posebni napravi (inhalatorju) 2. Težave pri uporabi aerosolov pod tlakom pri nekaterih bolnikih |
|
Lokalni PM |
1. Visoka učinkovita koncentracija zdravil na mestu injiciranja 2. Izognemo se neželenim sistemskim učinkom tega zdravila |
Če je celovitost kože kršena, lahko zdravilo vstopi v sistemski obtok - manifestacija neželenih sistemskih učinkov. |
Presistemsko izločanje zdravil (učinek prvega prehoda)- proces biotransformacije zdravila, preden zdravilo vstopi v sistemski obtok. Encimski sistemi črevesja, krv iz portalne vene in hepatociti so vključeni v presistemsko izločanje s peroralnim dajanjem zdravila.
Pri intravenski uporabi ni predsistemskega izločanja.
Da bi imelo peroralno zdravilo ugoden učinek, je treba povečati njegov odmerek, da se nadomestijo izgube.
6. Prevoz zdravil čez biološke ovire in njegove sorte. Glavni dejavniki, ki vplivajo na transport zdravil v telesu.
Načini absorpcije (transporta) zdravil skozi biološke membrane:
1) Filtracija (difuzija vode) - pasivno premikanje molekul snovi vzdolž koncentracijskega gradienta skozi pore, napolnjene z vodo v membrani vsake celice in med sosednjimi celicami, značilno za vodo, nekatere ione, majhne hidrofilne molekule (sečnina).
2) Pasivna difuzija (lipidna difuzija) je glavni mehanizem prenosa zdravil, proces raztapljanja zdravila v membranskih lipidih in gibanja skozi njih.
3) Transport s posebnimi nosilci - prenos zdravil s pomočjo nosilcev, vgrajenih v membrano (običajno beljakovin) je značilen za hidrofilne polarne molekule, številne anorganske ione, sladkorje, aminokisline, pirimidine:
a) olajšana difuzija - izvedena vzdolž koncentracijskega gradienta brez porabe ATP
b) aktivni transport - proti gradientu koncentracije s stroški ATP
Nasičen proces - to pomeni, da se stopnja absorpcije povečuje le, dokler število molekul zdravila ne postane enako številu nosilcev.
4) Endocitoza in pinocitoza - zdravilo se veže na posebno prepoznavno komponento celične membrane, pride do invaginacije membrane in nastane mehurček, ki vsebuje molekule zdravila. Nato se zdravilo sprosti iz mehurčka v celico ali pa se transportira iz celice. Značilno za polipeptide z visoko molekulsko maso.
Dejavniki, ki vplivajo na transport zdravil v telesu:
1) fizikalne in kemijske lastnosti snovi (hidro- in lipofilnost, ionizacija, polarizabilnost, velikost molekule, koncentracija)
2) struktura transfernih ovir
3) pretok krvi
7. Prevoz zdravilnih substanc s spremenljivo ionizacijo skozi membrane (Henderson-Hasselbalchova ionizacijska enačba). Načela nadzora prenosa.
Vsa zdravila so šibke kisline ali šibke baze, ki imajo svoje vrednosti ionizacijske konstante (pK). Če je pH vrednost medija enaka pK vrednosti zdravila, bo 50 % njegovih molekul v ioniziranem stanju in 50 % v neioniziranem stanju, medij za zdravilo pa bo nevtralen.
V kislem mediju (pH manjši od pK), kjer je presežek protonov, bo šibka kislina v nedisociirani obliki (R-COOH), torej bo vezana na proton - protonirana. Ta oblika kisline je nenapolnjena in je zlahka topna v lipidih. Če se pH premakne na alkalno stran (tj. pH postane večji od pK), se bo kislina začela disociirati in izgubila proton ter prešla v neprotonirano obliko, ki ima naboj in je slabo topna v lipidih. .
V alkalnem mediju, kjer primanjkuje protonov, bo šibka baza v nedisociirani obliki (R-NH2), torej neprotonirana in brez naboja. Ta oblika baze je zelo topna v lipidih in se hitro absorbira. V kislem mediju je protonov presežek in šibka baza bo začela disociirati, medtem ko bo protone vezala in tvorila protonirano, nabito obliko baze. Ta oblika je slabo topna v lipidih in se slabo absorbira.
zato Absorpcija šibkih kislin poteka predvsem v kislem mediju, šibkih baz pa v alkalnem mediju.
Značilnosti presnove šibkih kislin (SC):
1) želodec: SA v kisli vsebini želodca ni ioniziran, v alkalnem mediju tankega črevesa pa se bo disociral in molekule SA bodo pridobile naboj. Zato bo absorpcija šibkih kislin najbolj intenzivna v želodcu.
2) v krvi je medij dovolj alkalen in absorbirane SC molekule se bodo preoblikovale v ionizirano obliko. Filter ledvičnega glomerula omogoča prehod tako ioniziranim kot neioniziranim molekulam, zato se bo SC kljub naboju molekule izločil v primarni urin
3) če je urin alkalen, bo kislina ostala v ionizirani obliki, se ne bo mogla ponovno absorbirati v krvni obtok in se bo izločila z urinom; Če je urin kisel, bo zdravilo prešlo v neionizirano obliko, ki se zlahka absorbira nazaj v kri.
Značilnosti presnove šibkih baz: nasprotno SC (absorpcija je boljša v črevesju; v alkalnem urinu se reabsorbirajo)
to., Za pospešitev izločanja šibke kisline iz telesa je treba urin alkalizirati, za pospešitev izločanja šibke baze pa ga nakisati. (razstrupljanje po Popovu).
Kvantitativna odvisnost procesa ionizacije zdravila pri različnih pH vrednostih medija omogoča, da dobimo enačbo Henderson— Hasselbach:
kjer pKa ustreza vrednosti pH, pri kateri so koncentracije ionizirane in neionizirane oblike v ravnotežju .
Henderson-Hasselbachova enačba omogoča oceno stopnje ionizacije zdravila pri dani pH vrednosti in predvidevanje verjetnosti njegove penetracije skozi celično membrano.
(1)Za razredčeno kislino, A,
HA ↔ H + + A -, kjer je HA koncentracija neionizirane (protonirane) oblike kisline in A - koncentracija ionizirane (neprotonirane) oblike.
(2) Za šibka osnova, B,
BH + ↔ H + + B, kjer je BH + koncentracija protonirane oblike baze, B je koncentracija neprotonirane oblike
Če poznamo pH medija in pKa snovi, je mogoče iz izračunanega logaritma določiti stopnjo ionizacije zdravila in s tem stopnjo njegove absorpcije iz prebavil, reabsorpcije ali izločanja skozi ledvice pri različnih pH vrednosti urina itd.
8. Prenos zdravil v telesu. Difuzija vode in difuzija v lipidih (Fickov zakon). Aktivni transport.
Prenos zdravil v telesu se lahko izvaja z difuzijo vode in lipidov, aktivnim transportom, endo- in pinocitozo.
Značilnosti prenosa zdravil v telesu z difuzijo vode:
1. Epitelijske obloge (sluznice gastrointestinalnega trakta, ustne votline itd.) - difuzija vode le zelo majhnih molekul (metanol, litijevi ioni itd.)
2. Kapilare (razen cerebralnih) - filtracija snovi z molekulsko maso do 20-30 tisoč Da.
3. Kapilare možganov - v bistvu nimajo vodnih por, z izjemo predelov hipofize, epifize, prekata IV cone, horoidnega pleksusa, mediane eminence
4. Placenta - nima vodnih por (čeprav je vprašanje sporno).
5. Vezava zdravil na krvne beljakovine preprečuje njihov izstop iz krvnega obtoka in s tem difuzijo vode
6. Difuzija v vodi je odvisna od velikosti molekul zdravila in vodnih por
Značilnosti difuzije lipidov:
1. Glavni mehanizem prenosa zdravila čez celične membrane
2. Določena z lipofilnostjo difuzijske snovi (tj. koeficientom porazdelitve "olje/voda") in koncentracijskim gradientom je lahko omejena z zelo nizko topnostjo snovi v vodi (ki preprečuje prodiranje zdravila v vodna faza membran)
3. Nepolarne spojine zlahka razpršijo, ione je težko difundirati.
Vsaka difuzija (tako voda kot lipidi) upošteva Fickov zakon difuzije:
Hitrost difuzije - število molekul zdravila, ki se prenašajo na enoto časa; C1 je koncentracija snovi zunaj membrane; C2 je koncentracija snovi iz notranjosti membrane.
Posledica Fickovega zakona:
1) večja je filtracija zdravila, večja je njegova koncentracija na mestu injiciranja (S absorbirane površine v črevesju je večji kot v želodcu, zato je absorpcija zdravila v črevesju hitrejša)
2) višja kot je koncentracija zdravila na mestu injiciranja, višja je filtracija zdravila
3) večja je filtracija zdravil, manjša je debelina biološke membrane, ki jo je treba premagati (debelina pregrade v pljučnih alveolah je veliko manjša od kože, zato je stopnja absorpcije višja v pljuča)
Aktivni transport- prenos zdravil, ne glede na koncentracijski gradient z uporabo energije ATP, je značilen za hidrofilne polarne molekule, številne anorganske ione, sladkorje, aminokisline, pirimidine. Značilen po: a) selektivnost za določene spojine b) možnost konkurence dveh snovi za en transportni mehanizem c) nasičenost pri visokih koncentracijah snovi d) možnost transporta proti koncentracijskemu gradientu e) poraba energije.
9. Osrednji postulat farmakokinetike je koncentracija zdravila v krvi – glavni parameter za nadzor terapevtskega učinka. Problemi rešeni na podlagi poznavanja tega postulata.
Osrednji postulat (dogma) farmakokinetike: koncentracija zdravil v krvni plazmi določa (kvantitativno določa) farmakološki učinek.
V večini primerov je stopnja absorpcije, porazdelitve, presnove in izločanja zdravil sorazmerna z njihovo koncentracijo v krvni plazmi (upošteva zakon množičnega delovanja), torej, če vemo, da je možno:
1) določiti razpolovni čas (za zdravila s kinetiko prvega reda)
2) pojasnite trajanje nekaterih toksičnih učinkov zdravil (za zdravila v visoki odmerki s kinetiko nasičenosti)
10. Biološka uporabnost zdravil - definicija, bistvo, kvantitativni izraz, determinante. Biološka uporabnost
Biološka uporabnost (F) - označuje popolnost in hitrost absorpcije zdravil z izvensistemskimi načini dajanja - odraža količino nespremenjene snovi, ki je dosegla sistemski krvni obtok, glede na začetni odmerek zdravila.
F je 100 % za zdravila, ki se dajejo intravensko. Pri dajanju na druge načine je F običajno manjši zaradi nepopolne absorpcije in delne presnove v perifernih tkivih. F je 0, če se zdravilo ne absorbira iz lumna gastrointestinalnega trakta.
Za oceno F je narisana krivulja kot funkcija koncentracije zdravila v krvi glede na čas po intravenskem dajanju, pa tudi po dajanju po preiskani poti. To je t.i. farmakokinetične krivulje razmerja "čas-koncentracija". Površino pod farmakokinetično krivuljo najdemo z integracijo in F se izračuna kot razmerje:
![]() ≤ 1, kjer je AUC površina pod krivuljo
≤ 1, kjer je AUC površina pod krivuljo
Biološka uporabnost> 70 % velja za visoko, pod 30 % - nizko.
Determinatorji biološke uporabnosti:
1) hitrost sesanja
2) popolnost absorpcije - nezadostna absorpcija zdravil zaradi zelo visoke hidrofilnosti ali lipofilnosti, presnova črevesnih bakterij pri enteralnem dajanju itd.
3) predsistemsko izločanje - z visoko biotransformacijo v jetrih so zdravila F nizka (nitroglicerin pri peroralni uporabi).
4) dozirna oblika - sublingvalne tablete in rektalne supozitorije pomagajo zdravilom, da se izognejo predsistemskemu izločanju.
11. Porazdelitev zdravil v telesu. Kompartmenti, ligandi. Glavne determinante distribucije.
Distribucija Droge - proces širjenja zdravil po organih in tkivih po vstopu v sistemski krvni obtok.
Razdelna mesta:
1. Zunajcelični prostor (plazma, medcelična tekočina)
2. Celice (citoplazma, membrana organelov)
3. Maščobno in kostno tkivo (odlaganje zdravil)
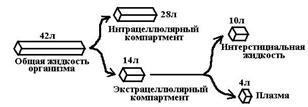 Pri osebi, ki tehta 70 kg, je prostornina tekočega medija skupaj 42 litrov, če:
Pri osebi, ki tehta 70 kg, je prostornina tekočega medija skupaj 42 litrov, če:
[Vd = 3-4 L, potem se vse zdravilo porazdeli v krvi;
[Vd = 4-14 L, potem se vse zdravilo porazdeli v zunajcelično tekočino;
[Vd = 14-42 l, potem se vse zdravilo približno enakomerno porazdeli po telesu;
[Vd> 42 L, potem se vse zdravilo nahaja predvsem v zunajceličnem prostoru.
Molekularni ligandi zdravil:
A) specifični in nespecifični receptorji
B) krvne beljakovine (albumin, glikoprotein) in tkiva
C) polisaharidi vezivnega tkiva
D) nukleoproteini (DNK, RNA)
Določilnice distribucije:
· Narava drog- manjša kot je velikost molekule in bolj lipofilno zdravilo, hitrejša in bolj enakomerna je njegova porazdelitev.
· Velikost organa- večji kot je organ, več zdravila lahko vstopi vanj pomembna sprememba koncentracijski gradient
· Pretok krvi v organ- v dobro prekrvljenih tkivih (možgani, srce, ledvice) se terapevtska koncentracija snovi ustvari veliko prej kot v slabo prekrvljenih tkivih (maščobno, kostno)
· Prisotnost histohematogenih ovir- zdravila zlahka prodrejo v tkiva s slabo izraženim GHB
· Vezava na plazemske beljakovine- večja kot je vezana frakcija zdravila, slabša je njegova porazdelitev v tkivu, saj lahko kapilaro zapustijo samo proste molekule.
· Odlaganje zdravila v tkivih- vezava zdravil na tkivne beljakovine prispeva k njihovemu kopičenju v njih, saj se koncentracija prostih zdravil v perivaskularnem prostoru zmanjša in se nenehno ohranja visok koncentracijski gradient med krvjo in tkivi.
Kvantitativna značilnost porazdelitve zdravila je navidezni volumen porazdelitve (Vd).
Navidezni obseg porazdelitveVd Je hipotetični volumen tekočine, v katerega se lahko porazdeli celoten dani odmerek zdravila, da se ustvari koncentracija, ki je enaka koncentraciji v krvni plazmi.
Vd je enak razmerju med uporabljenim odmerkom (skupna količina zdravila v telesu) in njegovo koncentracijo v krvni plazmi:
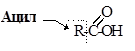 .
.
Večji kot je navidezni volumen porazdelitve, več zdravil se porazdeli v tkivo.
12. Konstanta izločanja, njeno bistvo, dimenzija, razmerje z drugimi farmakokinetičnimi parametri.
Konstanta hitrosti izločanja(kel, min-1) - prikazuje, kateri del zdravil se izloči iz telesa na enoto časa Þ Kel = Avid / Atot, kjer je Avid količina izločenih zdravil v enotah. čas, general - skupaj Droge v telesu.
Vrednost kel običajno najdemo z reševanjem farmakokinetične enačbe, ki opisuje proces izločanja zdravila iz krvi; zato se kel imenuje modelni kinetični indeks. Kel ni neposredno povezan z načrtovanjem režima odmerjanja, vendar se njegova vrednost uporablja za izračun drugih farmakokinetičnih parametrov.
Konstanta izločanja je neposredno sorazmerna z očistkom in obratno sorazmerna z volumnom porazdelitve (iz definicije očistka): Kel = CL / Vd; = ura-1 / min-1 = frakcija na uro.
13. Razpolovna doba zdravil, njegovo bistvo, razsežnost, razmerje z drugimi farmakokinetičnimi parametri.
Obdobje polovice izločanja(t½, min) je čas, potreben za zmanjšanje koncentracije zdravil v krvi za natanko polovico. V tem primeru ni pomembno, na kakšen način se doseže znižanje koncentracije – s pomočjo biotransformacije, izločanja ali zaradi kombinacije obeh procesov.
Razpolovni čas je določen s formulo:
![]()
Razpolovna doba je najpomembnejši farmakokinetični parameter, ki omogoča:
B) določite čas popolnega izločanja zdravila
C) kadar koli napovedati koncentracijo zdravil (za zdravila s kinetiko prvega reda)
14. Očistek kot glavni farmakokinetični parameter za upravljanje režima odmerjanja. Njegovo bistvo, razsežnost in razmerje z drugimi farmakokinetičnimi parametri.
Odstopanje(Cl, ml / min) - volumen krvi, ki se očisti iz zdravil na enoto časa.
Ker je plazma (kri) "vidni" del volumna porazdelitve, je očistek delež volumna porazdelitve, iz katerega se zdravilo sprosti na enoto časa. Če označimo celotno količino zdravila v telesu skozi General, in znesek, ki je bil dodeljen po tem Avyd, potem:
![]() Po drugi strani pa iz definicije volumna porazdelitve izhaja, da je skupna količina zdravila v telesu Absh =Vd´
CTer / plazma... Če to vrednost nadomestimo v formulo za odmik, dobimo:
Po drugi strani pa iz definicije volumna porazdelitve izhaja, da je skupna količina zdravila v telesu Absh =Vd´
CTer / plazma... Če to vrednost nadomestimo v formulo za odmik, dobimo:
![]() .
.
Tako je očistek razmerje med hitrostjo izločanja zdravila in njegovo koncentracijo v krvni plazmi.
V tej obliki se formula očistka uporablja za izračun vzdrževalnega odmerka zdravila ( DP), to je odmerek zdravila, ki bi moral nadomestiti izgubo zdravila in vzdrževati njegovo raven na konstantni ravni:
Hitrost injiciranja = Hitrost izločanja =Cl´ CTer(odmerek/min)
DP= hitrost vbrizgavanja´ T (T- interval med jemanjem zdravila)
Odmik od tal je dodatek, torej izločanje snovi iz telesa lahko poteka s sodelovanjem procesov v ledvicah, pljučih, jetrih in drugih organih: Clsystem = Clrenal. + Cl jetra + Cld.
Dovoljenje je vezano Z razpolovno dobo zdravila in volumnom porazdelitve: t1 / 2 = 0,7 * Vd / Cl.
15. Odmerek. Vrste odmerkov. Odmerne enote zdravila. Cilji odmerjanja zdravil, metode in možnosti dajanja, interval dajanja.
Učinek zdravil na telo je v veliki meri odvisen od njihovega odmerka.
Odmerek- količina snovi, ki se naenkrat vnese v telo; izraženo v teži, prostornini ali konvencionalnih (bioloških) enotah.
Vrste odmerkov:
A) enkratni odmerek - količina snovi na odmerek
B) dnevni odmerek - količina zdravila, predpisana za dan v enem ali več odmerkih
C) tečajni odmerek - skupna količina zdravila za potek zdravljenja
D) terapevtski odmerki - odmerki, v katerih se zdravilo uporablja v terapevtske ali profilaktične namene (prag ali minimalni učinkovit, povprečni terapevtski in višji terapevtski odmerki).
E) toksični in smrtonosni odmerki - odmerki zdravil, pri katerih začnejo imeti izrazite toksične učinke ali povzročijo smrt telesa.
E) polnilni (uvodni) odmerek - število injiciranih zdravil, ki zapolni celoten volumen porazdelitve telesa v efektivni (terapevtski) koncentraciji: VD = (Css * Vd) / F
G) vzdrževalni odmerek - sistematično uporabljena količina zdravil, ki nadomesti izgubo zdravil z očistkom: PD = (Css * Cl * DT) / F
Farmacevtske dozirne enote:
1) v gramih ali frakcijah grama zdravil
2) število zdravil na 1 kg telesna teža (na primer 1 Mg/kg) ali na enoto površine telesa (na primer 1 Mg / m2)
Cilji odmerjanja zdravil:
1) določi količino zdravil, ki je potrebna, da se doseže želeni terapevtski učinek z določenim trajanjem
2) preprečiti pojav zastrupitve in stranskih učinkov z uvedbo zdravil
Metode dajanja zdravila: 1) enteralno 2) parenteralno (glejte poglavje 5)
Možnosti dajanja zdravil:
A) kontinuirano (z dolgotrajno intravaskularno infuzijo zdravil po kapljicah ali prek avtomatskih razpršilnikov). Z neprekinjenim dajanjem zdravil se njegova koncentracija v telesu gladko spreminja in ne doživlja bistvenih nihanj.
B) intermitentno dajanje (z injekcijskimi ali neinjekcijskimi metodami) - dajanje zdravila v rednih časovnih presledkih (intervali odmerjanja). Z občasnim dajanjem zdravil njegova koncentracija v telesu nenehno niha. Po zaužitju določenega odmerka se najprej dvigne, nato pa postopoma zmanjšuje in doseže minimalne vrednosti pred naslednjim dajanjem zdravila. Nihanja v koncentraciji so pomembnejša, večji kot je uporabljeni odmerek zdravila in interval med injekcijami.
Interval vbrizgavanja- interval med danimi odmerki, ki zagotavlja vzdrževanje terapevtske koncentracije snovi v krvi.
16. Dajanje zdravil s konstantno hitrostjo. Kinetika koncentracije zdravila v krvi. Stacionarna koncentracija zdravila v krvi ( Css), čas njegovega doseganja, izračun in upravljanje z njim.
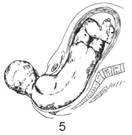 Posebnost vnosa zdravil s konstantno hitrostjo je gladka sprememba njegove koncentracije v krvi ob dajanju, medtem ko:
Posebnost vnosa zdravil s konstantno hitrostjo je gladka sprememba njegove koncentracije v krvi ob dajanju, medtem ko:
1) čas za dosego koncentracije zdravila v stanju dinamičnega ravnovesja je 4-5 t½ in ni odvisen od hitrosti infuzije (velikosti danega odmerka)
2) s povečanjem hitrosti infundiranja (vbrizganega odmerka) se sorazmerno krat poveča tudi vrednost CSS
3) izločanje zdravila iz telesa po koncu infuzije traja 4-5 t½.
ZSs- ravnotežna stacionarna koncentracija- koncentracija zdravil, dosežena pri hitrosti dajanja, ki je enaka hitrosti izločanja, torej:
![]() (iz definicije razmika)
(iz definicije razmika)
Za vsako naslednjo razpolovno dobo se koncentracija zdravila poveča za polovico preostale koncentracije. Vsa zdravila, ki izpolnjujejo zakon o izločitvi prvega reda, so Bo doseglaCsspo 4-5 razpolovnih časih.
Pristopi upravljanja na ravni CSs: spremenite odmerek zdravila ali interval vnosa
17. Občasno dajanje zdravil. Kinetika koncentracije zdravila v krvi, terapevtsko in toksično območje koncentracij. Izračun stacionarne koncentracije ( CSs), meje njegovih nihanj in nadzor. Ustrezen diskretni interval odmerjanja.
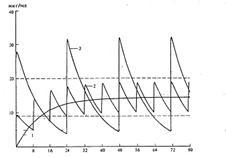 Nihanja koncentracije zdravil v krvni plazmi: 1 - s stalnim intravenskim kapljanjem; 2 - z delno uvedbo enakega dnevnega odmerka z intervalom 8 ur; 3 - z uvedbo dnevnega odmerka v intervalu 24 ur.
Nihanja koncentracije zdravil v krvni plazmi: 1 - s stalnim intravenskim kapljanjem; 2 - z delno uvedbo enakega dnevnega odmerka z intervalom 8 ur; 3 - z uvedbo dnevnega odmerka v intervalu 24 ur.
Intermitentno dajanje zdravil- dajanje določene količine zdravil v intervalih.
Ravnotežna koncentracija v stanju dinamičnega ravnovesja je dosežena po 4-5 obdobjih polovične izločanja, čas njenega doseganja ni odvisen od odmerka (na začetku, ko je koncentracija zdravila nizka, je nizka tudi hitrost njegovega izločanja; ko se količina snovi v telesu poveča, se poveča tudi hitrost njenega izločanja, zato bo zgodaj ali pozno prišel trenutek, ko bo povečana hitrost izločanja uravnotežila dani odmerek zdravila in se bo nadaljnje povečevanje koncentracije ustavilo)
Css je neposredno sorazmeren z odmerkom zdravila in obratno sorazmeren z intervalom injiciranja in očistkom zdravila.
Css Swing Meje: ![]() ; Cssmin = Cssmax × (1 - e-pošta). Nihanja koncentracije zdravila so sorazmerna s T / t1 / 2.
; Cssmin = Cssmax × (1 - e-pošta). Nihanja koncentracije zdravila so sorazmerna s T / t1 / 2.
Terapevtski obseg (varnostni hodnik, terapevtsko okno) Ali je območje koncentracije od minimalne terapevtske do povzroča videz prvi znaki neželenih učinkov.
Toksičen obseg- razpon koncentracije od najvišje terapevtske do smrtonosne.
Ustrezno dajanje diskretnih odmerkov: način dajanja, pri katerem nihanje koncentracije zdravila v krvi spada v terapevtsko območje. Za določitev ustreznega režima dajanja zdravila je treba izračunati. Razlika med Cssmax in Cssmin ne sme presegati 2Css.
Nadzor nihanjaCss:
Razpon nihanjaCssneposredno sorazmerna z odmerkom zdravila in obratno sorazmerna z intervalom njegove uporabe.
1. Spremenite odmerek zdravil: s povečanjem odmerka zdravila se razpon nihanj njegovega Css sorazmerno poveča
2. Spremenite interval dajanja zdravila: s povečanjem intervala dajanja zdravila se razpon nihanj njegovega Css sorazmerno zmanjša
3. Hkrati spremenite odmerek in interval dajanja
18. Uvodni (polnilni) odmerek. Terapevtski pomen, izračun po farmakokinetičnih parametrih, pogoji in omejitve uporabe.
Uvodni (polnilni) odmerek- enkratni odmerek, ki zapolni celoten volumen porazdelitve v trenutni terapevtski koncentraciji. VD = (Css * Vd) / F; = mg / l, = l / kg
Terapevtski pomen: začetni odmerek hitro zagotavlja učinkovito terapevtsko koncentracijo zdravil v krvi, kar omogoča, na primer, hitro zaustavitev napada astme, aritmij itd.
Uvodni odmerek se lahko daje naenkrat le, ko Proces distribucije snovi je prezrt
Omejitev uporabe VD: če se zdravilo distribuira Bistveno počasnejši od vstopa v krvni obtok, bo uvedba celotnega polnilnega odmerka naenkrat (zlasti intravensko) ustvarila koncentracijo, ki je bistveno višja od terapevtske, in bo povzročila pojav toksičnih učinkov. VD stanje uporabe: torej uvedba obremenilnih odmerkov Vedno naj bo počasen ali delno.
19. Vzdrževalne doze, njihov terapevtski pomen in izračun optimalnega režima odmerjanja.
Vzdrževalni odmerek- odmerek zdravila, ki se daje sistematično, ki zapolni volumen očistka, to je fragment Vd, ki se v intervalu DT očisti od zdravil: PD = (Css * Cl * DT) / F.
Terapevtski pomen: PD kompenzira izgube z očistkom v intervalu med injekcijami zdravila.
Izračun optimalnega odmerka zdravil (za hitro lajšanje napada):
1. Izračunaj VD: VD = (Css * Vd) / F
2. Izberite interval injiciranja DT (običajno je večina zdravil predpisana z intervalom blizu t1 / 2) in izračunajte AP: AP = (Css * Cl * DT) / F
3. Preverite, ali nihanja zdravila v krvi presegajo terapevtsko območje z izračunom Cssmax in Cssmin: ![]() ; Cssmin = Cssmax × (1 - e-pošta). Razlika med Cssmax in Cssmin ne sme presegati dveh Css.
; Cssmin = Cssmax × (1 - e-pošta). Razlika med Cssmax in Cssmin ne sme presegati dveh Css.
Frakcijo, ki jo je treba izločiti, najdemo v skladu z grafom (glej razdelek 16) ali po formuli: ![]()
4. Če v intervalu dajanja zdravila, ki smo ga izbrali, njegova nihanja presegajo terapevtsko območje, spremenimo DT in ponovimo izračun (točka 2 - točka 4)
Opomba! Če zdravilo ni namenjeno za lajšanje nujnih stanj ali se jemlje v tabletah, se VD ne izračuna.
20. Posamezne, starostne in spolne razlike v farmakokinetiki zdravil. Popravki za izračun posameznih vrednosti za volumen porazdelitve zdravil.
1. Starostne razlike v farmakokinetiki zdravil.
|
1. Rožena plast je tanjša, zato se zdravila pri nanosu na kožo bolje absorbirajo. Boljša je tudi absorpcija zdravil pri rektalni aplikaciji. 2. Količina tekočine v telesu otrok je 70-80 %, pri odraslih pa le »60 %, zato je Vd hidrofilnih zdravil, ki jih imajo, višji in so potrebni višji odmerki. 3. Pri novorojenčku je raven albumina v plazmi nižja kot pri odraslih, zato je vezava zdravil na beljakovine pri njih manj intenzivna. 4. Novorojenčki imajo nizko intenzivnost sistemov citokroma P450 in konjugacijskih encimov, vendar visoko aktivnost metilacijskih sistemov. 5. Stopnja glomerularne filtracije v ledvicah otrok, mlajših od 6 mesecev, je 30-40 % stopnje pri odraslih, zato se ledvično izločanje zdravil zmanjša. |
1. Prišlo je do zmanjšanja koncentracije albumina v krvni plazmi in deleža zdravila, povezanega z beljakovinami 2. Vsebnost vode v telesu se zmanjša s 60% na 45%, zato se kopičenje lipofilnih zdravil poveča. 3. Stopnja glomerularne filtracije lahko pade do 50-60 % stopnje zrelega bolnika, zato je izločanje zdravil preko ledvic močno omejeno. |
2. Spolne razlike v delovanju zdravil... Za ženske je značilna manjša telesna teža kot za moške, zato bi morala biti velikost odmerkov zdravila zanje praviloma na spodnji meji razpona terapevtskih odmerkov.
3. Patološka stanja telesa in učinek zdravil
A) bolezni jeter: F zdravila zaradi zaustavitve presnove pri prvem prehodu, del nevezanih zdravil zaradi pomanjkanja sinteze albuminov, učinki zdravil so podaljšani zaradi njihove biotransformacije.
B) patologija ledvic: izločanje zdravil, ki se izločajo skozi ledvice, se upočasni
4. Genetski dejavniki- pomanjkanje določenih encimov presnove zdravil lahko prispeva k podaljšanju njihovega delovanja (psevdoholinesteraza itd.)
Popravki za izračun posameznih vrednosti volumna porazdelitve zdravil:
A) pri debelosti so lipofobna zdravila netopna v maščobnem tkivu Þ je treba izračunati idealna teža po višini (Brocina formula: idealna teža = višina (v cm) - 100) in preračunaj Vd glede na idealno težo glede na višino.
B) v primeru edema morate izračunati presežek volumna vode = odvečna teža - idealno, Vd je treba povečati za liter vsakega odvečnega kilograma vode.
Odvisnost glavnih farmakokinetičnih parametrov od različnih dejavnikov:
1. Absorpcija zdravil: v starosti ¯ absorpcija zdravila, njegova presnova med predsistemskim izločanjem, biološka uporabnost zdravil se spremeni.
2. Volumen porazdelitve Vd: ¯ s starostjo in z debelostjo, z edemom
3. Razpolovna doba: spremembe s starostjo in debelostjo (saj se Vd zmanjša)
4. Očistek: določen s funkcionalnim stanjem ledvic in jeter
21. Ledvični očistek zdravil, mehanizmi, njihove kvantitativne in kvalitativne značilnosti.
Ledvični očistek je merilo volumna krvne plazme, ki jo ledvice na enoto časa očistijo od zdravila iz zdravila: Cl (ml / min) = U × V / P, kjer je U koncentracija zdravil v ml urina, V je prostornina izločenega urina v min in P = koncentracija zdravila v ml plazme.
Mehanizmi ledvičnega očistka in njihove značilnosti:
1. Filtracija: Izpuščajo se droge Samo filtriranje(inzulin) bo imel očistek enak GFR (125-130 ml / min)
Določajo: ledvični pretok krvi, nevezana frakcija zdravila in filtrirna zmogljivost ledvic.
Večina zdravil ima nizko molekulsko maso in se zato prosto filtrira iz plazme v glomerulu.
2. Aktivno izločanje: Izpuščajo se droge Filtracija in popolno izločanje(paraaminogipurna kislina), bo imel očistek enak ledvičnemu plazemskemu očistku (650 ml/min)
Ledvični tubul vsebuje dva transportna sistema ki lahko loči zdravila v ultrafiltrat, enega za organske kisline in drugo za organske baze. Ti sistemi potrebujejo energijo za aktivni transport proti gradientu koncentracije; so mesto tekmovanja za nosilca enih zdravil z drugimi.
Določeno z: največjo hitrostjo izločanja, količino urina
3. Reabsorpcija: vrednosti očistka med 130 in 650 ml/min kažejo, da je zdravilo Filtriran, izločen in delno reabsorbiran
Reabsorpcija poteka po celotnem ledvičnem kanalu in je odvisna od polarnosti zdravila, nepolarni, lipofilni se reabsorbirajo.
Določeno z: primarno vrednostjo pH in ionizacijo zdravila
Številni kazalniki kot npr Starost, skupna uporaba več zdravil, bolezni pomembno vplivajo na ledvični očistek:
A) ledvična odpoved ® zmanjšanje očistka zdravila visoka stopnja Droge v krvi
B) glomerulonefritis ® izguba serumske beljakovine, ki je bila običajno na voljo in povezana z zdravili ® povečanje ravni proste frakcije zdravil v plazmi
22. Dejavniki, ki vplivajo na ledvični očistek zdravil. Odvisnost očistka od fizikalno-kemijskih lastnosti zdravil.
Dejavniki, ki vplivajo na ledviceCl:
A) glomerularna filtracija
B) hitrost ledvičnega krvnega pretoka
B) največja hitrost izločanja
D) volumen urina
E) frakcija, nevezana v krvi
Odvisnost ledvičnega očistka od fizikalno-kemijskih lastnosti zdravil:
Splošni vzorci: 1) polarna zdravila se ne absorbirajo, nepolarna zdravila se reabsorbirajo 2) ionska zdravila se izločajo, neionska zdravila se ne izločajo.
I. Nepolarne neionske snovi: filtrirane samo v nevezanih oblikah, se ne izločajo, reabsorbirajo
Ledvični očistek je majhen in je določen z: a) deležem nevezanih zdravil v krvi b) volumnom urina
II. Polarne neionske snovi: filtrirane v nevezani obliki, ne izločajo, ne reabsorbirajo
Ledvični očistek je visok, kar določa: a) delež nevezanih zdravil v krvi b) hitrost glomerularne filtracije
III. Nepolarno ionizirano v urinu v neionski obliki: filtrirano, aktivno izločeno, nepolarno reabsorbirano
Ledvični očistek določa: a) delež nevezanih zdravil v krvi b) delež ioniziranih zdravil v urinu c) volumen urina
IV. Polarna ionizirana v urinu v neionizirani obliki: filtrirana, aktivno izločena, ne reabsorbirana
Ledvični očistek je določen z: a) ledvičnim pretokom krvi in hitrostjo glomerulne filtracije b) največjo hitrostjo izločanja
23. Jetrni očistek zdravil, njegove determinante in omejitve. Enterohepatični cikel zdravil.
Mehanizmi jetrnega očistka:
1) presnova (biotransformacija) z oksidacijo, redukcijo, alkilacijo, hidrolizo, konjugacijo itd.
Glavna strategija presnove ksenobiotikov: nepolarne snovi ® polarni (hidrofilni) presnovki, izločeni z urinom.
2) izločanje (izločanje netransformiranih snovi v žolč)
V žolč se prenašajo samo polarne snovi z molekulsko maso > 250 (organske kisline, baze).
Determinatorji jetrnega očistka:
A) Hitrost pretoka krvi v jetrih
B) Največja hitrost izločanja ali presnovne transformacije
B) Km - Michaelisova konstanta
D) Frakcija, ki ni vezana na beljakovine
Omejitve jetrnega očistka:
1. Če je Vmax / Km velik → Cl pecs = hitrost krvnega pretoka v jetrih
2. Če je Vmax / Km srednje vrednosti → Cl = vsota vseh faktorjev
3. Če je Vmax / Km majhen → Cl peč je majhna, omejena
Enterohepatični cikel zdravil -Številna zdravila in produkti njihovega preoblikovanja se v znatnih količinah izločajo z žolčem v črevesje, od koder se delno izločajo z iztrebki, delno pa - Reabsorbira se v kri, ponovno vstopi v jetra in se izloči v črevesje.
Izločanje zdravil iz jeter je lahko bistveno spremenjeno Bolezen jeter, starost, prehrana, genetika, trajanje predpisovanja zdravil(na primer zaradi indukcije jetrnih encimov) in drugih dejavnikov.
24. Dejavniki, ki spreminjajo očistek zdravilnih učinkovin.
1. Interakcije z zdravili na ravni: ledvično izločanje, biokemična transformacija, pojavi encimske indukcije
2. Bolezen ledvic: motnje krvnega obtoka, akutna in kronična okvara ledvic, izidi dolgotrajne ledvične bolezni
3. Bolezni jeter: alkoholna ciroza, primarna ciroza, hepatitis, hepatomi
4. Bolezni prebavil in endokrinih organov
5. Individualna intoleranca (pomanjkanje acetilacijskih encimov - intoleranca na aspirin)
25. Korekcija zdravljenja z zdravili za bolezni jeter in ledvic. Splošni pristopi. Popravek režima odmerjanja pod nadzorom celotnega očistka zdravila.
1. Prekličite zdravila, ki niso potrebna
2. Pri boleznih ledvic uporabljajte zdravila, ki se izločajo v jetrih in obratno.
3. Zmanjšajte odmerek ali povečajte interval med injekcijami
4. Natančno spremljanje stranskih učinkov in toksičnih učinkov
5. Če farmakološkega učinka ni, je treba odmerek povečevati počasi in pod nadzorom farmakoloških in toksičnih učinkov.
6. Če je mogoče, določite koncentracijo snovi v plazmi in individualno popravite terapijo z zdravilom Cl
7. Uporabite posredno metodo ocenjevanja Cl.
Popravek režima odmerjanja pod nadzorom celotnega očistka zdravila:
Prilagoditev odmerka : Dind = Dtyp. × Clind. / Cltyp.
Pri neprekinjenem intravenskem dajanju zdravila: individualna hitrost dajanja = tipična hitrost dajanja × Cl ind. / Cl tipično
Pri intermitentnem dajanju: 1) spremenite odmerek 2) spremenite interval 3) spremenite oba parametra. Na primer, če se očistek zmanjša za 50 %, lahko zmanjšate odmerek za 50 % in obdržite interval ali podvojite interval in obdržite odmerek. Zaželeno je zmanjšati odmerek in vzdrževati interval vnosa.
26. Popravek režima odmerjanja pod nadzorom preostale ledvične funkcije.
Očistek kreatinina- najpomembnejši kvantitativni kazalnik delovanja ledvic, na podlagi katerega je mogoče prilagoditi režim odmerjanja
Vemo:
A) preostala ledvična funkcija, določena z očistkom kreatinina pri danem bolniku Clcr/bolnik
B) skupni očistek danega zdravila (CLP/skupni) in delež ledvičnega očistka zdravila v celotnem očistku
B) normalen očistek kreatinina Clcr / normogram
3) Css in F za ta LAN (iz reference)
Najti: odmerek zdravila za tega bolnika
ClPP / ledvična stopnja = ClPP / skupni X delež ledvičnega očistka zdravila v celotnem očistku
Сlp / ledvični bolnik = Clcr / pacient / Сlcr / norma * Clls / ledvična norma
ClPP / neledvična stopnja = ClPP / skupna - ClPP / ledvična stopnja
ClPS / splošni bolnik = CLPS / ledvični bolnik + ClPS / neledvična norma
Odmerek tega zdravila v notranjosti z normalnim delovanjem ledvic je: norma PD = Css X Cl / F
Notranji odmerek tega zdravila za našega bolnika je enak: PD bolnika = norma PD X СlPS / splošni bolnik / СlPS / skupaj
Odgovori: PDbolny
27. Korekcija zdravljenja z zdravili za poškodbe jeter in druga patološka stanja.
Bolezen jeter lahko zmanjša očistek in podaljša razpolovno dobo številnih zdravil. Vendar pa se pri nekaterih zdravilih, ki jih izločajo jetra, ti parametri ne spremenijo v primeru okvare jeter, zato Bolezen jeter ne vpliva vedno na intrinzični jetrni očistek... Trenutno ni zanesljivega markerja, s katerim bi lahko napovedali jetrni očistek, podoben očistku kreatinina.
Popravek režima odmerjanja pri bolezni ledvic, glej odstavek 26 zgoraj, splošna načela popravek - v.25.
28. Strategija individualne terapije z zdravili.
Prepoznavanje pomembne vloge koncentracije kot povezave med farmakokinetiko in farmakodinamiko prispeva k oblikovanju strategije ciljne koncentracije – optimizirati odmerek pri danem bolniku na podlagi merjenja koncentracije zdravila. Sestavljen je iz naslednjih stopenj:
1. Izbira ciljne koncentracije
2. Izračunajte Vd in Cl na podlagi tipičnih vrednosti in prilagodite dejavnike, kot sta telesna teža in delovanje ledvic.
3. Vnos polnilnega ali vzdrževalnega odmerka, izračunanega ob upoštevanju vrednosti TC, Vd in Cl.
4. Registracija bolnikove reakcije in določanje koncentracije zdravila
5. Revizija Vd in Cl na podlagi rezultatov meritev koncentracij.
6. Ponovite korake 3-6, da prilagodite vzdrževalni odmerek, potreben za optimalen odziv na zdravilo.
29. Biotransformacija zdravil, njen biološki pomen, glavna usmeritev in vpliv na delovanje zdravil. Glavne faze presnovnih transformacij zdravil v telesu.
Biotransformacija zdravil- kemične transformacije zdravil v telesu.
Biološki pomen biotransformacije zdravil: ustvarjanje substrata, ki je primeren za naknadno odstranjevanje (kot energijski ali plastični material) ali pri pospeševanju izločanja zdravil iz telesa.
Glavna smer presnovnih transformacij zdravil: nepolarna zdravila → polarni (hidrofilni) presnovki, izločeni z urinom.
Obstajata dve fazi presnovnih reakcij zdravil:
1) Metabolična transformacija (nesintetične reakcije, faza 1)- transformacija snovi zaradi mikrosomske in ekstramikrosomske oksidacije, redukcije in hidrolize
2) konjugacija (sintetične reakcije, faza 2)- biosintetični proces, ki ga spremlja dodajanje številnih kemičnih skupin ali molekul endogenih spojin zdravilu ali njegovim metabolitom z a) tvorbo glukuronidov b) glicerolnimi estri c) sulfoestri d) acetilacijo e) metilacijo
Učinek biotransformacije na farmakološko aktivnost zdravil:
1) najpogosteje metaboliti biotransformacije nimajo farmakološke aktivnosti ali pa je njihova aktivnost zmanjšana v primerjavi z začetno snovjo
2) v nekaterih primerih lahko presnovki ohranijo aktivnost in celo presežejo aktivnost matične snovi (kodein se presnovi v bolj farmakološko aktivni morfin)
3) včasih med biotransformacijo nastanejo strupene snovi (metaboliti izoniazida, lidokaina)
4) včasih med biotransformacijo nastanejo presnovki z nasprotnimi farmakološkimi lastnostmi (presnovki neselektivnih agonistov b2-adrenergičnih receptorjev imajo lastnosti blokatorjev teh receptorjev)
5) številne snovi so predzdravila, ki sprva ne dajejo farmakoloških učinkov, vendar se med biotransformacijo pretvorijo v biološko aktivne snovi (neaktivna L-dopa, ki prodre v BBB, se v možganih spremeni v aktivni dopamin, medtem ko obstajajo ni sistemskih učinkov dopamina).
30. Klinični pomen biotransformacije zdravil. Vpliv spola, starosti, telesne teže, okoljskih dejavnikov, kajenja, alkohola na biotransformacijo zdravil.
Klinični pomen biotransformacije zdravil: ker se lahko odmerek in pogostost dajanja, potrebni za doseganje učinkovite koncentracije v krvi in tkivih, pri bolnikih razlikujeta zaradi individualnih razlik v porazdelitvi, hitrosti presnove in izločanja zdravil, je pomembno, da jih upoštevamo v klinični praksi.
Vpliv različnih dejavnikov na biotransformacijo zdravil:
A) Funkcionalno stanje jeter: v primeru njenih bolezni se očistek zdravil običajno zmanjša, razpolovna doba izločanja pa se poveča.
B) Vpliv okoljskih dejavnikov: kajenje spodbuja indukcijo citokroma P450, zaradi česar se presnova zdravil med mikrosomsko oksidacijo pospeši
V) Vegetarijanci biotransformacija zdravil se upočasni
D) za starejše in mlade bolnike je značilna preobčutljivost na farmakološke ali toksične učinke zdravil (pri starejših in otrocih, mlajših od 6 mesecev, se zmanjša aktivnost mikrosomske oksidacije)
E) pri moških je presnova nekaterih zdravil hitrejša kot pri ženskah, saj androgeni spodbujajo sintezo mikrosomskih jetrnih encimov (etanola)
E) Visoka vsebina beljakovin v hrani in intenzivne telesne dejavnosti: pospeševanje presnove zdravil.
F) Alkohol in debelost upočasni presnovo zdravil
31. Metabolične interakcije z zdravili. Bolezni, ki vplivajo na njihovo biotransformacijo.
Metabolična interakcija zdravil:
1) indukcija encimov presnove zdravil - absolutno povečanje njihovega števila in aktivnosti zaradi izpostavljenosti nekaterim zdravilom. Indukcija vodi do pospeševanja presnove zdravil in (praviloma, vendar ne vedno) do zmanjšanja njihove farmakološke aktivnosti (rifampicin, barbiturati - induktorji citokroma P450)
2) zaviranje encimov presnove zdravil - zaviranje aktivnosti presnovnih encimov pod vplivom nekaterih ksenobiotikov:
A) kompetitivna presnovna interakcija - zdravila z visoko afiniteto za določene encime zmanjšajo presnovo zdravil z nižjo afiniteto za te encime (verapamil)
B) vezava na gen, ki inducira sintezo nekaterih izoencimov citokroma P450 (cimedin)
C) neposredna inaktivacija izoencimov citokroma P450 (flavonoidi)
Bolezni, ki vplivajo na presnovo zdravil:
A) bolezen ledvic (okvarjen ledvični pretok krvi, akutna in kronična ledvična bolezen, izidi dolgotrajne ledvične bolezni)
B) bolezni jeter (primarna in alkoholna ciroza, hepatitis, hepatom)
C) bolezni prebavil in endokrinih organov
C) individualna intoleranca na nekatera zdravila (pomanjkanje acetilacijskih encimov - intoleranca na aspirin)
32. Načini in mehanizmi izločanja zdravil iz telesa. Možnosti nadzora izločanja zdravil.
Načini in mehanizmi izločanja zdravila: izločanje zdravil z jetri in ledvicami ter nekaterimi drugimi organi:
A) preko ledvic s filtracijo, izločanjem, reabsorpcijo
B) jetra z biotransformacijo, izločanje z žolčem
C) skozi pljuča, slino, znoj, mleko itd. z izločanjem, izhlapevanjem
Možnosti za vodenje procesov odvzema drog:
1. nadzor pH: v alkalnem urinu se poveča izločanje kislih spojin, v kislem urinu izločanje bazičnih spojin
2.uporaba holeretičnih zdravil (holenzim, alohol)
3.hemodializa, peritonealna dializa, hemosorpcija, limfosorpcija
4. Prisilna diureza (IV NaCl ali glukoza za obremenitev z vodo + furosemid ali manitol)
5.izpiranje želodca, uporaba klistirjev
33. Pojem receptorjev v farmakologiji, molekularna narava receptorjev, signalni mehanizmi delovanja zdravil (vrste transmembranske signalizacije in sekundarni mediatorji).
Receptorji - Molekularne komponente celice ali organizma, ki medsebojno delujejo z zdravili in povzročajo številne biokemične dogodke, ki vodijo do razvoja farmakološkega učinka.
Koncept receptorjev v farmakologiji:
1. Receptorji določajo kvantitativne vzorce delovanja zdravila
2. Receptorji so odgovorni za selektivnost delovanja zdravila
3. Receptorji posredujejo delovanje farmakoloških antagonistov
Koncept receptorjev je osnova za ciljno uporabo zdravil, ki vplivajo na regulacijske, biokemične procese in komunikacijo.
Molekularna narava receptorjev:
1.regulacijski proteini, mediatorji delovanja različnih kemičnih signalov: nevrotransmiterji, hormoni, avtokoidi
2.encimi in transmembranski nosilci beljakovin (Na +, K + ATPaza)
3.strukturne beljakovine (tubulin, citoskeletni proteini, celična površina)
4.jedrske beljakovine in nukleinske kisline
Signalni mehanizmi delovanja zdravila:
1) prodiranje ligandov, topnih v lipidih, skozi membrano in njihov učinek na znotrajcelične receptorje.
2) signalna molekula se veže na zunajcelično domeno transmembranskega proteina in aktivira encimsko aktivnost njegove citoplazemske domene.
3) signalna molekula se veže na ionski kanal in uravnava njegovo odpiranje.
4) signalna molekula se veže na receptor na celični površini, ki je preko G-proteina vezan na efektorski encim. G-protein aktivira sekundarni sel.
Vrste transmembranske signalizacije:
A) prek receptorjev 1-TMS z aktivnostjo tirozin kinaze in brez nje
B) prek receptorjev 7-TMS, povezanih z G-proteinom
B) skozi ionske kanale (odvisni od liganda, napetostno odvisni, kontakti z vrzeljo)
Sekundarni posredniki: cAMP, Ca2 + ioni, DAG, IF3.
34. Fizikalno-kemijski in kemijski mehanizmi delovanja zdravilnih učinkovin.
A) Fizikalno-kemijska interakcija z biosubstratom- neelektrolitsko delovanje.
Glavni farmakološki učinki: 1) narkotični 2) splošni depresivni 3) paralizirajoči 4) lokalno dražeč 5) membranolitično delovanje.
Kemična narava snovi: kemično inertni ogljikovodiki, etri, alkoholi, aldehidi, barbiturati, plinske droge
Mehanizem delovanja je reverzibilno uničenje membran.
B) kemični(molekularno-biokemijski) mehanizem delovanja zdravil.
Glavne vrste kemične interakcije z biosubstratom:
- Šibke (nekovalentne, reverzibilne interakcije) (vodikove, ionske, monodipolne, hidrofobne).
- Kovalentne vezi (alkilacija).
Pomen nekovalentnih interakcij zdravil: delovanje je nespecifično, ni odvisno od kemične strukture snovi.
Pomen kovalentnih interakcij zdravil: delovanje je specifično, kritično odvisno od kemične strukture, uresničuje se z delovanjem na receptorje.
35. Izrazi in pojmi kvantitativne farmakologije: učinek, učinkovitost, aktivnost, agonist (polni, delni), antagonist. Klinična razlika med konceptoma delovanja in učinkovitosti zdravil.
 Učinek (odziv)- kvantitativni izkoristek reakcije interakcije celice, organa, sistema ali organizma s farmakološkim sredstvom.
Učinek (odziv)- kvantitativni izkoristek reakcije interakcije celice, organa, sistema ali organizma s farmakološkim sredstvom.
Učinkovitost- merilo reakcije vzdolž osi učinka - velikost odziva biološkega sistema na farmakološki učinek; To je sposobnost zdravil, da zagotovijo največji možni učinek.... To je pravzaprav največja velikost učinka, ki jo je mogoče doseči z uvedbo danega zdravila. Številčno označeno z vrednostjo Emax. Višji kot je Emax, večja je učinkovitost zdravila.
dejavnost- merilo občutljivosti na zdravila vzdolž koncentracijske osi, označuje afiniteto (afiniteto liganda do receptorja), kaže, kakšen odmerek (koncentracija) zdravila lahko povzroči razvoj standardnega učinka, ki je enak 50 % največje možno za to zdravilo. Številčno označeno z vrednostjo EC50 ali ED50. Večja kot je aktivnost zdravila, manjši je odmerek potreben za reprodukcijo terapevtskega učinka.
Učinkovitost: 1 = 2 > 3
Dejavnost: 1> 3> 2
Pri klinični dejavnosti je bolj pomembno poznavanje učinkovitosti kot aktivnosti, saj nas bolj zanima sposobnost zdravil, da povzročijo določeno delovanje v telesu.
Agonist- ligand, ki se veže na receptor in povzroči biološki odziv, ki sproži fiziološki sistem. Popoln agonist- največji odziv, Delno- povzročajo manjšo reakcijo, tudi če so vsi receptorji zasedeni.
Antagonist- ligandi, ki zasedajo receptorje ali jih spremenijo tako, da izgubijo sposobnost interakcije z drugimi ligandi, sami pa ne povzročijo biološke reakcije (blokirajo delovanje agonistov).
 Konkurenčni antagonisti- reverzibilno delujejo z receptorji in tako tekmujejo z agonisti. Povečanje koncentracije agonista lahko popolnoma odpravi učinek antagonista. Kompetitivni antagonist premakne krivuljo odmerka in odziva za agonist, poveča EC50, ne vpliva na Emax.
Konkurenčni antagonisti- reverzibilno delujejo z receptorji in tako tekmujejo z agonisti. Povečanje koncentracije agonista lahko popolnoma odpravi učinek antagonista. Kompetitivni antagonist premakne krivuljo odmerka in odziva za agonist, poveča EC50, ne vpliva na Emax.
Nekonkurenčni antagonisti- ireverzibilno spremeni afiniteto receptorjev za agonist, vezava se pogosto ne zgodi z aktivnim mestom receptorja, povečanje koncentracije agonista ne odpravi učinka antagonista. Nekonkurenčni antagonist zmanjša Emax, ne spremeni EC50, krivulja odmerek-učinek pa se stisne okoli navpične osi.
36. Kvantitativni vzorci delovanja zdravil. Zakon padajočega odziva bioloških sistemov. Clarkov model in njegove posledice. Splošna oblika odvisnosti koncentracija - učinek v normalnih in lognormalnih koordinatah.
Clark-Ariens model:
1. Interakcija med ligandom (L) in receptorjem (R) je reverzibilna.
2. Vsi receptorji za dani ligand so enakovredni in neodvisni (njihova nasičenost ne vpliva na druge receptorje).
3. Učinek je neposredno sorazmeren s številom zasedenih receptorjev.
4. Ligand obstaja v dveh stanjih: prost in vezan na receptor.
A) ![]() , kjer je Kd ravnotežna konstanta, Ke je notranja aktivnost.
, kjer je Kd ravnotežna konstanta, Ke je notranja aktivnost.
B) Ker bodo s povečanjem števila ligandov v nekem trenutku vsi receptorji zasedeni, je največje možno število nastalih kompleksov ligand-receptor opisano s formulo:
= [R] × ![]() (1)
(1)
Učinek je določen z verjetnostjo aktivacije receptorja ob vezavi na ligand, torej z njegovo intrinzično aktivnostjo (Ke), torej E = Ke ×. V tem primeru je učinek največji pri Ke = 1 in najmanjši in Ke = 0. Seveda je največji učinek opisan z razmerjem Emax = Ke ×, kjer je skupno število receptorjev za dani ligand
Učinek je torej odvisen tudi od koncentracije liganda na [C] receptorjih
E = Emax ![]() (2)
(2)
Iz zgornjih razmerij sledi, da je EC50 = Kd
![]()
Emax je največji učinek, Bmax je največje število vezanih receptorjev, EC50 je koncentracija zdravila, pri kateri se pojavi učinek, enak polovici največjega, Kd je konstanta disociacije snovi od receptorja, pri kateri 50 % receptorji so vezani.
Zakon padajočega odziva ustreza parabolična odvisnost "koncentracija - učinkovitost". Odziv na nizke odmerke zdravil se običajno poveča neposredno sorazmerno z odmerkom... Vendar, ko se odmerek poveča, se povečanje odziva zmanjša in sčasoma je mogoče doseči odmerek, pri katerem ni nadaljnjega povečanja odziva (zaradi zasedenosti vseh receptorjev za dani ligand).
37. Spreminjanje učinka zdravil. Postopno in kvantno vrednotenje učinka, bistva in klinične uporabe. Ukrepi za kvantificiranje aktivnosti in učinkovitosti zdravil v eksperimentalni in klinični praksi.
Vse farmakološke učinke lahko v grobem razdelimo v dve kategoriji:
A) Postopni (neprekinjeni, integralni) učinki- takšni učinki zdravil, ki jih je mogoče kvantitativno izmeriti (učinek antihipertenzivnih zdravil - po ravni krvnega tlaka). Opisana je postopna "krivulja odmerek-učinek" (glej str. 36), na podlagi katere je mogoče oceniti: 1) individualno občutljivost na zdravila 2) aktivnost zdravila 3) največjo učinkovitost zdravila.
B) Kvantni učinki- takšni učinki zdravil, ki so diskretna vrednost, kvalitativni znak, torej jih opisuje le nekaj variant stanj (glavobol po jemanju analgetika, prisoten ali ne). Opisana je kvantna krivulja odmerek-učinek, kjer je ugotovljena odvisnost manifestacije učinka v populaciji od vrednosti zaužitega odmerka zdravila. Graf odmerka in učinka je v obliki kupole in je identičen Gaussovi krivulji normalne porazdelitve. Na podlagi kvantne krivulje lahko: 1) ocenimo populacijsko občutljivost zdravil; 2) opazimo prisotnost učinka pri danem odmerku; 3) izberemo povprečni terapevtski odmerek.
Razlike med postopnimi in kvantnimi značilnostmi odmerka in učinka:
Kvantitativna ocena aktivnosti in učinkovitosti zdravil se izvede na podlagi sestave krivulj odmerek-učinek in njihove naknadne ocene (glej 35. odstavek).
38. Vrste delovanja zdravil. Spremembe delovanja zdravil ob ponovnem dajanju.
Vrste delovanja zdravila:
1. Lokalno delovanje- učinek snovi, ki se pojavi na mestu nanosa (anestetik - na sluznico)
2. Resorptivno (sistemsko) delovanje- učinek snovi, ki se razvije po njeni absorpciji, vstopu v splošni krvni obtok in nato v tkiva. Odvisno od poti dajanja zdravil in njihove sposobnosti, da prodrejo skozi biološke ovire.
Z lokalnim in resorptivnim delovanjem imajo lahko zdravila oboje Neposredno oz Refleks vpliv:
A) neposredni vpliv – neposreden stik s ciljnim organom (adrenalin na srce).
B) refleks - sprememba delovanja organov ali živčnih centrov z vplivom na ekstero- in interoreceptorje (gorčični ometi refleksno izboljšajo svojo trofizem pri patologiji dihal)
Spremembe delovanja zdravil, ko se ponovno uvedejo:
1. Kumulacija- povečanje učinka zaradi kopičenja zdravil v telesu:
a) kumulacija materiala - kopičenje učinkovine v telesu (srčni glikozidi)
b) funkcionalna kumulacija - naraščajoče spremembe v delovanju telesnih sistemov (spremembe delovanja centralnega živčevja pri kroničnem alkoholizmu).
2. Toleranca (odvisnost) - Zmanjšanje odziva telesa na ponavljajoče se injekcije zdravil; za ponovno vzpostavitev reakcije na zdravila ga je treba dajati v vedno večjih odmerkih (diazepam):
A) resnična toleranca - opažena tako pri enteralnem kot parenteralnem dajanju zdravil, ni odvisna od stopnje njegove absorpcije v krvni obtok. Temelji na farmakodinamičnih mehanizmih odvisnosti:
1) desenzibilizacija - zmanjšanje občutljivosti receptorja na zdravilo (b-adrenergični agonisti pri dolgotrajni uporabi vodijo do fosforilacije b-adrenergičnih receptorjev, ki se ne morejo odzvati na b-adrenergične agoniste)
2) Down-regulation - zmanjšanje števila receptorjev za zdravila (pri večkratnem dajanju narkotičnih analgetikov se zmanjša število opioidnih receptorjev in potrebnih je vedno več odmerkov zdravila za induciranje želenega odziva). Če zdravilo blokira receptorje, je lahko mehanizem tolerance nanj povezan z regulacijo navzgor – povečanjem števila receptorjev za zdravila (b-blokatorji)
3) vključitev kompenzacijskih mehanizmov regulacije (pri ponavljajočih se injekcijah antihipertenzivnih zdravil se kolaps pojavlja veliko manj pogosto kot pri prvem dajanju zaradi prilagoditve baroreceptorjev)
B) relativna toleranca (psevdotoleranca) - se razvije le z vnosom zdravil v notranjost in je povezana z zmanjšanjem hitrosti in popolnosti absorpcije zdravila
3. Tahifilaksa- stanje, pri katerem pogosto dajanje zdravil povzroči razvoj tolerance po nekaj urah, pri dokaj redkih dajah zdravil pa se njegov učinek v celoti ohrani. Razvoj tolerance je običajno povezan z izčrpanjem efektorskih sistemov.
4. Zasvojenost z mamili- neustavljiva želja po zaužitju predhodno uporabljene snovi. Razdelite duševno (kokain) in fizično (morfij) odvisnost od drog.
5. Preobčutljivost- alergijska ali druga imunološka reakcija na zdravila ob večkratnem dajanju.
39. Odvisnost delovanja zdravil od starosti, spola in posameznih značilnosti organizma. Pomen cirkadianih ritmov.
A) Od starosti: pri otrocih in starejših je povečana občutljivost na zdravila (ker imajo otroci pomanjkanje številnih encimov, delovanje ledvic, povečana prepustnost BBB, v starosti je absorpcija zdravil upočasnjena, presnova je manj učinkovita, hitrost izločanja zdravila preko ledvic se zmanjša):
|
1. Novorojenčki imajo zmanjšano občutljivost na srčne glikozide, saj imajo več Na + / K + -ATPaz (tarče glikozidnega delovanja) na enoto površine kardiomiocita. 2. Otroci imajo manjšo občutljivost za sukcinilholin in atrakurijo, vendar povečano občutljivost na vse druge mišične relaksante. 3. Psihotropna zdravila lahko pri otrocih povzročijo nenormalne reakcije: psihostimulansi – lahko povečajo koncentracijo in zmanjšajo motorično hiperaktivnost, pomirjevala – nasprotno, lahko povzročijo t.i. atipična vznemirjenost. |
1. Občutljivost na srčne glikozide se močno poveča zaradi zmanjšanja števila Na + / K + -ATPaz. 2. Zmanjša občutljivost na b-blokatorje. 3. Občutljivost na zaviralce kalcijevih kanalčkov se poveča, ker je barorefleks oslabljen. 4. Obstaja netipična reakcija na psihotropna zdravila, podobna reakciji otrok. |
B) S tal:
1) antihipertenzivi - klonidin, b-blokatorji, diuretiki lahko povzročijo spolne motnje pri moških, vendar ne vplivajo na delo razmnoževalni sistemženske.
2) anabolični steroidi so učinkovitejši pri ženskah kot pri moških.
V) Od posameznih značilnosti organizma: pomanjkanje ali presežek nekaterih encimov presnove zdravil vodi do povečanja ali zmanjšanja njihovega delovanja (pomanjkanje krvne psevdoholinesteraze - nenormalno podaljšana mišična relaksacija pri uporabi sukcinilholina)
G) Iz cirkadianih ritmov: sprememba učinka zdravil na telo, kvantitativno in kvalitativno, odvisno od časa dneva (maksimalni učinek z največjo aktivnostjo).
40. Spremenljivost in variabilnost delovanja zdravil. Hipo- in hiperreaktivnost, toleranca in tahifilaksija, preobčutljivost in idiosinkrazija. Razlogi za variabilnost delovanja zdravil in racionalne strategije terapije.
Spremenljivost odraža razlike med posamezniki v odzivu na dano zdravilo.
Razlogi za variabilnost delovanja zdravila:
1) sprememba koncentracije snovi v receptorskem območju - zaradi razlik v hitrosti absorpcije, njene porazdelitve, presnove, izločanja
2) variacije v koncentraciji endogenega liganda receptorja - propranolol (β-blokator) upočasni srčni utrip pri ljudeh s povišanimi ravnmi kateholaminov v krvi, ne vpliva pa na srčni utrip v ozadju pri športnikih.
3) spremembe gostote ali delovanja receptorjev.
4) spremembe v reakcijskih komponentah, ki se nahajajo distalno od receptorja.
Strategija racionalne terapije: imenovanje in odmerjanje zdravil ob upoštevanju zgornjih razlogov za variabilnost delovanja zdravila.
Hiporeaktivnost- zmanjšanje učinka danega odmerka zdravil v primerjavi z učinkom, ki ga opazimo pri večini bolnikov. Hiperreaktivnost- povečanje učinka danega odmerka zdravil v primerjavi z učinkom, ki ga opazimo pri večini bolnikov.
Toleranca, tahifilaksa, preobčutljivost - glej točko 38
Idiosinkrazija- sprevržena reakcija telesa na dano zdravilo, povezana z genetskimi značilnostmi presnove zdravil ali z individualno imunološko reaktivnostjo, vključno z alergijskimi reakcijami.
41. Ocena varnosti zdravil. Terapevtski indeks in standardne varnostne meje.
Ocena varnosti se izvaja na dveh ravneh:
A) predklinični (pridobivanje informacij o toksičnosti zdravil, učinkih na reproduktivno funkcijo, embriotoksičnosti in teratogenosti, dolgotrajnih učinkih)
B) klinični (nadaljnja ocena učinkovitosti in varnosti zdravil)
Če po doseženem platoju učinka odmerek zdravila še naprej raste, se bo po določenem času začel manifestirati njegov toksični učinek. Odvisnost toksičnega učinka od odmerka (koncentracije) zdravila je enake narave kot njegov ugoden učinek in ga lahko opišemo s postopnimi ali kvantnimi krivuljami. Te krivulje je mogoče uporabiti tudi za določitev vrednosti TD50 ali TC50- toksični odmerek (koncentracija) zdravil, ki povzroči toksični učinek, enak 50 % največjega (za kvantno krivuljo - toksični učinek pri 50 % posameznikov v populaciji). Včasih namesto TD50 uporabljajo indikator LD50 - smrtonosni odmerek, kar povzroči smrt 50 % predmetov v populaciji.
Ocena varnosti zdravila je označena na podlagi stopenj ali kvantnih krivulj odmerka in učinka in naslednjih kazalnikov:
A) Terapevtski indeks Je razmerje med toksičnimi in učinkovitimi odmerki zdravila, ki povzročajo pojav polovičnega maksimalnega učinka: TI = TD50 / ED50. Višja kot je vrednost terapevtskega indeksa, varnejše je zdravilo.
B) Terapevtska širina (terapevtsko okno) Je razpon odmerkov med minimalnimi terapevtskimi in minimalnimi toksičnimi odmerki zdravil. Je bolj pravilen kazalnik varnosti zdravila, saj omogoča upoštevanje stopnje povečanja neželenih učinkov na krivulji odmerek-učinek.
V) Zanesljiv varnostni faktor Ali je razmerje med najmanjšim toksičnim odmerkom in največjim učinkovitim odmerkom (NFD = TD1 / ED99), kaže, kolikokrat je mogoče preseči terapevtski odmerek zdravila brez tveganja zastrupitve (neželeni učinki).
G) Terapevtski koridor Je obseg učinkovitih koncentracij zdravila v krvi, ki ga je treba ustvariti in vzdrževati v telesu, da se doseže želeni terapevtski učinek.
42,46. Interakcija zdravil. Nezdružljivost zdravil (ker so vprašanja medsebojno povezana, izberite glede na okoliščine)
Interakcija z zdravili- to je sprememba resnosti in narave učinkov ob hkratni ali predhodni uporabi več zdravil.
Razlogi za neželene interakcije:
1) polifarmacija - 6 ali več zdravil daje 7-krat več stranskih učinkov, kot če je zdravil manj kot 6.
2) napake zdravnikov
3) kršitev režima odmerjanja
Utemeljitev kombinirane terapije:
1. Monoterapija ni dovolj učinkovita.
2. Odsotnost etiotropne terapije pri večini bolezni Þ potreba po delovanju zdravila na različnih povezavah patogeneze
3. Polimorbidnost – starejši ko je človek, več bolezni ima, ki se pojavljajo hkrati
4. Potreba po odpravi neželenih učinkov zdravil
5. Zmanjšanje števila sprejemov in dajanja zdravil (udobje za pacienta, prihranek dela zdravstvenih delavcev)
Vrste interakcij:
jaz. Farmacevtske interakcije - Vrsta interakcije, povezana s fizikalno-kemijsko reakcijo med zdravili med proizvodnim procesom zdravilo, še pred vnosom teh sredstev v človeško telo
A) tipične napake, ki vodijo v farmacevtsko nezdružljivost: pisanje zapletenih receptov, nepravilno shranjevanje, možnost adsorpcije zdravil na površini plastike (organski nitrati) se ne upošteva
B) težave z infuzijsko terapijo: mešanje topnih soli, derivatov netopnih šibkih kislin ali baz vodi do njihove precipitacije; v tekočini dozirne oblike srčni glikozidi in alkaloidi se hidrolizirajo, AB se uniči; pH medija (alkaloidi se oborijo v alkalnem mediju)
C) priporočila: 1) Vse mešanice je bolje pripraviti ex tempore 2) Najbolj zanesljiva rešitev je z enim zdravilom 3) Vse raztopine je treba pred uporabo preveriti glede suspenzije 4) Do interakcije lahko pride brez vidnih sprememb v raztopinah 5) Zdravila ne morejo dodajati v kri in raztopine AK 6) Če ni posebnih navodil, je treba pripravke raztopiti v 5 % raztopini glukoze (pH 3,5-6,5), izotonični raztopini NaCl (pH 4,5-7,0).
Raztopina glukoze, stabilizirana s HCl, ni združljiva z epinefrinom, benzilpenicilinom, apomorfinom, kanamicinom, vitaminom C, oleandomicinom, srčnimi glikozidi. Srčni glikozidi so nezdružljivi z atropinom, papaverinom, platifilinom. AB so nezdružljivi s heparinom, hidrokortizonom. Vitamini skupine B so med seboj nezdružljivi, z vitamini PP, C. Tudi vitamini PP in C so med seboj nezdružljivi.
Ne sme se mešati z drugimi zdravili: fenotiazidom, klorpromazinom, barbiturati, pripravki vitamina C, amfotericinom B, furosemidom, sulfadiazinom, aminofilinom, adrenomimetiki.
II... Farmakološki- interakcija z zdravili, ki se kaže le v človeškem telesu po njihovi kombinirani uporabi
A) farmakokinetika
1) med fazo sesanja.
Pri uvajanjuPer Osinterakcijo določa:
1.kislost okolja
2.neposredna interakcija v prebavnem traktu
Tetraciklini medsebojno delujejo s kalcijem, aluminijem, železom, magnezijem in tvorijo kelatne komplekse. Holestiramin moti absorpcijo kislinskih derivatov, pripravkov kalcija, varvarina, digoksina, digitoksina, vitaminov, topnih v maščobah, trimetoprima, klindamicina, cefaleksina, tetraciklina. Pripravki železa se bolje absorbirajo z vitaminom C. Pripravki železa s karbonati, tetraciklini se slabo absorbirajo.
3.Gastrointestinalna gibljivost
Upočasnitev peristaltike: nekateri antidepresivi, antihistaminiki, fenotiazinski antipsihotiki, narkotiki, povečajo absorpcijo digoksina, kortikosteroidi, antikoagulanti, zmanjšajo absorpcijo levodope. Okrepiti peristaltiko in povečati evakuacijo iz prebavil: metoklopramid, odvajala. Zmanjšajo absorpcijo zdravil: fenobarbital - grizeofulvin, aspirin - indometacin in diklofenak, PASK - rifampicin.
Metode za nadzor absorpcije med parenteralnim dajanjem: lokalni anestetiki + epinefrin + fenilefrin - zmanjša se absorpcija lokalnih anestetikov
4.črevesna flora
5.sprememba sesalnega mehanizma
2) pri distribuciji in deponiranju:
1. neposredna interakcija v krvni plazmi: gentamicin + ampicilin ali karbenicilin - zmanjša aktivnost gentamicina
2. konkurenčni odmik od povezave z albuminom v krvni plazmi: indometacin, digitoksin, varfarin so povezani s krvnimi beljakovinami za 90-98%, zato je dvakratno povečanje proste frakcije zdravil močno povečanje toksičnih učinkov; Nesteroidna protivnetna zdravila nadomeščajo: varfarin, fenitoin, metotreksat.
Determinante za klinični pomen te interakcije:
ü Vd vrednost (velika - ni problema, majhna - možno)
ü učinek ene zdravilne učinkovine na delovanje transportnih mehanizmov prek mehanizmov drugih zdravil: transport zdravila se povečuje odvisno od odmerka - insulina, ACTH, angiotenzina, kininov itd.; insulin poveča koncentracijo izoniazida samo v pljučih, koncentracijo bombaža - samo v SMC.
3. Izpodrivanje iz vezave na tkivne beljakovine: kinidin izpodriva digoksin + zmanjša izločanje skozi ledvice, s čimer se poveča tveganje za toksičnost digoksina
3) v procesu presnove
Zdravila lahko povečajo ali zmanjšajo aktivnost citokroma P450 in njegovih encimov (etanol poveča aktivnost nekaterih izoencimov citokroma)
Pogosto medsebojno delujoči zaviralci encimov:
1. AB: ciprofloksacin, eritromicin, izoniazid, metronidazol
2. Srčno-žilna zdravila: amiodaron, diltiazem, kinidin, verapamil
3. Antidepresivi: fluoksetin, sertralen
4. Antisekretorna zdravila: cimetidin, omeprazol
5. Protirevmatična zdravila: alopurinol
6. Fungicidi: flukonazol, intrakanazol, ketokonazol, mikonazol
7. Protivirusna zdravila: indinavir, retonavir, sakvinavir
8. Drugi: disulfiram, natrijev valproat
Zdravila, ki imajo toksične učinke pri zaviranju MAO: adrenomimetiki, simpatikomimetiki, antiparkinsoniki, narkotični analgetiki, fenotiazini, pomirjevala, antihipertenzivni diuretiki, hipoglikemična zdravila
4) V procesu valjenja- več kot 90 % zdravil se izloči z urinom.
Vpliv na pH urina in na stopnjo ionizacije zdravila, na njihovo lipofilnost in njihovo reabsorpcijo
1.interakcija med pasivno difuzijo: del zdravila se izloči nespremenjen, del zdravila se ionizira pri pH urina 4,6-8,2. Alkalinizacija urina je klinično pomembna: zastrupitev z acetilsalicilno kislino ali fenobarbitalom, pri jemanju sulfonamidov (zmanjšanje tveganja za kristalurijo), jemanju kinidina. Povečana kislost urina: povečano izločanje amfetamina (praktičnega pomena za odkrivanje tega zdravila pri športnikih)
2. interakcija v obdobju aktivnega transporta: probenezid + penicilin poveča trajanje gibanja penicilina, probenecid + salicilati - odprava urikozurnega delovanja probenecida, penicilin + CA - zmanjšanje izločanja penicilina
Vpliv sestave urina na izločanje zdravila:
Povečanje sladkorja v urinu - povečanje izločanja: vitamina C, kloramfenikola, morfija, izoniazida, glutationa in njihovih metabolitov.
B) farmakodinamični Ali je medsebojno delovanje zdravil povezano s spremembo farmakodinamike enega od njih pod vplivom drugega (pod vplivom ščitničnih hormonov se poveča sinteza b-adrenergičnih receptorjev v miokardu in poveča učinek adrenalina na miokard ).
Primeri klinično pomembnih nezaželenih sinergijskih interakcij:
NSAID + varvarin - povečano tveganje za krvavitev
Alkohol + benzodiazepini - okrepitev sedativnega učinka
Zaviralci ACE + K + -varčevalni diuretiki - povečano tveganje za hiperkaliemijo
Verapamil + b-blokatorji - bradikardija in asistola
Alkohol je močan induktor mikrosomskih encimov, vodi v razvoj tolerance na zdravila (zlasti na anestetike in hipnotike), povečuje tveganje za odvisnost od drog.
43. Interakcija z zdravili. Antagonizem, sinergija, njihove vrste. Narava spremembe učinka zdravil (aktivnost, učinkovitost) je odvisna od vrste antagonizma.
Pri medsebojnem delovanju zdravila se lahko razvijejo naslednji pogoji: a) povečanje učinkov kombinacije zdravil b) oslabitev učinkov kombinacije zdravil c) nezdružljivost zdravil
Krepitev učinkov kombinacije zdravil se izvaja na tri načine:
1) Seštevanje učinkov ali aditivna interakcija- vrsta interakcije z zdravili, pri kateri je učinek kombinacije enak preprosti vsoti učinkov vsakega od zdravil posebej. tj. 1+1=2 ... Značilna je za zdravila iz ene farmakološke skupine, ki imajo skupen cilj delovanja (kislinsko nevtralizirajoča aktivnost kombinacije aluminijevega in magnezijevega hidroksida je enaka vsoti njihovih sposobnosti nevtralizacije kisline posebej)
2) sinergija - vrsta interakcije, pri kateri učinek kombinacije presega vsoto učinkov vsake od snovi, vzetih posebej. tj. 1+1=3 ... Sinergija se lahko nanaša tako na želene (terapevtske) kot na neželene učinke zdravil. Kombinirana uporaba tiazidnega diuretika dihlotiazida in zaviralca ACE enalaprila vodi do povečanja hipotenzivnega učinka vsakega od zdravil, ki se uporablja pri zdravljenju hipertenzije. Vendar pa sočasno dajanje aminoglikozidnih antibiotikov (gentamicin) in diuretika zanke furosemida močno poveča tveganje za ototoksično delovanje in razvoj gluhosti.
3) potenciranje - vrsta interakcije z zdravili, pri kateri lahko eno od zdravil, ki samo po sebi nima tega učinka, povzroči močno povečanje učinka drugega zdravila. tj. 1+0=3 (klavulanska kislina nima protimikrobnega učinka, lahko pa okrepi učinek b-laktamskega antibiotika amoksicilina, ker blokira b-laktamazo; adrenalin nima lokalnega anestetičnega učinka, če pa ga dodamo raztopini ultrakaina , močno podaljša svoj anestetični učinek z upočasnitvijo absorpcije anestetika z mesta injiciranja).
Blažilni učinki Droge, kadar se uporabljajo skupaj, imenujemo antagonizem:
1) Kemični antagonizem ali protistrup- kemična interakcija snovi med seboj s tvorbo neaktivnih produktov (kemični antagonist železovih ionov deferoksamin, ki jih veže v neaktivne komplekse; protamin sulfat, katerega molekula ima presežek pozitivni naboj - kemični antagonist heparina, molekula od tega ima presežek negativni naboj). Kemični antagonizem je osnova delovanja protistrupov (antidotov).
2) Farmakološki (neposredni) antagonizem- antagonizem, ki ga povzroča večsmerno delovanje dveh zdravilnih učinkovin na iste receptorje v tkivih. Farmakološki antagonizem je lahko konkurenčen (reverzibilen) in nekonkurenčen (nepovraten):
A) kompetitivni antagonizem: kompetitivni antagonist se reverzibilno veže na aktivno središče receptorja, torej ga ščiti pred delovanjem agonista. Ker je stopnja vezave snovi na receptor sorazmerna s koncentracijo te snovi, je učinek kompetitivnega antagonista mogoče premagati s povečanjem koncentracije agonista. Izpodrinil bo antagonist z aktivnega mesta receptorja in povzročil popoln odziv tkiva. To kompetitivni antagonist ne spremeni največjega učinka agonista, vendar je za interakcijo agonista z receptorjem potrebna višja koncentracija. Konkurenčni antagonist Premakne krivuljo odmerka in odziva za agonist v desno glede na začetne vrednosti in poveča EC50 za agonist, ne da bi vplival na vrednost E maks.
Konkurenčni antagonizem se pogosto uporablja v medicinski praksi. Ker je učinek kompetitivnega antagonista mogoče premagati, če njegova koncentracija pade pod raven agonista, je treba med zdravljenjem s kompetitivnimi antagonisti nenehno vzdrževati dovolj visoko raven. Z drugimi besedami, klinični učinek kompetitivnega antagonista bo odvisen od njegove razpolovne dobe izločanja in koncentracije celotnega agonista.
B) nekonkurenčni antagonizem: nekonkurenčni antagonist se skoraj nepopravljivo veže na aktivno središče receptorja ali na splošno deluje z njegovim alosteričnim centrom. Zato, ne glede na to, kako se koncentracija agonista poveča, ne more izpodriniti antagonista iz njegove povezave z receptorjem. Ker nekaterih receptorjev, ki so povezani z nekonkurenčnim antagonistom, ni več mogoče aktivirati , vrednost Emaks zmanjša, se afiniteta receptorja za agonist ne spremeni, zato ostane vrednost EC50 enaka. Na krivulji odziva na odmerek se delovanje nekonkurenčnega antagonista kaže kot stiskanje krivulje glede na navpično os, ne da bi se premaknila v desno.
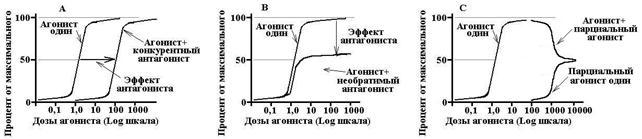
Shema 9. Vrste antagonizma.
A - kompetitivni antagonist premakne krivuljo odmerek-učinek v desno, to pomeni, da zmanjša občutljivost tkiva na agonist, ne da bi spremenil njegov učinek. B - nekonkurenčni antagonist zmanjša obseg odziva tkiva (učinek), vendar ne vpliva na njegovo občutljivost na agonist. C - različica uporabe delnega agonista v ozadju polnega agonista. Ko se koncentracija poveča, delni agonist izpodrine celotnega iz receptorjev in posledično se odziv tkiva zmanjša od največjega odziva na polni agonist do največjega odziva na delni agonist.
Nekonkurenčni antagonisti se v medicinski praksi redkeje uporabljajo. Po eni strani imajo nedvomno prednost, saj njihovega učinka po vezavi na receptor ni mogoče premagati in zato ni odvisen od obdobja polovične izločanja antagonista ali od nivoja agonista v telesu. Učinek nekonkurenčnega antagonista bo določen samo s hitrostjo sinteze novih receptorjev. Toda po drugi strani, če pride do prevelikega odmerjanja tega zdravila, bo zelo težko odpraviti njegov učinek.
|
Konkurenčni antagonist |
Nekonkurenčni antagonist |
|
Po strukturi je podoben agonistu |
Strukturno drugačen od agonista |
|
Veže se na aktivno središče receptorja |
Veže se na alosterično mesto receptorja |
|
Premakne krivuljo odmerek-odziv v desno |
Navpično premakne krivuljo odziva na odmerek |
|
Antagonist zmanjša občutljivost tkiva na agonist (EC50), vendar ne vpliva na največji učinek (Emax), ki ga je mogoče doseči pri višji koncentraciji. |
Antagonist ne spremeni občutljivosti tkiva na agonist (EC50), ampak zmanjša notranjo aktivnost agonista in največji odziv tkiva nanj (Emax). |
|
Delovanje antagonista je mogoče obrniti z visokim odmerkom agonista |
Antagonističnega učinka ni mogoče obrniti z visokim odmerkom agonista. |
|
Učinek antagonista je odvisen od razmerja odmerkov agonista in antagonista |
Učinek antagonista je odvisen le od njegovega odmerka. |
Losartan je kompetitivni antagonist proti receptorjem AT1 angiotenzina; moti interakcijo angiotenzina II z receptorji in pomaga zniževati krvni tlak. Učinke losartana je mogoče premagati z dajanjem velikega odmerka angiotenzina II. Valsartan je nekonkurenčni antagonist za iste receptorje AT1. Njegovega učinka ni mogoče premagati niti z dajanjem velikih odmerkov angiotenzina II.
Zanimiva je interakcija, ki poteka med polnimi in delnimi agonisti receptorjev. Če koncentracija celotnega agonista presega raven delnega, se v tkivu opazi največji odziv. Če se raven delnega agonista začne povečevati, izpodrine polni agonist iz vezave na receptor in odziv tkiva se začne zmanjševati od maksimuma za polni agonist do maksimuma za delni agonist (tj. zaseda vse receptorje).
3) Fiziološki (posredni) antagonizem- antagonizem, povezan z vplivom dveh zdravil na različne receptorje (tarče) v tkivih, kar vodi do medsebojnega oslabitve njihovega učinka. Na primer, opazimo fiziološki antagonizem med insulinom in adrenalinom. Inzulin aktivira inzulinske receptorje, zaradi česar se poveča transport glukoze v celico in zmanjša raven glikemije. Epinefrin aktivira b2-adrenergične receptorje v jetrih, skeletnih mišicah in spodbuja razgradnjo glikogena, kar na koncu vodi v zvišanje ravni glukoze. Ta vrsta antagonizma se pogosto uporablja pri nujni oskrbi bolnikov s prevelikim odmerkom insulina, ki je povzročil hipoglikemično komo.
44. Stranski in toksični učinki zdravil. Teratogeni, embriotoksični, mutageni učinki zdravil.
Stranski učinki- tisti učinki, ki se pojavijo pri uporabi snovi v terapevtskih odmerkih in predstavljajo spekter njihovega farmakološkega delovanja (analegetik morfij v terapevtskih odmerkih povzroča evforijo), so lahko primarni in sekundarni:
A) primarni stranski učinki- kot neposredna posledica vpliva tega zdravila na določenem substratu (hiposalivacija pri uporabi atropina za odpravo bradiaritmije)
B) sekundarni stranski učinki - posredni neželeni učinki (AB, ki zavira normalno mikrofloro, lahko vodi do superinfekcije)
Toksični učinki – neželeni učinki se pri tem zdravilu manifestira, ko zapusti terapevtsko območje (preveliko odmerjanje zdravila)
Selektivnost delovanja zdravila je odvisna od njegovega odmerka. Višji kot je odmerek zdravila, manj selektivno postane.
Teratogeno delovanje- sposobnost zdravil pri nosečnici, da povzročijo anatomske nepravilnosti v razvoju ploda (talidomid: fokomelija, antiblastomska zdravila: več okvar)
Embriotoksično delovanje- škodljiv učinek, ki ni povezan s kršitvijo organogeneze v prvih treh mesecih nosečnosti. Kasneje se pojavi Fetotoksično delovanje.
Mutageni učinek zdravil- poškodba zarodne celice in njenega genetskega aparata zdravil, ki se kaže s spremembo genotipa potomcev (adrenalin, citostatiki).
Rakotvorni učinek zdravil- sposobnost nekaterih zdravil, da inducirajo karcinogenezo.
45. Medicinski in socialni vidiki boja proti odvisnosti od drog, odvisnosti od drog in alkoholizma. Koncept zlorabe snovi.
« Malo verjetno je, da bo človeštvo kot celota kdaj brez umetnega raja. Večina moških in žensk živi tako boleče življenje, ki je v najboljšem primeru tako monotono, bedno in omejeno, da je želja, da bi ga »zapustili«, da bi se vsaj za nekaj trenutkov odklopili, bila in je vedno bila ena glavnih. Zaželeno Nja duša"(Huxley, delo "Vrata zaznave")
1) Zasvojenost z mamili- stanje duha in/ali fizično stanje, ki je posledica delovanja zdravil na telo in za katerega so značilne specifične vedenjske reakcije, težko je premagati željo po ponovnem jemanju zdravil, da bi dosegli posebno duševni učinek ali da bi se izognili nelagodju v odsotnosti zdravil v telesu. Za odvisnost od drog je značilno:
A) Psihološka odvisnost- razvoj čustvene stiske ob prenehanju jemanja drog. Človek se počuti praznega, pade v depresijo, doživlja občutek strahu, tesnobe, njegovo vedenje postane agresivno. Vsi ti psihopatološki simptomi se pojavijo v ozadju misli o potrebi po injiciranju zdravila, ki je povzročilo odvisnost. Želja po uživanju drog se lahko giblje od preproste želje do strastne žeje po jemanju drog, ki absorbira vse druge potrebe in se spremeni v smisel človekovega življenja. Menijo, da se psihološka odvisnost razvije, ko se človek zave, da lahko optimalno počutje doseže le z uvajanjem drog. Osnova psihološke odvisnosti je človekovo prepričanje v delovanje zdravila (v literaturi so opisani primeri razvoja psihološke odvisnosti od placeba).
B) Fizična odvisnost- kršitev normalnega fiziološkega stanja telesa, ki zahteva stalno prisotnost zdravil v njem za vzdrževanje stanja fiziološkega ravnovesja. Prenehanje jemanja zdravila povzroči razvoj specifičnega kompleksa simptomov - odtegnitvenega sindroma - kompleksa duševnih in nevrovegetativnih motenj v obliki disfunkcije v nasprotni smeri od tiste, ki je značilna za delovanje (morfij odpravlja bolečino, zavira dihalni center, zoži zenice, povzroči zaprtje; z odtegnitvenimi simptomi se pri bolniku pojavijo hude bolečine, pogosto hrupno dihanje, zenice so razširjene in se razvije vztrajna driska)
V) Toleranca... Toleranca do zdravil, ki povzročajo odvisnost od drog, je pogosto medsektorska, torej ne le na določeno kemično spojino, temveč tudi na vse strukturno podobne spojine. Na primer, pri bolnikih z odvisnostjo od zdravil od morfija se toleranca ne pojavi le do njega, ampak tudi do drugih opioidnih analgetikov.
Za razvoj odvisnosti od drog prisotnost vseh 3 meril ni nujen pogoj; Tabela 3 prikazuje glavne vrste odvisnosti od drog in njene sestavine.
Opioidi, barbiturati, alkohol povzročajo močno fizično in psihično odvisnost ter toleranco. Anksiolitiki (diazepam, alprazolam) povzročajo predvsem psihološko odvisnost.
2) Zasvojenost ( zasvojenost z mamili) - To je izredno huda oblika odvisnosti od drog, kompulzivne uporabe drog, za katero je značilna vedno večja, neustavljiva želja po dajanju tega zdravila, povečanju njegovega odmerka. Kompulzivnost želje pomeni, da potreba po dajanju zdravila prevladuje nad vsemi drugimi (celo vitalnimi) potrebami bolnika. S stališča to definicijo, hrepenenje po morfiju je odvisnost od drog, medtem ko je hrepenenje po nikotinu odvisnost od drog.
3) Odvisen od medicine- zaznamuje manj intenzivno hrepenenje po zdravilih, ko zavrnitev zdravila povzroči le občutek rahlega nelagodja, brez razvoja fizične odvisnosti ali podrobne slike psihične odvisnosti. To Zasvojenost zajema tisti del odvisnosti od drog, ki ne ustreza definiciji odvisnosti. Na primer, prej omenjena odvisnost od nikotina je oblika odvisnosti.
4) Zloraba drog- nedovoljena uporaba zdravil v takih odmerkih in na načine, ki se razlikujejo od sprejetih zdravstvenih ali socialnih standardov v tej kulturi in v danem času... To zloraba drog zajema samo družbene vidike uživanja drog. Primer zlorabe je uporaba anabolični steroidi v športu ali za izboljšanje postave mladih moških.
5) Alkoholizem- kronična zloraba alkohola (etilnega alkohola), ki danes vodi v okvare številnih organov (jetra, prebavila, centralni živčni sistem, srčno-žilni sistem, imunski sistem) in jo spremlja psihofizična odvisnost.
6) Zloraba substanc- kronična zloraba različnih drog (vključno z drogami, alkoholom, halucinogeni), ki se kaže v različnih duševnih in somatskih motnjah, vedenjskih motnjah, socialni degradaciji.
Zdravljenje odvisnosti od drog težka in nehvaležna naloga. Še vedno ni ustvarjen učinkovita metodologija, kar bi zagotovilo uspešnost zdravljenja pri več kot 30-40 % bolnikov. Doseganje vidnih rezultatov je možno le ob popolnem sodelovanju bolnikov, zdravnika in družbenega okolja, v katerem je bolna oseba (načelo prostovoljnosti in individualnosti). Sodobne tehnike temeljijo na naslednjih načelih:
ü psihoterapevtske in delovnoterapevtske metode;
ü skupinsko zdravljenje in rehabilitacija (Društvo anonimnih alkoholikov, odvisnikov od drog)
ü postopna ali nenadna ukinitev zdravila v ozadju razstrupljevalne terapije
ü izvajanje nadomestne terapije (zamenjava narkotične droge s počasnimi in dolgodelujočimi analogi z njihovo kasnejšo odpovedjo; na primer program metadonske nadomestne terapije za odvisnike od heroina)
ü zdravljenje s specifičnimi antagonisti (nalokson in naltrekson) ali sredstvi za preobčutljivost (teturam)
ü nevrokirurške metode kriodestrukcije cingularnega vijuga in hipokampusa
47. Vrste farmakoterapije. Deontološki problemi farmakoterapije.
Farmakoterapija (FT) - niz metod zdravljenja, ki temeljijo na uporabi zdravil. Glavne vrste FT:
1.etiotropni PT - popravek in odprava vzroka bolezni (AB pri nalezljivih boleznih)
2.patogenetski FT - vpliv na mehanizem razvoja bolezni (zaviralci ACE pri hipertenziji)
3. simptomatska FT - odprava simptomov bolezni, če ni mogoče vplivati na njen vzrok ali patogenezo (NSAID za gripo)
4.Substitucija FT - uporaba zdravil v primeru pomanjkanja naravnih biološko aktivnih snovi (inzulin pri sladkorni bolezni)
5.profilaktični FT (cepiva, serumi, acetilsalicilna kislina za ishemično srčno bolezen)
Odnos družbe do drog na sedanji fazi : 1) želja po koristih brez tveganja 2) upanje na čudež, vizije 3) nerazumevanje tveganja uporabe drog 4) ogorčenje in "pravična ogorčenost", prenagljene ocene drog 5) želja po novih zdravilih
Odnos zdravnika do drog: terapevtski optimizem (zanašanje na zdravila kot močan sestavni del terapije), terapevtski nihilizem (zanikanje novih zdravil, privrženost določenim zdravilom, nezaupanje do novih zdravil)
Skladnost (skladnost) bolnika z zdravljenjem 1) razumevanje zdravnikovih navodil in ciljev zdravljenja 2) prizadevanje za natančno upoštevanje zdravnikovih predpisov.
Trenutno je na svetu približno 100.000 zdravil, v Republiki Belorusiji jih je registriranih več kot 4.000, od tega približno 300 vitalnih zdravil. Študij farmakologije pomaga, da se ne utopite v morju zdravil.
48. Osnovna načela zdravljenja in preprečevanja zastrupitve z zdravili. Antidotna terapija.
Razvrstitev strupenih snovi (OM):
1. Po pripadnosti določenim razredom kemičnih spojin: barbiturati, benzodiazepini, cianidi.
2. Po izvoru: nebiološke narave (kisline, alkalije, soli težkih kovin), strupeni odpadni produkti nekaterih MB (botulinum toksin), rastlinskega izvora (alkaloidi, glikozidi), živalskega izvora (kačji in čebelji strup)
3. Glede na stopnjo strupenosti: a) izjemno strupeno (DL50< 1 мг/кг) б) высоко токсические (1-50) в) сильно токсические (50-500) г) умеренно токсические (500-5000) д) мало токсические (5000-15000) е) практически нетоксические (> 15.000)
4. Po toksikološkem učinku: a) živčno-paralitični (bronhospazem, dispneja) b) kožno resorptivni c) splošno toksični (hipoksični krči, koma, paraliza) d) zadušljiv e) solzni in dražilni e) psihotropni (oslabljena duševna aktivnost, )
5. Glede na področje prednostne uporabe: industrijski strupi, pesticidi, gospodinjski strupi, kemična bojna sredstva, zdravilne snovi.
6. Glede na strupenost zdravil: Seznam A - zdravila, katerih namen, uporabo, odmerjanje in shranjevanje je treba zaradi visoke toksičnosti izvajati zelo previdno. Na istem seznamu so tudi zdravila, ki povzročajo odvisnost od drog; seznam B - zdravila, katerih imenovanje, uporabo, odmerjanje in shranjevanje je treba izvajati previdno v zvezi z možni zapleti pri uporabi brez zdravniškega nadzora.
Selektivno toksični učinek zdravil.
A) kardiotoksični: srčni glikozidi, kalijevi pripravki, antidepresivi
B) nevrotoksični: psihofarmakološka sredstva, oksikinolini, aminoglikozidi
B) hepatotoksični: tetraciklini, kloramfenikol, eritromicin, paracetamol
D) nefrotoksični: vankomicin, aminoglikozidi, sulfonamidi
E) gastroenterotoksični: steroidna protivnetna zdravila, nesteroidna protivnetna zdravila, rezerpin
E) hematotoksični: citostatiki, kloramfenikol, sulfonamidi, nitrati, nitriti
G) pnevmotoksični
Toksikokinetika - preučuje absorpcijo, porazdelitev, presnovo in izločanje zdravil, zaužitih v toksičnih odmerkih.
Vnos strupenih snovi v telo je možen a) enteralno b) parenteralno. Hitrost in popolnost absorpcije odražata hitrost razvoja toksičnega učinka in njegovo resnost.
Porazdelitev v telesu: Vd = D / Cmax - dejanski volumen, v katerem je strupena snov porazdeljena v telesu. Vd> 5-10 l / kg - OM je težko prenašati njegovo odstranitev (antidepresivi, fenotiazini). Vd< 1 л/кг – ОВ легче удалить из организма (теофиллин, салицилаты, фенобарбитал).
Preveliko odmerjanje- spremembe v farmakokinetičnih procesih: topnost, povezava z beljakovinami, presnova ® znatno povečanje proste frakcije zdravil ® toksični učinek.
Kinetika prvega reda se s povečanjem koncentracije zdravila spremeni v kinetiko ničelnega reda.
Toksigena faza je detoksikacijska terapija, somatogena faza je simptomatska terapija.
Toksikodinamika . Glavni mehanizmi toksičnega delovanja:
A) mediator: neposredni (po vrsti kompetitivne blokade - FOS, psihomimetiki) in posredni (aktivatorji ali zaviralci encimov)
B) interakcija z biomolekulami in znotrajceličnimi strukturami (hemolitične snovi)
C) presnova po vrsti smrtonosne sinteze (etilni alkohol, tiofos)
D) encimski (kačji strupi itd.)
Vrste delovanja: lokalno, refleksno, resorptivno.
Razvrstitev zastrupitve:
1. Etiopatogenetika:
a) nenamerno (samozdravljenje, napačen sprejem)
b) namerno (z namenom samomora, umora, razvoja nemočnega stanja pri žrtvi)
2. Klinična:
a) odvisno od stopnje razvoja zastrupitve: akutna (zaužitje enkratnega odmerka ali s kratkim časovnim intervalom toksičnega odmerka snovi), subakutna (zapozen razvoj klinične slike po enkratnem odmerku), kronična
b) odvisno od manifestacije glavnega sindroma: poškodba CVS, poškodba DS itd.
c) odvisno od resnosti bolnikovega stanja: blaga, zmerna, huda, izredno huda
3. Nozološki: upošteva ime zdravila, ime skupine snovi
Splošni mehanizem smrti v primeru zastrupitve:
A) poraz CVS:
1) znižanje krvnega tlaka, hipovolemija perifernih žil, kolaps, bradija ali tahikardija (triciklični antidepresivi, zaviralci beta, zaviralci kalcijevih kanalčkov)
2) aritmije (ventrikularna tahikardija, fibrilacija - triciklični antidepresivi, teofilin, amfetamin)
B) poškodbe centralnega živčnega sistema: stupor, koma ® depresija dihanja (zdravila, barbiturati, alkohol, hipno-sedativna zdravila)
C) konvulzije, mišična hiperreaktivnost in rigidnost ® hipertermija, mioglobinurija, odpoved ledvic, hiperkalemija
Toksikološka triada:
1) trajanje uporabe, odmerek in anamneza snovi ®.
2) ocena stanja zavesti po simptomih: dihanje, krvni tlak, telesna temperatura
3) laboratorijski podatki
Osnovna načela zdravljenja:
JAZ. Prva pomoč: umetno dihanje, masaža srca, anti-šok terapija, nadzor vodno-elektrolitnega ravnovesja
II... Zakasnjena absorpcija in odstranitev neabsorbiranega OM iz telesa:
Namen: prekiniti stik z OV
1. Parenteralna pot:
a) skozi pljuča:
1) ustavite vdihavanje
2) dražilne snovi (amoniak, formaldehid) ® za utrjevanje aktivnih gibov, ogrevanje, dajanje kisika in penilcev (za amoniak je sredstvo proti peni kis, za formaldehid pa razredčena raztopina amoniaka)
b) skozi kožo: sperite z veliko količino tople vode z milom ali detergentom, specifičnimi protistrupi, nevtralizacija in prenehanje izpostavljenosti OM na koži (FOS: sperite z vodo, odstranite z 10-15% amoniakom ali 5- 6 % raztopina natrijevega bikarbonata z vodo; fenolkrezol: rastlinsko olje ali etilen glikol, vendar ne vazelinsko olje, KMNO4: 0,5-1 % raztopina askorbinske kisline ali enake količine 3 % vodikovega peroksida in 3 % raztopine ocetne kisline, CCl4, terpentin, bencin : topla milnica)
c) pri injiciranju v okončino: podvezek nad mestom injiciranja
d) v primeru stika z očmi: izpirati s toplo fiziološko raztopino ali mlekom 10-20 minut, nakapati lokalni anestetik; v primeru stika s kislinami in alkalijami jih ni mogoče nevtralizirati. Potreben je posvet z oftalmologom.
2. Enteralna pot: osvoboditi želodec pred OM, pospešiti prehod
a) odstranitev OM:
1) predhodni vnos vode. Ne jemljite mleka (z izjemo jedkih strupenih snovi) in etanola (z izjemo metanola).
2) bruhanje - indicirano predvsem v primeru zastrupitve z velikimi tabletami ali kapsulami, ki ne morejo preiti skozi sondo. Lahko se izzove zaradi refleksa ali bruhanja (NaCl: 1 žlica na 1 kozarec vode; Ipecakov sirup: odrasli 2 žlici, otroci 2 žlički; gorčica: 1-2 žlički na kozarec vode; apomorfin: 5-10 mg/kg subkutano, razen za otroke, mlajše od 5 let). Ne povzročajte bruhanja po zaužitju: organska topila - nevarnost vdihavanja, detergenti - penjenje, konvulzivne snovi - nevarnost aspiracije, jedke snovi - poškodbe požiralnika)
3) sonda izpiranje želodca - je nujen in obvezen ukrep. Želodec se opere, če od zastrupitve ni minilo več kot 4-6 ur, včasih tudi do 10 ur; v primeru zastrupitve z acetilsalicilno kislino - po 24 urah. Pacienta predhodno intubiramo s cevko z napihljivo manšeto: v komi brez kašlja in laringealnega refleksa. Želodec speremo z vodo ali fiziološko raztopino 30 ° C, postopek traja 4 ure ali več. Na koncu izpiranja - Aktivno oglje in natrijevega sulfata.
b) zmanjšanje absorpcije iz prebavil: aktivno oglje v notranjosti po praznjenju želodca + natrijev ali magnezijev sulfat. Značilnosti ukrepov za zmanjšanje absorpcije:
1) organska topila: ne povzročajte bruhanja, izpiranje želodca po intubaciji, aktivno oglje + tekoči parafin
2) detergenti: ne povzročajte bruhanja in izpirajte želodec, potrebno je dati veliko vode + sredstva proti penjenju (simetikon)
3) kisline in alkalije: bruhanja ni mogoče izzvati, izpiranje želodca skozi cevko, namazano z rastlinskim oljem po dajanju narkotičnega analgetika, je edina indikacija za dajanje mleka. Za zastrupitev s kislino - antacidi, za alkalno zastrupitev - citronska ali ocetna kislina.
III... Odstranitev absorbiranega OM iz telesa
a) prisilna diureza (pogoji: zadosten ledvični pretok krvi in glomerularna filtracija; vlijte 20-25 litrov v 24 urah)
b) peritonealna hemodializa
c) hemosorpcija
d) izmenjava transfuzije krvi
e) prisilna hiperventilacija
IV... Simptomatsko zdravljenje funkcionalnih motenj.
Protistrupi: 1) toksikotropni - vežejo, nevtralizirajo in preprečujejo absorpcijo OM: delujejo na principu aktivnega oglja, delujejo na kemično (unitiol, penicilamin, pentacin)
2) toksikokinetični - pospešujejo biotransformacijo OM (trimedoksim bromid, natrijev tiosulfat, etanol, AO)
3) farmakološki - atropin, nalokson
4) imunološki protistrupi
Unithiol, succimer - veže težke kovine, metaloide, srčne glikozide. Esmolol veže teofilin, kofein. Kalcijev trinatrijev pentotat - tvori komplekse z dvo- in trivalentnimi kovinami.
49. Recept in njegova struktura. Splošna pravila pisanje recepta. Državna ureditev pravil predpisovanja in izdajanja zdravil.
Recept- to je pisni poziv zdravnika farmacevtu z zahtevo po sprostitvi zdravila v določeni obliki in odmerku z navedbo načina njegove uporabe
V receptu se razlikujejo naslednji deli:
1. Inscriptio - naslov, napis. Tukaj so napisani datum izdaje recepta, priimek, začetnice in starost pacienta, priimek in začetnice zdravnika.
2. Invocatio - stik s farmacevtom. Izraža se z besedo "Recept" (vzemi) ali s kratico (Rp.)
3. Designatio materiarum - poimenovanje ali ime zdravil z navedbo njihovih odmerkov. V kompleksnem receptu je seznam zdravilnih snovi opravljen v določenem zaporedju. Prva je glavna zdravilna snov (osnova). Nato so napisani adjuvani. Nato so navedene sestavine, ki popravljajo okus, vonj, barvo zdravila (korigens). Zadnje pišejo snovi, ki dajejo zdravilu določeno dozirno obliko (constituens).
4. Subscriptio - recept (indikacija) farmacevtu. Označuje dozirno obliko, farmacevtske operacije, potrebne za njegovo izdelavo, število izdanih odmerkov zdravila.
5. Signatura - navodilo bolniku, kako uporabljati zdravilo.
6. Subscriptio medici - podpis zdravnika, ki je napisal recept, njegov osebni pečat.
Zdravnikova pritožba na farmacevta, ime zdravil, ki so vključena v recept, ime dozirne oblike in narava farmacevtskih operacij, so napisani v latinščina... Imena zdravil, botanična imena rastlin so zapisana z veliko začetnico. Recept za bolnika je napisan v ruskem ali nacionalnem jeziku.
Splošna pravila za predpisovanje:
1. Recept je napisan na posebnem obrazcu, odvisno od zdravila, ki se izpisuje, z jasnim rokopisom, s črnilom ali kemičnim svinčnikom brez popravkov.
2. Recept vsebuje datum, mesec, leto, priimek, ime, patronim in starost bolnika, priimek, ime in patronimik zdravnika. Nato sledi besedilo recepta, ki navaja imena snovi, ki so vključene v recept, v rodilniku in navaja njihovo količino.
3. Enota mase v receptih je gram ali ENOT.
4. Če je največji odmerek strupenih in močnih snovi presežen, se to potrdi z besedami
5. Recept je potrjen s podpisom in osebnim pečatom zdravnika
Republika Belorusija ima državno ureditev pravil za predpisovanje in izdajanje zdravil.
50. Pravila za predpisovanje strupenih, narkotičnih in močnih zdravil.
Seznam A vključuje zdravila, katerih imenovanje, uporabo, odmerjanje in shranjevanje je treba zaradi visoke toksičnosti izvajati zelo previdno. Isti seznam vključuje zdravila, ki povzročajo odvisnost od drog.
Seznam B vključuje zdravila, katerih imenovanje, uporabo, odmerjanje in shranjevanje je treba izvajati previdno v zvezi z možnimi zapleti pri njihovi uporabi brez zdravniškega nadzora.
Za strupena in močna zdravila so bili določeni največji višji enkratni in dnevni odmerki. Ti odmerki so za odrasle, starejše od 25 let. Pri ponovnem izračunu odmerkov za osebe, starejše od 60 let, starostna občutljivost na različne skupine LS. Odmerki zdravil, ki zavirajo centralni živčni sistem, pa tudi srčnih glikozidov in diuretikov se zmanjšajo za 50%, odmerki drugih strupenih in močnih zdravil se zmanjšajo na 2/3 odmerka za odrasle. Odmerki AB, sulfonamidov in vitaminov so običajno enaki za vse starostne skupine začenši pri 25 letih.
1. Narkotična zdravila (seznam A) so predpisana za obrazec na recept Obrazec 2. Ena oblika - eno zdravilo. Prisotni morajo biti: podpis in pečat lečečega zdravnika, podpis glavnega zdravnika zdravstvene ustanove, okrogel žig zdravstvene ustanove.
2. Na receptnem obrazcu obrazca 1 so predpisana strupena zdravila (seznam A), močna zdravila (seznam B). Na voljo mora biti podpis in osebni pečat zdravnika, pečat zdravstvene ustanove.
51. Zdravila pod nadzorom. Zdravila na recept.
Narkotične, strupene in močne droge so pod nadzorom (glejte razdelek 20)
A) Zdravila, ki niso registrirana v Republiki Belorusiji in niso odobrena za uradno uporabo
B) zdravila na zahtevo bolnikov in njihovih svojcev brez pregleda bolnika in postavitve diagnoze
C) recepti za narkotična zdravila za injekcije, anestetik eter, kloroetil, pentamin, fluorotan, natrijev oksibutirat v ampulah, litijev oksibutirat, barijev sulfat za fluoroskopijo.
52. Farmakokinetični modeli (enokomorni in dvokomorni), kvantitativni zakoni absorpcije in izločanja zdravil.
![]() Enokomorni model.
Enokomorni model.
Celoten organizem je ena sama homogena posoda. Predpostavke:
1) se vzpostavi hiter dinamičen razvoj med vsebnostjo zdravila v krvnem obtoku in njegovo koncentracijo v ekstravaskularnih tkivih
2) Zdravilo se hitro in enakomerno porazdeli po celotnem volumnu krvi
3) Izločanje zdravil je v skladu s kinetiko prvega reda: hitrost zmanjšanja vsebnosti zdravila v krvi je sorazmerna z njegovo koncentracijo
Če mehanizmi za izločanje zdravila (biotransformacija v jetrih, ledvično izločanje) z uvedbo terapevtskega odmerka niso nasičeni, bo graf sprememb plazemske koncentracije skozi čas prikazan logaritmično normalen linearna.
Nagib lognormalna os - Kel, kjer je Kel konstanta hitrosti izločanja in ima dimenzijo časa-1. Vrednost C0 dobimo z ekstrapolacijo grafa na presečišče z ordinatno osjo. Koncentracija zdravila v plazmi(Ct) kadar koli t po dajanju v telo je:
Ln Ct = Ln C0 - kt. Konstanta izločanja Kel, Vd in celotni očistek (CL) sta povezana z izrazom: CL = k × Vd
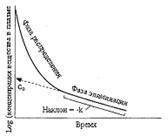 Dvokomorni model.
Dvokomorni model.
Pogosto po vstopu zdravila v telo ni mogoče hitro doseči ravnovesja med vsebnostjo zdravila v krvi in njegovo koncentracijo v ekstravaskularni tekočini. Potem se verjame, da je v agregatu tkiv in bioloških tekočin telesa mogoče razlikovati dve komori, ki se razlikujeta po stopnji dostopnosti za prodiranje zdravila. Osrednja komora vključuje kri (pogosto z intenzivno prekrvavimi organi - jetra, ledvice), periferna komora pa intersticijsko tekočino notranjih organov in tkiv.
Nastali graf prikazuje začetno Faza distribucije (Čas, potreben, da zdravilo doseže ravnotežno stanje med osrednjo in periferno komoro in naslednji počasni Faza eliminacije Prvo naročilo.
Vrednost C0, dobljena z ekstrapolacijo Faze izločanja pred prečkanjem ordinate. C0 se uporablja za izračun volumna porazdelitve in izločitvene konstante. Formule za izračun Ct in Cl, podane za enokomorni model, se uporabljajo tudi v fazi izločanja za zdravila, ki izpolnjujejo pogoje dvokomornega modela.
53. Selektivnost in specifičnost delovanja zdravila. Terapevtski, stranski in toksični učinki zdravil, njihova narava z vidika koncepta receptorjev. Terapevtska strategija za boj proti stranskim in toksičnim učinkom zdravil.
Posebnost- to je, ko se zdravilo veže na vrsto receptorja, ki je zanj strogo specifičen.
Selektivnost- to je, ko se zdravilo lahko veže na eno ali več vrst receptorjev natančneje kot druge.
Bolj zaželeno je uporabiti izraz selektivnost, saj je malo verjetno, da se katera koli molekula zdravila veže samo na eno vrsto receptorske molekule, saj je število potencialnih receptorjev pri vsakem bolniku astronomskega pomena.
Terapevtsko delovanje - glavni želeni farmakološki učinek, ki se pričakuje od danega farmakološkega pripravka.
Stranski učinki- tiste učinke, ki se pojavijo pri uporabi snovi v terapevtskih odmerkih in predstavljajo spekter njihovega farmakološkega delovanja.
Toksični učinki- neželeni učinki, ki se kažejo pri tem zdravilu, ko zapusti terapevtsko območje.
Razmerja med terapevtskimi in toksičnimi učinki zdravil na podlagi analize receptorsko-efektorskih mehanizmov:
1) terapevtski in toksični učinki, ki jih posreduje isti mehanizem receptor-efektor (prazosin deluje kot alfa-selektivni antagonist na vaskularne SMC receptorje in ima hipotenzivni učinek pri esencialni hipertenziji, vendar pri visokem odmerku lahko bolnik doživi posturalno hipotenzijo)
2) terapevtski in toksični učinki, ki jih posredujejo enaki receptorji, vendar različna tkiva ali različne efektorske poti (srčni glikozidi se uporabljajo za povečanje kontraktilnosti miokarda, hkrati pa motijo delovanje gastrointestinalnega trakta, vid zaradi blokade Na + / K + -ATPaza celične membrane)
3) terapevtski in toksični učinki, posredovani različni tipi receptorje (na primer norepinefrin ima hipertenzivni učinek preko a1-Ap, hkrati pa povzroča tahikardijo prek b1-Ap)
Terapevtska strategija za boj proti terapevtskim in stranskim učinkom zdravil:
1. Zdravilo je treba vedno dajati v najmanjšem odmerku, ki povzroči sprejemljiv terapevtski učinek
2. Zmanjšanje odmerka enega zdravila zaradi imenovanja drugega zdravila s podobnim učinkom, vendar prek različnih receptorjev in z drugačnim profilom toksičnosti.
3. Selektivnost delovanja zdravila lahko povečamo z nadzorovanjem koncentracije zdravila v predelu receptorjev različnih delov telesa (lokalna uporaba zdravil - inhalacijska uporaba salbutamola pri bronhialni astmi)
Podatke o času absorpcije, porazdelitve in izločanja, torej o farmakokinetiki zdravilnih učinkovin, lahko izrazimo matematično. To je potrebno pri načrtovanju režimov za klinično uporabo zdravil. Na podlagi farmakokinetičnih podatkov se razvijajo načela racionalne izbire in odmerjanja slednjih. Hkrati je poleg teh izračunov potrebno stalno klinično spremljanje delovanja zdravila, saj farmakokinetične študije le dopolnjujejo to kontrolo in omogočajo bolj objektivne zaključke.
Izločanje večine zdravilnih učinkovin poteka v skladu z eksponentno kinetiko, in sicer tako, da za vsako enako časovno obdobje iz telesa izgine konstanten del celotne količine dane zdravilne snovi. V večini primerov se hitrost, s katero zdravilo izgine iz telesa, odraža v ustrezni stopnji znižanja plazemskih ravni zdravila.
Koncentracijo zdravil v bioloških tekočinah določamo s tekočinsko ali plinsko-tekočinsko kromatografijo, radioimunskim testom ali encimsko analizo, polarografijo ali spektrofotometrijo. Ponavljajoče se določanje koncentracij zdravil v krvi med zdravljenjem imenujemo TERAPEVTSKI MONITORING. V ta namen se včasih uporablja slina, ki je ultrafiltrat krvi brez beljakovin.
Na podlagi dobljenih vrednosti se izriše graf, na abscisi katerega je označen čas vzorčenja, na ordinati pa koncentracija zdravila v biološkem vzorcu (najpogosteje v krvni plazmi) v ustreznih enotah. Nastala krivulja označuje farmakokinetične procese, ki se pojavljajo z zdravilom. Torej, po enkratni intravenski injekciji se koncentracija zdravila v plazmi eksponentno zmanjša. Hitrost eksponentnega procesa je mogoče označiti s konstanto hitrosti (K), ki odraža spremembo koncentracije na enoto časa ali skozi obdobje poleksponentnega procesa (označeno kot T 1/2 ali t / 2). To obdobje je enako času, ki je potreben za dokončanje postopka za 50%.
Izločanje zdravil iz telesa lahko presojamo po razpolovnem času ali razpolovnem času, razpolovnem času, razpolovnem času, ki je opredeljen kot čas, ko se koncentracija zdravila v krvi zmanjša za 50 % dane količine. zdravila ali izločanje 50 % biološko razpoložljive količine zdravila.
Izraz "OBDOBJE POL-ELIMINACIJE" je uspešnejši od "OBDJE POL-ELIMINACIJE", saj se zdravila ne samo izločajo, temveč tudi biotransformirajo. Razpolovni čas izločanja je mogoče določiti iz grafa koncentracija-čas z merjenjem časovnega intervala, v katerem se je katera koli koncentracija snovi na krivulji zmanjšala za polovico.
Praktično je pomembno zapomniti, da v eni razpolovni dobi
50 % zdravila se izloči iz telesa, 75 % v dveh obdobjih, 90 % v treh obdobjih, 94 % v štirih.
Ker je za popolno izločanje eksponentnega tipa potreben čas, daljši od štirih (4) razpolovnih časov, potem pri ponovnem dajanju zdravila v krajših intervalih opazimo njegovo kumulacijo (akumulacijo). Ocenjuje se, da so za dosego koncentracijskega platoja, torej stalne plazemske koncentracije zdravila, potrebna približno štiri obdobja biološke razpolovne dobe zdravila.
Pomembno je, da zmanjšanje izločanja zdravila povzroči podaljšanje biološke razpolovne dobe in podaljšanje delovanja zdravila.
Za nekatera zdravila je lahko farmakološko delovanje daljše, kot bi predlagal t/2. V zvezi s tem lahko zdravila, kot je rastni hormon, anaprilin, dajemo v intervalih, daljših od njihovega T / 2.
Da bi se izognili nevarnemu zvišanju plazemske koncentracije zdravila pri bolnikih z zmanjšanim izločanjem v primeru okvarjenega delovanja jeter, ledvic ali srčno-žilnega sistema, je treba vzdrževalne odmerke zmanjšati bodisi z zmanjševanjem vsakega odmerka bodisi s sorazmernim podaljšanjem intervalov med uporabo. za podaljšanje njihove biološke razpolovne dobe...
BIOLOŠKA RAZPOLOŽLJIVOST ZDRAVIL
Za zagotovitev terapevtskega učinka je treba zdravilno snov dostaviti v tiste organe ali tkiva, v katerih se izvaja njeno specifično delovanje (v biofazi). Z intravaskularno injekcijo zdravilo takoj in v celoti vstopi v krvni obtok. Pri drugih načinih dajanja (oralno, intramuskularno, subkutano itd.) mora zdravilo pred vstopom v krvni obtok preiti skozi številne biološke celične membrane (želodčna sluznica, jetrne celice, mišice itd.) in šele nato del nekega dela. vstopila bo v sistemski krvni obtok. Učinek zdravila je v veliki meri odvisen od tega, kolikšen del danega odmerka zdravila vstopi v sistemski krvni obtok. Ta indikator označuje biološko uporabnost sredstva (F). Tako v bistvu biološka uporabnost zdravila odraža njegovo koncentracijo na receptorjih, to je v krvi in telesnih tkivih po absorpciji. Seveda bo biološka uporabnost istega zdravila za vsakega bolnika različna. Očitno je pri intravenskem dajanju zdravila njegova biološka uporabnost približno 100 %, pri drugih načinih dajanja pa biološka uporabnost skoraj nikoli ne doseže 100 %.
Razlikujte med ABSOLUTNO IN RELATIVNO BIO RAZPOLOŽLJIVOST. Absolutna biološka uporabnost je delež absorbiranega zdravila med ekstravaskularnim dajanjem glede na njegovo količino po intravenski aplikaciji.
Pomemben kazalnik je RELATIVNA BIOLOŠKA RAZPOLOŽLJIVOST, ki določa relativno stopnjo absorpcije zdravila iz testnega zdravila in iz referenčnih zdravil. Z drugimi besedami, relativna biološka uporabnost je določena za različne serije zdravil, za zdravila ob menjavi
proizvodna tehnologija, za zdravila različnih proizvajalcev, za različne dozirne oblike. Za določitev relativne biološke uporabnosti se lahko uporabijo podatki o ravni zdravilne snovi v krvi ali njenem izločanju z urinom po enkratnem ali večkratnem dajanju. Ta izraz je pomemben pri primerjavi dveh zdravil med seboj.
Primerjalna biološka uporabnost istih zdravil različnih podjetij (primer: kokarboksinaza poljskega porekla in izdelana v Dnepropetrovsku) se določi s primerjavo kemičnih, bioloških in terapevtskih enakovrednosti.
KEMIJSKA EKVIVALENCA ni le naključje pri zdravilih kemična formula zdravil, ampak tudi naključje izomerizma, prostorske konfiguracije atomov v molekuli zdravila.
BIOLOŠKA EKVIVALENCA pomeni enako, enako koncentracijo učinkovine v krvi pri jemanju zdravila različnih podjetij.
Končno, TERAPEVTSKA EKVIVALENCA pomeni enak, enak terapevtski učinek.
Če so navedene 3 lastnosti enake, naj bi imela zdravila enako biološko uporabnost (biološka uporabnost). Trenutno obstaja veliko primerov, da so podobna zdravila biološko neenakomerna zaradi razlik v biološki uporabnosti. Zdravnik se mora tega spomniti, zlasti pri prenosu bolnika z enega zdravila na podobno zdravilo drugega podjetja.
Seveda na vsa ta vprašanja lahko odgovori le nova znanost – in sicer KLINIČNA FARMAKOLOGIJA. Je samostojna znanost s svojim predmetom in raziskovalnimi cilji. Zakaj je izstopal kot samostojen predmet? Najprej zato, ker, kot se je izkazalo, v poskusu na živalih ni mogoče preučiti vsega. Na primer duševni procesi, ki so zelo značilni samo za ljudi.
Hiter razvoj farmacevtske industrije je pripeljal do nastanka ogromnega števila zdravil. Pojavil se je plaz zdravil, ki je ustvarila nekakšno zdravilno džunglo. Trenutno stanje zelo otežuje izbiro pravega zdravila tudi v eni skupini zdravil, preprečuje, da bi se zdravnik orientiral na zdravilo, ki je optimalno za posameznega bolnika. Klinična farmakologija pomaga odgovoriti na vsa ta vprašanja.
Kot primer lahko navedemo možnost izbire zdravila za kolagenoze (bolezni vezivnega tkiva, revmatoidni artritis, revmatizem, sistemski eritematozni lupus itd.). Z enim
strani - acetilsalicilna kislina (aspirin), hkrati pa obstajajo tudi drugi sodobni nenarkotični analgetiki, ki imajo v primerjavi z aspirinom številne prednosti: naproksen, piroksikam itd.
Kaj je bolje, katero zdravilo bo primernejše za danega bolnika, katero daje najbolj izrazit terapevtski učinek? Klinična farmakologija pomaga odgovoriti na ta vprašanja.
Glavne naloge kliničnega farmakologa so:
1) Izbira zdravil za zdravljenje določene bolečine
2) Določitev najprimernejših zdravil zanj
oblike in način njihove uporabe.
3) Izbira načina dajanja zdravila.
4) Spremljanje učinka zdravila.
V ta namen so nameščeni senzorji, ki na monitorju dajejo stalno sliko koncentracije zdravila v krvi. Vsi drugi vidiki farmakokinetike se preučujejo.
5) Študija neželenih reakcij in stranskih učinkov na zdravila, njihovega izločanja ter preučevanje posledic medsebojnega delovanja zdravil pri posameznem bolniku.
6) Prenos nabranega znanja z usposabljanjem.
7) Organizacija laboratorija in informacijske storitve in nasveti o načrtovanju raziskav (WHO, 1971).
FARMAKODINAMIKA (PD) je veja farmakologije, ki preučuje
1) mehanizmi delovanja (to je bistvo procesov interakcije s tkivnimi, celičnimi ali subcelularnimi receptorji - specifičnimi ali nespecifičnimi) 1.
1 02) farmakološki učinki (to je vsebina in spremembe učinka zdravila glede na starost, spol bolnika, naravo in potek bolezni, sočasno patologijo), kot tudi 3) lokalizacijo zdravila dejanje. Skratka, PD lahko opredelimo kot vejo farmakologije, ki preučuje učinek zdravil na telo.
Običajno se mehanizem delovanja zdravila preučuje v poskusih na živalih, saj so pri živalih in ljudeh skoraj vedno enaki. Poznavanje mehanizma delovanja zdravila omogoča zdravniku, da inteligentno izbere potrebno zdravilo za zdravljenje.
Mehanizmov delovanja zdravil je veliko, vendar jih je mogoče pogojno omejiti na 2 skupini.
Prva skupina mehanizmov je povezana s tistimi primeri, ko zdravila delujejo na specifične receptorje - to so RECEPTORSKI MEHANIZMI.
Druga skupina mehanizmov je povezana z zdravili, ki zaradi svojih fizikalno-kemijskih lastnosti ne delujejo preko receptorjev. Tu lahko najprej navedemo učinek zdravil na specifične encime, njihov fizikalno-kemijski učinek na celične membrane in neposredno kemično interakcijo s celičnimi snovmi.
Primer nereceptorskih mehanizmov je
primer z zdravili za anestezijo, recimo s fluorotanom. Je odlično topilo za maščobe, zato deluje predvsem na membrane živčnih celic, kar povzroča farmakološki učinek - anestezijo.
Poglejmo glavne, najpogosteje najdene receptorje in mehanizme delovanja zdravil.
V farmakološkem smislu so receptorji funkcionalne biokemične makromolekularne membranske strukture, ki so selektivno občutljive na delovanje določenih kemičnih spojin, v našem primeru pa na delovanje zdravil. Raziskave V zadnjih letih pokazala, da so farmakološki receptorji beljakovine ali encimi (G-proteini so ena sama peptidna veriga s 7 domenami) - to je njihova temeljna razlika od morfoloških receptorjev.
Selektivna občutljivost zdravila na receptor pomeni dejstvo, da se zdravilo lahko, prvič, veže na receptor, torej ima afiniteto ali afiniteto zanj. Z drugimi besedami, afiniteta ali afiniteta se nanaša na sposobnost zdravila, da se veže na receptor.
Afiniteta ali afiniteta odraža kinetične konstante, ki vežejo zdravilo, receptor in odziv na molekularni ravni. Interakcija zdravilnih učinkovin z receptorjem vodi do pojava številnih biokemičnih in fizioloških sprememb v telesu, ki se izražajo v takšnem ali drugačnem učinku.
Druga značilnost zdravilne učinkovine je njena sposobnost, da povzroči farmakološki odziv, učinek po interakciji z receptorjem. Ta sposobnost se imenuje intrinzična aktivnost zdravila ali njegova učinkovitost. Do določene mere se biološki odziv uravnava s spreminjanjem števila receptorjev in njihove občutljivosti.
V teku evolucije so se oblikovali receptorji, občutljivi na različne endogene regulatorje. Po teoriji receptorjev je mehanizem delovanja zdravil spremeniti hitrost delovanja določenih telesnih sistemov, ko na receptorje delujejo naravni mediatorji ali eksogene snovi.
Zdravila, katerih delovanje je povezano z neposrednim vzbujanjem ali povečanjem funkcionalnih zmožnosti (zmožnosti) receptorjev, imenujemo AGONISTI, snovi, ki ovirajo delovanje specifičnih agonistov, pa ANTAGONISTI. Z drugimi besedami, če ima zdravilo obe značilnosti (to je tako afiniteto kot intrinzično aktivnost), potem je agonist. Zato je agonist snov z visoko afiniteto do receptorja in visoko intrinzično aktivnostjo. Če ima snov sposobnost samo vezave na receptor (to je, da ima afiniteto), vendar hkrati ne more povzročiti farmakoloških učinkov, potem povzroči blokado receptorja in se imenuje antagonist.
Zdravila, ki imajo enako afiniteto do receptorja kot agonist ali šibkejšo, vendar imajo manj izrazito intrinzično
aktivnosti imenujemo delni agonisti ali agonist-antagonist. Ta zdravila, ki se uporabljajo sočasno z agonisti, zmanjšajo učinek slednjih zaradi njihove sposobnosti, da zasedejo receptor.
Primer: atropin - ima večjo aktivnost kot acetilholin (endogeni mediator). Atropin deluje z receptorji, a ker nima notranje aktivnosti, ne bo povzročil fiziološkega učinka. Zaradi večje afinitete do receptorja v primerjavi z acetilholinom bo motil delovanje agonista, to je acetilholina, in bo zato njegov antagonist.
Zdravilne snovi lahko delujejo enako ali nasprotno endogenim mediatorjem. Če zdravilna snov deluje kot mediator (acetilholin, norepinefrin itd.), se taka snov imenuje MIMETIČNA. Mim - koren "mime", pantomima, mimika. Od tod holinomimetik, adrenergični agonist.
Zdravilo, ki preprečuje interakcijo mediatorja z receptorjem, se imenuje blokator (antiholinergik, adrenergični blokator, blokator histamina itd.).
V literaturi lahko najdete izraz "litični" (liza - raztapljanje, fizikalni proces). Izraz je precej star, vendar se včasih uporablja (antiholinergik, adrenolitik). Tako se izraza "litik" in "blokator" uporabljata izmenično.
V medicinski praksi se vse pogosteje uporablja hkratna uporaba več zdravil. Hkrati lahko medsebojno delujejo, spreminjajo resnost in naravo glavnega učinka, njegovo trajanje ali oslabijo stranske in toksične učinke. V zvezi s tem je poseben del farmakodinamike posvečen INTERAKCIJI ZDRAVIL, ki je razvrščen na naslednji način. Razlikujte FARMAKOLOŠKO interakcijo in FARMACEVTSKO interakcijo.
Farmacevtske interakcije so povezane s farmacevtsko nezdružljivostjo zdravil med njihovo proizvodnjo ali shranjevanjem, pa tudi pri mešanju v eni brizgi. V tem primeru se prej obstoječa farmakološka aktivnost zdravil zmanjša ali izgine, včasih pa se pojavijo celo nove, toksične lastnosti.
Farmakološka interakcija zdravil je povezana s spremembami njihove farmakokinetike, farmakodinamike ali temelji na kemičnih in fizikalno-kemijskih interakcijah v okoljih telesa. V tem primeru lahko zdravila medsebojno delujejo v kateri koli fazi prehoda skozi bolnikovo telo: med absorpcijo, v transportni fazi, v procesu presnove, pa tudi pri izločanju (farmakokinetična interakcija).
Farmakodinamična interakcija odraža spremembo, ki jo povzroči vsako zdravilo posebej, procesi, povezani z izvajanjem učinka. Z drugimi besedami, farmakodinamična vrsta interakcije temelji na posebnostih sprememb mehanizmov in lokalizacije delovanja uporabljenih zdravil, njihovih glavnih učinkih. Če interakcija poteka na receptorski ravni, potem gre predvsem za agoniste in antagoniste različnih vrst receptorjev. V tem primeru lahko ena zdravilna učinkovina okrepi ali oslabi učinek druge. Če je zdravilno ve
Snovi delujejo glede na učinek enosmerno – to so sinergijska zdravila (sin – skupaj, ergo – delo). Tako sinergizem spremlja povečanje končnega učinka. Običajno ta zdravila delujejo na iste receptorje. Obstajata 2 različici sinergije:
1) Učinki so enaki po principu preproste vsote. Povzeto (ali aditiv, - lat. - additio - dodatek). Učinek opazimo s preprostim dodajanjem učinkov vsake od komponent. Tako na primer delujejo zdravila za anestezijo (dušikov oksid + fluorotan). Različica aditivnega učinka je podobna pri hkratni uporabi aspirina in analgina. Zakaj morate to vedeti? Če je bolnik prisiljen jemati aspirin dlje časa, je treba upoštevati, da aspirin deluje ulcerogeno, to je, da povzroča razjede na sluznici prebavil, analgin pa ima tako neželen učinek, kot je zaviranje hematopoeze. Ob upoštevanju aditivnega analgetičnega učinka je mogoče zmanjšati brez bistvenega tveganja za njegov pojav, znatno zmanjšati odmerek obeh zdravil, ki jih jemlje bolnik.
2) Druga različica sinergije je potenciranje ali krepitev učinka. Ta možnost nastane, ko z vnosom dveh snovi skupni učinek preseže vsoto učinkov obeh učinkovin. Primer je interakcija antipsihotikov (aminazina) in anestetikov, interakcija antibiotikov in protimikrobnih sulfonilamidov.
Včasih se razlikuje tretja (3) varianta sinergizma - senzibilizacija. Senzibilizacija - ko eno zdravilo v minimalnem odmerku poveča učinek drugega v njihovi kombinaciji (uporaba majhnih odmerkov insulina v kombinaciji s KCl poveča raven prodiranja kalija v celice).
Poleg sinergije obstaja še fenomen antagonizma. Sposobnost ene snovi, da v takšni ali drugačni meri zmanjša učinek druge, se imenuje ANTAGONIZEM, torej v tem primeru eno zdravilo preprečuje delovanje drugega.
Obstajajo fizikalni, kemični in fiziološki antagonizmi. Ta vrsta interakcij se najpogosteje uporablja v primeru prevelikega odmerjanja ali akutne zastrupitve z zdravili. Primer FIZIČNEGA antagonizma lahko nakazuje sposobnost adsorpcijskih sredstev, da ovirajo absorpcijo snovi iz prebavnega trakta (aktivno oglje, adsorbirajoči strup na svoji površini; holestiramin).
Ilustracija KEMIJSKE interakcije je lahko tvorba kompleksonov (ioni nekaterih težkih kovin - živo srebro, svinec - vežejo penicilamin, EDTA) ali pa tako medsebojno delujeta želodčna klorovodikova kislina in natrijev bikarbonat (alkalija).
FIZIOLOŠKI antagonizem je povezan z interakcijami zdravil na ravni receptorjev, katerih narava je bila že omenjena zgoraj.
Po analogiji s sinergizmom ločimo NEPOSREDNI (ko obe zdravilni spojini delujeta na iste receptorje) in INDIREKTNI (različna lokalizacija delovanja zdravila) antagonizem. Po drugi strani pa je neposredni antagonizem KONKURENČEN in NE
KONKURENČNO. S konkurenčnim antagonizmom zdravilo vstopi v konkurenčno razmerje z naravnimi regulatorji (mediatorji) za vezavna mesta na specifičnih receptorjih. Blokada receptorjev, ki jo povzroča kompetitivni antagonist, se lahko razbremeni z visokimi odmerki agonista ali naravnega mediatorja.
Nekonkurenčni antagonizem je situacija, ko zdravilo ne more izpodriniti naravnega mediatorja iz receptorja, ampak z njim tvori kovalentne vezi (mediator).
TOČKE INTERAKCIJE ZDRAVILA Glavna
masa receptorjev se nahaja na zunanji in znotraj membrane celice in njenih organelov. Najpogostejše točke medsebojnega delovanja zdravil vključujejo: 1) mediatorje in hormonske receptorje; 2) ATP-faza Na / K črpalke, Ca, K in Na - intramembranski kanali.
Slednje še enkrat dokazuje, da zdravila delujejo na razpoložljive ključne mehanizme bioloških reakcij, torej na filogenetsko določene procese, in ne z ustvarjanjem novih reakcij.
Interakcija zdravil z receptorjem poteka na ravni kemičnih ali fizikalno-kemijskih procesov. Najpogosteje so narava reakcije, njena moč, reverzibilnost in trajanje posledica lastnosti povezave zdravila z receptorjem. Moč vezi je odvisna od razdalje elektrostatične interakcije med atomoma. Narava interakcije je praviloma zapletena, lahko vključuje različne vrste komunikacijo, ki jo določata komplementarnost zdravila in receptorja, stopnja njune konvergence med seboj.
Najšibkejše povezave so van der Waalsove (določite specifičnost interakcije snovi z reaktivnimi sistemi). V večini primerov med zdravilom in receptorjem nastanejo ionske vezi (reverzibilne).
VRSTE DELOVANJA ZDRAVILA
1) LOKALNI UČINEK - delovanje snovi, ki se pojavi na mestu njene aplikacije. Primer: uporaba lokalnih anestetikov - vnos raztopine dikaina v konjunktivno votlino. Uporaba 1% raztopine novokaina med ekstrakcijo
zob. Ta izraz (lokalno delovanje) je nekoliko poljuben, saj se resnično lokalno delovanje opazi zelo redko, saj se snovi lahko delno absorbirajo ali imajo refleksni učinek.
2) REFLEKTIVNO DELOVANJE - to je takrat, ko zdravilo deluje na poti refleksa, torej vpliva na ekstero- ali interoreceptorje, učinek pa se kaže s spremembo stanja bodisi ustreznih živčnih centrov bodisi izvršilnih organov. Torej uporaba gorčičnih ometov za patologijo dihal refleksno izboljša njihovo trofizem (eterično gorčično olje stimulira eksteroreceptorje kože). Zdravilo cytiton (respiratorni analeptik) vznemirljivo vpliva na kemoreceptorje karotidnega glomerula in z refleksno stimulacijo centra dihanja poveča volumen in frekvenco dihanja. Drug primer je uporaba amoniaka za omedlevico (amoniak), ki refleksno izboljša
možganska cirkulacija in tonični vitalni centri.
3) REZORPTIVNO DELOVANJE - to je, ko se po absorpciji (resorpcija - absorpcija; latinsko - resorbeo - absorbiram) razvije delovanje snovi, ki vstopi v splošni krvni obtok, nato v tkiva. Resorptivno delovanje je odvisno od načina dajanja zdravila in njegove sposobnosti prodiranja skozi biološke ovire. Če snov deluje samo s funkcionalno enotočkovnimi receptorji določene lokalizacije in ne vpliva na druge receptorje, se delovanje takšne snovi imenuje SELEKTIVNO. Torej nekatere kurariformne snovi (mišični relaksanti) precej selektivno blokirajo holinergične receptorje končne plošče, kar povzroča sprostitev skeletnih mišic. Delovanje zdravila prazosin je povezano s selektivnim blokiranjem postsinaptičnih alfa-on adrenergičnih receptorjev, kar na koncu vodi do znižanja krvnega tlaka. Osnova selektivnosti delovanja zdravil (selektivnosti) je afiniteta (afiniteta) snovi do receptorja, ki jo določata prisotnost določenih funkcionalnih skupin v molekuli teh snovi in splošna strukturna organizacija snovi. , kar je najbolj primerno za interakcijo s temi receptorji, torej POPOLNOST.
SPLOŠNA ZNAČILNOST UČINKA ZDRAVILA NA TELO
Kljub obilici zdravil, vseh ogromno
ki jih povzročajo v telesu, imajo določeno skupnost in
enotnost. Glede na koncept reakcijske hitrosti obstaja 5
vrste sprememb
povzročajo farmakološka sredstva (N.V. Vershinin):
1) toniranje (povečanje funkcije na normalno);
2) razburjenje (povečana funkcija nad normo);
3) pomirjujoč učinek (pomirjevalo), to je zmanjšanje povečane funkcije na normalno;
4) zatiranje (zmanjšanje funkcije pod normalno);
5) paraliza (prenehanje funkcije). Količina tonika in vozička
učinek prebujanja se imenuje prebujevalno dejanje.
GLAVNI UČINKI ZDRAVILA
Najprej je treba razlikovati med:
1) fiziološki učinki, ko zdravila povzročijo spremembe, kot so zvišanje ali znižanje krvnega tlaka, srčnega utripa itd.;
2) biokemični (povišane ravni encimov v krvi, glukoze
Shl itd.). Poleg tega obstajajo BASIC (ali glavni) in
SEKUNDARNI (manjši) učinki zdravil. OSNOVNI EF
DEJSTVO je tisto, na katerem zdravnik temelji svoje izračune pri zdravljenju tega (!) Bolnika (analgetiki - za analgetični učinek, antihipertenzivi - za zniževanje krvnega tlaka itd.).
POMEMBNI ali neglavni učinki, dodatni, sicer tisti, ki so neločljivi za to zdravilo, vendar njihov razvoj pri tem bolniku ni potreben (nenarkotični analgetiki - poleg analgetičnega učinka povzročajo antipiretični učinek, itd.). Neželeni učinki lahko vključujejo PREDNOSTI in NEŽELENE (ali NEŽELENE) učinke.
Primer. Atropin - sprošča gladke mišice notranjih organov
organov. Hkrati pa hkrati izboljša prevodnost v AV vozlišču srca (s srčnim blokom), poveča premer zenice itd. Vse te učinke je treba obravnavati posebej v vsakem posameznem primeru.
DEJAVNIKI, KI VPLIVAJO NA VREDNOST UČINKA ZDRAV
1) Najprej se morate spomniti farmakokinetičnih dejavnikov, ki so značilni za vsako zdravilo. To je bilo že omenjeno zgoraj, spomnim vas le, da govorimo o njegovi stopnji absorpcije oziroma absorpcije, biotransformacije, izločanja (zdravilo, zdravilo).
2) Druga skupina dejavnikov je fiziološka.
a) Starost. Dejansko se vsi dobro zavedajo, da se občutljivost pacienta na zdravila s starostjo spreminja. Tudi v tem pogledu so izstopali:
Perinatalna farmakologija;
Pediatrična farmakologija;
Geriatrična farmakologija;
Reproduktivna farmakologija;
b) Teža bolnika. Znano je, da večja kot je masa, višja je
odmerek. Zato se zdravila odmerjajo v (mg / kg).
c) Spol. Ugotovljena je različna občutljivost pri moških in ženskah
nekatere snovi, na primer nikotin, alkohol itd.,
kar je razloženo z razliko v presnovi, razliko v specifičnih
telesne maščobe itd.
c) Stanje organizma. Učinek zdravil na telo po su
socialno telesna aktivnost bo drugače kot brez njega.
e) Biološki ritmi (dnevni, mesečni, sezonski, letni
vye, zdaj pa celo prebivalstvo) imajo najbolj resne
vpliva na delovanje zdravil v telesu. 3) Patološka dejstva
ry (na primer raven hormonske aktivnosti). Torej z ba
toksične odmerke morfija se lažje prenašajo, poveča pa se občutljivost miokarda na adrenalin. 1 0 Vpliv srčnih glikozidov na krvni obtok se kaže le v ozadju srčnega popuščanja. Učinek zdravil se bistveno spremeni s hipo- in hipertermijo, z nalezljivimi boleznimi, s spremembo funkcionalnega stanja centralnega živčnega sistema itd.).
4) Genetski dejavniki. Znano je, da odsotnost encima glukoza-6-fosfat dehidrogenaze (G-6-FDG) pri talaseniji onemogoča predpisovanje antimalaričnih zdravil, kot je primakin. Pomanjkanje encima butirilholinesteraze v krvi, ki se pojavi pri enem od 2500 ljudi, je vzrok za dolgotrajno sprostitev mišic po dajanju ditilina.
5) Sugestivnost bolnikov ali placebo učinek. V zvezi s tem antianginalni učinek placebo zdravil na primer doseže 40 %, do 81 % placebo učinka pa izhaja iz načina injiciranja zdravila. Verjetno je prav zato v veliki meri posledica tega učinka uporaba vitaminskih pripravkov, tonikov, pomirjeval.
6) Odmerek zdravila. Učinek zdravil je v veliki meri odvisen od njihovega odmerka. Odmerek se nanaša na količino zdravilne snovi
enkratni odmerek (običajno imenovan enkratni odmerek). Odmerek zdravila ni odvisen le od učinkovitosti zdravljenja, ampak tudi od varnosti bolnika. Že ob koncu 18. stoletja je William Withering zapisal: "Strup v majhnih odmerkih - najboljše zdravilo; koristno zdravilo v prevelikem odmerku je strup.»To je še toliko bolj pravilno v našem času, ko so v medicinsko prakso uvedli izjemno aktivna zdravila, katerih odmerki se merijo v delcih miligrama.
Navedite odmerek v gramih ali delcih grama. Za natančnejše odmerjanje zdravil se njihova količina izračuna na 1 kg telesne teže (ali na 1 m² telesne površine), na primer 1 mg / kg; 1 μg / kg itd. Zdravnik se mora orientirati ne le v odmerku, izračunanem za enkratni odmerek (pro dosi), ampak tudi v dnevnem odmerku (pro die).
Najmanjši odmerki, pri katerih zdravila povzročijo začetni biološki (terapevtski) učinek, se imenujejo pragovi ali minimalni učinkoviti (terapevtski) odmerki. V praktična medicina najpogosteje se uporabljajo povprečni terapevtski odmerki, pri katerih zdravila zagotavljajo potreben optimalen farmakoterapevtski učinek. Če pri njihovem predpisovanju bolniku učinek ni dovolj izrazit, se odmerek poveča na najvišji terapevtski odmerek. Višji terapevtski odmerki so lahko enkratni in dnevni. Najvišji enkratni odmerek je največja količina zdravila, ki se lahko daje enkrat brez škode za bolnika. Ti odmerki se redko uporabljajo, v skrajnih primerih (v nujnih, nujnih primerih). Povprečni terapevtski odmerki so običajno 1 / 3-1 / 2 največjega enkratnega odmerka.
Najvišje terapevtske doze strupenih in močnih snovi so navedene v Državni farmakopeji ZSSR. V nekaterih primerih, na primer pri uporabi kemoterapevtskih sredstev, je odmerek zdravila indiciran za potek zdravljenja (tečajni odmerek). Če je treba hitro ustvariti visoko koncentracijo zdravila v telesu (sepsa, srčno-žilna odpoved), uporabite prvi odmerek, tako imenovani nakladalni odmerek, ki presega vse naslednje. Obstajajo tudi toksični (nevarni učinki) in smrtonosni odmerki.
Za zdravnika je pomembno, da pozna še eno značilnost - in sicer koncept širine terapevtskega delovanja zdravila. Širina terapevtskega delovanja se razume kot razdalja, razpon od najmanjšega terapevtskega odmerka do najmanjšega toksičnega odmerka. Seveda je večja kot je ta razdalja, varnejša je to zdravilo.
1/20 odmerka x starost otroka.
Za kvantitativne značilnosti in pri ocenjevanju učinkovitosti novega farmakološkega sredstva se praviloma uporabljata dve standardni primerjavi - bodisi s placebom bodisi z anal.
gic vrsta delovanja, ki je eno najučinkovitejših sredstev v tej skupini.
Placebo (slepka) je indiferentna snov v dozirni obliki, ki posnema določeno farmakološko ali zdravilo. Uporaba placeba je nujna ob prisotnosti: a) učinka domnevnosti, vpliva osebnosti, pričakovanj in pristranskosti s strani pacienta ali raziskovalca; b) spontane spremembe v poteku bolezni, simptomi, pa tudi pojavi, ki niso povezani z zdravljenjem.
Placebo je latinski izraz, ki pomeni "lahko ti ugodim."
Učinek placeba je učinek, ki ga ne povzročajo specifične farmakodinamične lastnosti zdravila za dano patologijo, temveč DEJSTVO UPORABE zdravil, ki vpliva psihično. Placebo zdravila so običajno farmakološko inertna in vsebujejo neaktivne snovi, kot sta škrob ali laktoza. V kliničnih preskušanjih se placebo uporablja za ugotavljanje učinka sugestije tako s strani bolnika kot zdravnika, še posebej, če je treba preučevati zdravila, namenjena zdravljenju bronhialne astme, hipertenzije, angine pektoris, koronarne bolezni. V takih primerih se placebo pripravek po barvi ali drugih fizikalnih lastnostih (vonj, okus, oblika) ne sme razlikovati od aktivnega pripravka. Placebo je učinkovitejši, če sta tako zdravnik kot bolnik o njem slabo obveščena.
PRIMER. Pri ishemični bolezni srca (IHD), če je eni skupini bolnikov z IHD predpisano aktivno zdravilo, drugi pa placebo, se pri 40% bolnikov v drugi skupini napadi angine ustavi.
Najbolj izrazit placebo učinek (do 81%) je opažen pri načinu injiciranja. Napitki in tablete so manj učinkoviti.
Izraz FARMAKOTERAPIJA (FT) se pogosto uporablja v literaturi o izpostavljenosti bolnika zdravilu. Farmakoterapija je del farmakologije, ki preučuje zdravljenje z zdravili pri bolniku.
Obstajajo naslednje vrste farmakoterapije:
1) ETIOTROPNA - idealna oblika farmakoterapije. Ta vrsta FT je namenjena odpravi vzroka bolezni. Primeri etiotropne PT so lahko zdravljenje nalezljivih bolnikov s protimikrobnimi sredstvi (benzilpenicilin za streptokokno pljučnico), uporaba antidotov pri zdravljenju bolnikov s toksičnimi
snovi. 2) PATOGENETSKA FARMAKOTERAPIJA - usmerjena
odpraviti oz
zatiranje mehanizmov razvoja bolezni. Večina trenutno uporabljenih zdravil spada prav v skupino zdravil patogenetske FT. Antihipertenzivi, srčni glikozidi, antiaritmična, protivnetna, psihotropna in mnoga druga zdravila imajo terapevtski učinek z zatiranjem ustreznih mehanizmov razvoja bolezni.
3) SIMPTOMATSKA TERAPIJA – usmerjena v odpravo oz
omejitev posameznih manifestacij bolezni. Simptomatska zdravila vključujejo zdravila proti bolečinam, ki ne vplivajo na vzrok ali mehanizem bolezni. Antitusiki so tudi dober primer simptomatskih zdravil. Včasih ta zdravila (odstranitev sindrom bolečine z miokardnim infarktom) lahko pomembno vpliva na potek glavnega patološkega procesa in hkrati igra vlogo sredstev patogenetske terapije.
4) SUBSTITUCIONALNA FARMAKOTERAPIJA se uporablja v primeru pomanjkanja naravnih hranil. Sredstva za nadomestno zdravljenje vključujejo encimske pripravke (pankreatin, panzinorm itd.), Hormonska zdravila (inzulin za diabetes mellitus, tiroidin za miksedem), vitaminske pripravke (vitamin D, na primer za rahitis). Zdravila za nadomestno zdravljenje, ne da bi odpravili vzroke bolezni, lahko zagotovijo normalen obstoj telesa več let. Ni naključje, da je tako huda patologija kot sladkorna bolezen- velja za poseben življenjski slog med Američani.
5) PREVENTIVNA TERAPIJA se izvaja za preprečevanje bolezni. Profilaktična zdravila vključujejo nekatera protivirusna sredstva (na primer med epidemijo gripe - remantadin), razkužila in številna druga. Uporaba protituberkuloznih zdravil, kot je izonizid, se lahko šteje tudi za profilaktično FT. Cepiva so dober primer preventivne terapije.
KEMOTERAPIJO je treba ločiti od farmakoterapije. Če FT obravnava dva udeleženca patološkega procesa, in sicer zdravilo in makroorganizem, potem so med kemoterapijo že 3 udeleženci: zdravilo, makroorganizem (bolnik) in povzročitelj bolezni.
Ko smo že pri odmerkih, smo izpostavili predvsem alopatske odmerke, v nasprotju s homeopatskimi. Zato nekaj besed o HOMEOPATIJI. Izraz "homeopatija" izhaja iz dveh grških besed: homois - podobno in pathos - trpljenje, bolezen. Dobesedno je homeopatija prevedena kot podobna, podobna bolezen. Ustanovitelj homeopatije, nemški znanstvenik Samuel Hahnemann, je v svojem znana knjiga"Orgaon medicinske umetnosti ali osnovna teorija homeopatskega zdravljenja" nazaj v začetek XIX stoletja (1810) začrtal temeljna načela te znanosti. Obstaja več načel, vendar sta 2 osnovni:
1) To je zakon podobnosti, ki pravi, da je treba zdravljenje bolezni izvajati s podobnimi, podobnimi sredstvi. Po tem načelu Hahnemann svetuje »posnemati naravo, ki včasih ozdravi kronično bolezen prek druge spremljajoče bolezni«. Zato je treba "proti bolezni, ki jo je treba pozdraviti (predvsem kronične), uporabiti takšno zdravilno snov, ki lahko povzroči drugo, najbolj podobno umetno bolezen, prva pa bo ozdravljena." Similia
similibus (tako kot podobno). Na primer, zlatenico je treba zdraviti z rumeno itd.
2) Drugo načelo je zdravljenje z zelo majhnimi odmerki. Razredčitve zdravil, ki jih uporabljajo homeopati, se izračunajo v več vrstnih redih velikosti, včasih jih dosežejo na desetine: 10 v peti; 10 v desetem; 10 na osemnajsto ali več potenco (to je milijon
in več kot delček gramov). Za razlago učinka uporabe le
ogljikovih hidratov v
visoke razredčitve Hahnemann je predstavil spekulativni koncept: "Majhne odmerke odlikuje posebna duhovna moč, večja aktivnost, sposobnost prodiranja v prizadete organe in tkiva."
Ni znano, kaj je s posebno duhovno močjo, ampak znanstveno življenje v zadnjem desetletju je predstavila zelo močne dokaze za veljavnost Hahnemannove izjave. Tako so na primer poskusi Francoza Jacquesa Bekvenista, ki jih je naredil z razredčitvijo snovi 10 na osemdeseto potenco, pokazali, da imajo molekule vode "spomin" na prisotnost določene snovi, kar povzroča določen fiziološki učinek. Če bo to v bližnji prihodnosti opaženo dejstvo našlo potrditev, torej če bo ugotovljeno, ali so molekule vode vir informacij, bomo zagotovo v osnovi največje odkritje, ki lahko razloži terapevtsko učinkovitost homeopatskih zdravil.
Nato razmislite o poglavju, ki se nanaša na FARMAKOLOŠKE VIDIKE STRUPNEGA UČINKA ZDRAV, in sicer TOKSIKOLOGIJA ZDRAV. Toksikologija zdravil je veja farmakologije, ki preučuje toksične učinke teh zdravil. Vendar je zdaj bolj pravilno govoriti o neželenih reakcijah človeškega telesa na zdravila. To dejstvo je znano že dolgo, nabralo se je ogromno dejstev, ki kažejo, da se pri jemanju skoraj vseh zdravil lahko pojavijo neželene reakcije različne stopnje.
Obstaja veliko klasifikacij stranskih učinkov zdravil in zapletov farmakoterapije, čeprav nobena ni popolna. Hkrati pa lahko na podlagi patogenetskega načela vse neželene učinke ali reakcije razdelimo na 2 vrsti:
1) neželeni učinki, povezani z
a) prevelik odmerek zdravila
b) zastrupitev;
2) toksične reakcije, povezane s farmakološkimi lastnostmi zdravil.
Preveliko odmerjanje se običajno pojavi pri uporabi velikih odmerkov zdravil. Še posebej pogosto pride do prevelikega odmerjanja pri jemanju zdravil z majhno širino terapevtskega delovanja. Na primer, toksičnosti se je težko izogniti pri uporabi aminoglikozidnih antibiotikov (streptomicin, kanamicin, neomicin). Ta zdravila povzročajo vestibularne motnje in gluhost, če jih zdravimo v odmerkih, ki niso veliko višji od terapevtskih. Pri nekaterih zdravilih se je preprosto nemogoče izogniti toksičnim zapletom (antineoplastika, citotoksična zdravila), ki poškodujejo vse hitro delečeče se celice in
Inertni možgani ne izginejo, hkrati pa učinkovito vplivajo na rast tumorskih celic.
Poleg tega je preveliko odmerjanje lahko povezano ne le z uporabo velikih odmerkov, temveč tudi s pojavom kumulacije (srčni glikozidi).
Zastrupitev je lahko naključna ali namerna. Namerna zastrupitev se običajno pojavi s samomorilnim ciljem (samomor). V regiji Omsk so najpogosteje v splošni strukturi zastrupitve zastrupitve s tekočinami za kauterizacijo, na drugem mestu so zastrupitve z zdravili. To so najprej zastrupitve s uspavalnimi tabletami, pomirjevali, FOS, alkoholom, ogljikovim monoksidom.
Kljub razliki v etioloških dejavnikih so ukrepi pomoči na stopnjah zdravstvene pomoči v osnovi podobni.
Ta načela so naslednja:
1) BOJ Z NEOPLJENIM STRUPOM IZ PREBAVLEČNEGA TRAKTA. Najpogosteje je to potrebno za peroralno zastrupitev s strupom. Najpogostejša akutna zastrupitev je posledica zaužitja snovi. Obvezen in nujen ukrep v zvezi s tem je izpiranje želodca skozi cev tudi 10-12 ur po zastrupitvi. Če je bolnik pri zavesti, se opravi izpiranje želodca z uporabo velike količine vode in naknadna indukcija bruhanja. Bruhanje se sproži mehansko. V nezavestnem stanju se bolniku opravi izpiranje želodca skozi cev. Treba je usmeriti prizadevanja za adsorbcijo strupa v želodcu, za kar se uporablja aktivno oglje (1 žlica v notranjosti ali 20-30 tablet hkrati, pred in po izpiranju želodca). Želodec po 3-4 urah večkrat speremo, dokler se popolnoma ne očisti iz snovi.
Bruhanje je kontraindicirano v naslednjih primerih:
S komo;
V primeru zastrupitve z jedkimi tekočinami;
V primeru zastrupitve s kerozinom, bencinom (možnost hidrokarbonatne pljučnice z nekrozo pljučnega tkiva itd.).
Če je žrtev majhen otrok, je za pranje bolje uporabiti fiziološke raztopine v majhnih količinah (100-150 ml).
Najbolje je odstraniti strup iz črevesja s slanimi odvajali. Zato lahko ob koncu izpiranja v želodec vnesemo 100-150 ml 30-odstotne raztopine natrijevega sulfata, še bolje pa magnezijevega sulfata. Slana odvajala so najmočnejša, hitro delujoča odvajala v celotnem črevesju. Njihovo delovanje je podrejeno zakonom osmoze, zato so kratko obdobječas, se delovanje strupa ustavi.
Dobro je dajati adstringente (raztopine taninov, čaj, ptičja češnja), pa tudi obloge (mleko, jajčni beljak, rastlinsko olje).
V primeru stika s kožo s strupom je potrebno kožo temeljito sprati, po možnosti z vodo iz plute. Če strupene snovi vstopijo skozi pljuča, je treba njihovo vdihavanje ustaviti tako, da žrtev odstranimo iz zastrupljenega ozračja.
Pri subkutanem injiciranju strupene snovi lahko njeno absorpcijo z mesta injiciranja upočasnimo z injekcijami raztopine adrenalina.
okoli mesta injiciranja, pa tudi hlajenje tega predela (led na koži na mestu injiciranja).
2) Drugo načelo pomoči pri akutni zastrupitvi je vplivanje na absorbirani strup, ODSTRANITEV IZ TELA.
Da bi strupeno snov čim prej odstranili iz telesa, se najprej uporablja prisilna diureza. Bistvo te metode je v kombinaciji povečane obremenitve vode z uvedbo aktivnih, močnih diuretikov. Telo preplavimo z obilico tekočine bolniku ali z intravenskim injiciranjem različnih raztopin (raztopine krvnih nadomestkov, glukoze ipd.). Od diuretikov se najpogosteje uporablja FUROSEMIDE (lasix) ali MANIT. Z metodo prisilne diureze nekako "speremo" pacientova tkiva in jih osvobodimo strupenih snovi. Ta metoda uspe odstraniti le proste snovi, ki niso povezane z beljakovinami in krvnimi lipidi. Pri uporabi je treba upoštevati ravnovesje elektrolitov ta metoda se lahko poslabša zaradi izločanja znatne količine ionov iz telesa.
Pri akutni srčno-žilni odpovedi, hudi ledvični disfunkciji in tveganju za nastanek možganskega ali pljučnega edema je prisilna diureza kontraindicirana.
Poleg prisilne diureze se uporabljata hemodializa in peritonealna dializa, ko kri (hemodializa ali umetna ledvica) prehaja skozi polprepustno membrano in se osvobodi strupenih snovi ali se izvaja "spiranje" peritonealne votline z raztopino elektrolita. .
IZVENTELESNE METODE razstrupljanja. Uspešna metoda razstrupljanja, ki je postala zelo razširjena, je metoda HEMOSORPCIJE (limfosorpcija). V tem primeru se strupene snovi v krvi adsorbirajo na posebnih sorbentih (zrnati ogljik, prevlečen s krvnimi beljakovinami, alo vranica). Ta metoda omogoča uspešno razstrupljanje telesa v primeru zastrupitve z nevroleptiki, pomirjevali, FOS itd. Metoda hemosorpcije odstranjuje snovi, ki se slabo odstranijo s hemodializo in peritonealno dializo.
NADOMESTENJE KRVI se uporablja, kadar se krvavitev kombinira s transfuzijo krvi dajalca.
3) Tretje načelo boja proti akutnim zastrupitvam je RAZVARANJE POSESNEGA STRUPA z uvedbo ANTAGONISTOV in ANTIDOTOV.
Antagonisti se pogosto uporabljajo pri akutni zastrupitvi. Na primer, atropin za zastrupitev z antiholinesterazo, FOS; nalorfin - v primeru zastrupitve z morfinom itd. Običajno farmakološki antagonisti kompetitivno medsebojno delujejo z istimi receptorji kot snovi, ki so povzročile zastrupitev. V zvezi s tem se zdi zelo zanimivo ustvarjanje SPECIFIČNIH PROTITELES (monoklonskih) v odnosu do snovi, ki so še posebej pogosto vzrok za akutne zastrupitve (monoklonska protitelesa proti srčnim glikozidom).
Za specifično zdravljenje bolnikov s kemično zastrupitvijo je učinkovita ANTIDODNA TERAPIJA. ANTIDOTI so sredstva, ki se uporabljajo za specifično vezavo strupa, nevtralna
lizanje, inaktiviranje strupov, bodisi s kemično ali fizično interakcijo.
Torej, v primeru zastrupitve s težkimi kovinami se uporabljajo spojine, ki z njimi tvorijo nestrupene komplekse (na primer unitiol za zastrupitev z arzenom, D-penicilamin, desferal za zastrupitev s pripravki železa itd.).
4) Četrto načelo je izvajanje SIMPTOMATSKE TERAPIJE. Še posebej velik pomen simptomatsko terapijo pridobimo v primeru zastrupitve s snovmi, ki nimajo posebnih protistrupov.
Simptomatsko zdravljenje podpira vitalne funkcije: CIRKULACIJA in DIHANJE. Uporabljajo srčne glikozide, vazotonike, sredstva za izboljšanje mikrocirkulacije, kisikovo terapijo in stimulanse dihanja. Konvulzije se odpravijo z injekcijami sibazona. Pri cerebralnem edemu se izvaja dehidracijsko zdravljenje (furosemid, manitol). uporabite analgetike, popravite kislinsko-bazično stanje krvi. Ko se dihanje ustavi, se bolnik prenese na umetno prezračevanje pljuč s kompleksom ukrepov za oživljanje.
Nato se bomo osredotočili na DRUGO VRSTO NEŽELENIH UČINKOV, torej na neželene učinke, povezane s farmakološkimi lastnostmi zdravil. Neželeni učinki zdravil se kažejo pri 10-20% ambulantnih bolnikov, 0,5-5% bolnikov pa potrebuje hospitalizacijo za odpravo motenj zdravil. Te nezaželene z vidika patogeneze so lahko: a) NEPOSREDNE in b) povezane s SPREMENJENO OBČUTLJIVOSTjo bolnikovega telesa.
Poglejmo DIREKTNE STRUPENE REAKCIJE. Imenujejo se neposredni, ker so zdravila neposredno, neposredno strupena za funkcionalni sistem. Na primer, antibiotiki iz serije aminoglikozidov (streptomicin, kanamicin, gentamicin) kažejo NEVROTOKSIČNOST, ki imajo toksični učinek na slušni organ (ototoksičnost) in vestibularni aparat. Poleg tega ta razred antibiotiki imajo toksičnost glede na vedenjske reakcije, ki se kažejo z letargijo, apatijo, letargijo, zaspanostjo.
Zdravila imajo lahko DIREKTNE GLATOTOKSIČNE REAKCIJE. Na primer, fluorotan (anestetik) ima lahko ob večkratni uporabi v kratkem času izrazit toksični učinek do akutne rumene jetrne distrofije.
Neposredne toksične učinke lahko dosežemo z NEFROTOKSIČNOSTM. Ta učinek imajo micinski antibiotiki-aminoglikozidi. Pri predpisovanju zdravil te serije bolnik potrebuje stalni nadzor za stanje preiskav urina (beljakovine, kri v urinu itd.).
Naslednji neposredni toksični učinek je ULTSEROGEN (ulcerativen). Na primer, predpisovanje salicilatov, glukokortikoidov, antihipertenzivnega sredstva rezerpin - vodi do razjede želodčne sluznice, kar je treba upoštevati pri predpisovanju teh razredov zdravil, zlasti pri bolnikih, ki že trpijo za peptično ulkusno boleznijo.
Neposredni toksični učinki se lahko izrazijo z EMBRIOTOKSIČNOST. Naj vas spomnim, da je neugodna
učinek zdravil, ki ni povezan s kršitvijo organogeneze, ki se pojavi pred 12 tednom nosečnosti. In toksični učinek zdravil je več pozno obdobje nosečnost se imenuje FETOTOKSIČNA. Na ta učinek se je treba spomniti pri predpisovanju zdravil nosečnicam, ki izvajajo farmakoterapijo zanje le ob strogih indikacijah.
Primeri: 1) imenovanje streptomicina nosečnicam lahko povzroči gluhost pri plodu (poškodba VIII para lobanjskih živcev); 2) tetraciklini negativno vplivajo na razvoj kosti pri plodu; 3) pri materi, ki trpi za morfinom, je novorojenček lahko tudi fizično odvisen od morfija.
Zdravila imajo lahko TERATOGENIČNOST, torej tako škodljiv učinek na diferenciacijo tkiv in celic, kar vodi v rojstvo otrok z različnimi anomalijami. Na primer, uporaba talidomida, ki ima izrazit teratogen učinek, kot pomirjevala in hipnotika, je privedla do rojstva v državah. Zahodna Evropa več tisoč otrok z različnimi deformacijami (fokomelija - plavuti podobni udi; amelija - odsotnost udov; obrazni hemangiji, gastrointestinalne anomalije).
Za preučevanje teratogenega učinka snovi se raziskuje učinek zdravil na živali, čeprav ni neposredne povezave z vplivom zdravil na živali in ljudi. Na primer, pri istem talidomidu je bila teratogenost v poskusu na miših razkrita pri odmerku 250-500 mg / kg telesne mase, pri ljudeh pa je bila enaka 1-2 mg / kg.
Najbolj nevarno glede teratogenega delovanja je prvo trimesečje (zlasti obdobje 3-8 tednov nosečnosti), to je obdobje organogeneze. V teh obdobjih je še posebej enostavno povzročiti hudo anomalijo v razvoju zarodka.
Pri ustvarjanju novih zdravil je treba upoštevati tudi možnost tako resnih negativnih učinkov, kot sta KEMIJSKA MUTAGENOST in KARCINOGENOST. MUTAGENCIJA je sposobnost snovi, da povzročijo trajne poškodbe zarodne celice, predvsem pa njenega genetskega aparata, kar se kaže v spremembi genotipa potomca. KARCINOGENOST je sposobnost snovi, da povzročijo nastanek malignih tumorjev. Estrogeni prispevajo k razvoju raka dojke pri ženskah v rodni dobi.
Mutageni in teratogeni učinki se lahko pojavijo mesece ali celo leta pozneje, zaradi česar je težko ugotoviti njihovo pravo delovanje. Teratogenost je značilna za antineoplastična zdravila, kortikosteroide, androgene, alkohol. Ciklofosfamid in nekatera hormonska sredstva imajo rakotvorni učinek.
Neželeni učinki pri jemanju zdravil se lahko izrazijo z razvojem ODVISNOSTI ZDRAVILA ali, bolj globalno, z ZDRAVLJENOSTJO. Obstaja več glavnih znakov odvisnosti.
1) To je prisotnost DUŠEVNE ODVISNOSTI, to je stanje, ko bolnik razvije neustavljivo duševno privlačnost do ponavljajočega se dajanja zdravilne snovi, npr.
droga.
2) FIZIČNA ODVISNOST - ta izraz označuje prisotnost hude telesne bolezni pri bolniku brez ponovnega injiciranja zdravila, zlasti zdravila. Z nenadnim prenehanjem jemanja zdravila, ki je povzročilo odvisnost od drog, se razvije pojav ODKRIVLJENJA ali ABSTINENCE. Pojavijo se strah, tesnoba, melanholija, nespečnost. Morda se pojavi motorični nemir, agresivnost. Številne fiziološke funkcije so motene. V hudih primerih so lahko odtegnitveni simptomi usodni.
3) Razvoj strpnosti, torej odvisnosti. Druge vrste
Neželeni učinki, ki jih povzročajo lastnosti samih zdravil, so motnje, povezane s premiki v bolnikovem imunobiološkem sistemu pri jemanju visoko aktivnih zdravil. Na primer, uporaba antibiotikov širokega spektra se lahko kaže s spremembo normalne bakterijske flore telesa (črevesja), ki se uresniči z razvojem superinfekcije, disbioze, kandidoze. Najpogosteje so v te procese vključena pljuča in črevesje.
Terapija s kortikosteroidi in imunosupresivna terapija oslabita imunski sistem, kar ima za posledico povečano tveganje za razvoj nalezljivih bolezni, predvsem oportunistične narave (pnevmocistoza, citomegalovirus itd.).
Ta podskupina reakcij je dveh vrst:
1) ALERGIJSKE REAKCIJE;
2) Idiosinkrazija. Treba je reči, da negativni vplivi
v povezavi z
kemične reakcije so v medicinski praksi zelo pogoste. Njihova pogostost se ves čas povečuje. Pojavijo se ne glede na odmerek danega zdravila, pri njihovem nastanku pa sodelujejo imunski mehanizmi. Alergijske reakcije so lahko 2 tipa: PREOBČUTLJIVOST TAKŠNEGA TIPA, GNT - povezana s tvorbo protiteles razredov IgE in IgG4) in POČASNE (kopičenje senzibiliziranih T-limfocitov in makrofagov) vrste.
Klinična slika je zelo raznolika: urtikarija, kožni izpuščaji, angioedem, serumska bolezen, bronhialna astma, zvišana telesna temperatura, hepatitis itd. Toda glavna stvar je možnost razvoja anafilaktičnega šoka. Če sta za razvoj alergijske reakcije potrebna vsaj dva stika bolnika z zdravilno snovjo, potem je razvoj IDIOSINKRAZIJE - intolerance na zdravilne snovi ob začetnem stiku s ksenobiotikom vedno povezan z nekakšno GENETSKO OKVARO, ki se običajno izraža z odsotnost ali izjemno nizka aktivnost encima. Na primer, uporaba antimalarnega zdravila primaquine pri posameznikih z genetsko encimopatijo (pomanjkanje akt. G-6-FDG) povzroči nastanek kinona, ki ima hemolitični učinek. V prisotnosti te fermentopatije je nevarno predpisovanje zdravil, ki so oksidanti, saj lahko to povzroči hemolizo.
eritrociti, hemolitična anemija (aspirin, kloramfenikol, kinidin, primakin, furadonin).
NEKAJ BESEDI O USTVARJANJU NOVIH ZDRAV, VREDNOTENJU ZDRAVIL IN NJIHOVI NOMENKLATURI. Za napredek farmakologije je značilno nenehno iskanje in ustvarjanje novih zdravil. Ustvarjanje zdravil se začne z raziskavami kemikov in farmakologov, katerih ustvarjalno sodelovanje je nujno pri odkrivanju novih zdravil. Hkrati se iskanje novih sredstev razvija v več smereh.
Glavni način je KEMIJSKA sinteza zdravil, ki se lahko izvaja v obliki DIREKTNE sinteze ali pa EMPIRIČNO. Če je usmerjena sinteza povezana z razmnoževanjem biogenih snovi (inzulin, adrenalin, norepinefrin), nastajanjem antimetabolitov (PABA-sulfonamidi), modifikacijo molekul spojin z znano biološko aktivnostjo (sprememba strukture acetilholina - gongliobakterja). higronija) itd., potem je empirična pot sestavljena bodisi iz naključnih najdb ali iskanja s presejanjem, to je presejanjem različnih kemičnih spojin za farmakološko aktivnost.
Eden od primerov empiričnih ugotovitev je lahko primer oviranja hipoglikemičnega učinka pri uporabi sulfonamidov, kar je nato privedlo do nastanka sintetičnih sulfonamidnih perforalnih antidiabetikov (butamid, klorpropamid).
Zelo naporna je tudi druga varianta empiričnega načina ustvarjanja zdravil, PRESIJALNA METODA. Vendar je neizogibno, še posebej, če se raziskuje nov razred kemičnih spojin, katerih lastnosti je glede na strukturo težko napovedati (neučinkovit način). In tu igra informatizacija znanstvenih raziskav v današnjem času ogromno vlogo.
Trenutno se zdravila pridobivajo predvsem s ciljno kemično sintezo, ki jo je mogoče izvesti a) s podobnostjo (uvedba dodatnih verig, radikalov) b) s komplementarnostjo, torej skladnostjo s katerim koli receptorjem tkiv in organov.
V arzenalu mamil, poleg sintetičnih drog, pomembno mesto zasedajo pripravki in posamezne snovi iz zdravilnih surovin rastlinskega ali živalskega izvora, pa tudi iz različnih mineralov. To so predvsem galenska, novogalenska zdravila, alkaloidi, glikozidi. Tako se iz opija pridobivajo morfin, kodein, papaverin, iz serpentina serpentina pridobiva rezerpin, iz lisičarke pa se pridobivajo srčni glikozidi – digitoksin, digoksin; iz številnih endokrinih žlez goveda - hormoni, imunoaktivna zdravila (insulin, tiroidin, taktivin itd.).
Nekatera zdravila so odpadni produkti gliv in mikroorganizmov. Primer so antibiotiki. Zdravilne snovi rastlinskega, živalskega, mikrobnega, glivičnega izvora pogosto služijo kot osnova za njihovo sintezo, pa tudi za kasnejše kemične preobrazbe in proizvodnjo polsintetičnih in sintetičnih zdravil.
Hitrost razvoja zdravil z uporabo pridobiva na zagonu
razvoj metod genskega inženiringa (inzulin itd.).
Novo zdravilo, ki je prešlo skozi vsa ta "sita" (študija farmakološke aktivnosti, farmakodinamike, farmakokinetike, študija stranskih učinkov, toksičnosti itd.), je dovoljeno za klinična preskušanja. Uporablja metodo "slepo kontrolo", placebo učinek, metodo dvojne "slepe kontrole", ko niti zdravnik niti bolnik ne vedo, kdaj je ta placebo uporabljen. Ve samo posebna komisija. Klinična preskušanja se izvajajo na ljudeh, v mnogih državah pa na prostovoljcih. Tu je seveda veliko pravnega, deontološkega, moralni vidiki problemi, ki zahtevajo njihov jasen razvoj, ureditev in potrditev zakonov v zvezi s tem.
NOMENKLATURA ZDRAVIL
Številna zdravila z eno učinkovino lahko poimenujemo po njih kemična struktura... Toda zaradi velike zapletenosti njihovega pomnjenja in neprijetnosti njihove uporabe se kemična imena v medicinski praksi ne uporabljajo.
Trenutno se za označevanje zdravil uporabljata dve vrsti imen:
1) NEPAtentirane mednarodne, ki jih odobrijo uradni zdravstveni organi in se uporabljajo v nacionalnih in mednarodnih farmakopejah;
2) KOMERCIALNE ali blagovne znamke, ki so komercialna lastnina farmacevtskih podjetij. Poleg tega ima lahko eno in isto zdravilo več imen. Pomirjevalo diazenam ima blagovne znamke "seduxen", "sibazon", "relanium" itd. Nekatera zdravila imajo več kot 100 imen (na primer vitamin B12). Običajno ima zdravilo na embalaži tako blagovno znamko kot mednarodno nelastniško ime.
Zaželeno je generično predpisovanje zdravil, kar zmanjša možnost zdravniške napake... Ta zdravila so cenejša od blagovnih znamk. Poleg tega predpisovanje zdravil pod njihovim generičnim imenom omogoča lekarni, da pacientu zagotovi zdravilo katerega koli podjetja, ki to zdravilo proizvaja.
Za klinike je najprimernejša razvrstitev zdravil tista, ki temelji na NOZOLOŠKEM PRINCIPU (npr. zdravila za zdravljenje bronhialne astme, miokardnega infarkta, antidiabetiki ipd.). Toda najboljše klasifikacije upoštevajo značilnosti zdravil, kot so lokalizacija delovanja, farmakološko delovanje in terapevtska uporaba. Ena izmed takih klasifikacij, ki je najbolj popolna, je klasifikacija akademika M. D. Maškovskega, po kateri je predstavljena tudi njegova znana referenčna knjiga.
Blokator H1-histaminskih receptorjev prve generacije. Učinek na centralni živčni sistem je posledica blokade H3-histaminskih receptorjev v možganih in zaviranja osrednjih holinergičnih struktur. Lajša krče gladkih mišic (neposredno delovanje), zmanjšuje prepustnost kapilar, preprečuje in oslabi alergijske reakcije, deluje lokalno anestetično, antiemetično, sedativno, zmerno blokira holinergične receptorje avtonomnih ganglijev, deluje hipnotično.
Indikacije - anafilaktične in anafilaktoidne reakcije (v kombiniranem zdravljenju); - Quinckejev edem;
Serumska bolezen; - druga akutna alergijska stanja (v kombiniranem zdravljenju in v primerih, ko je uporaba v obliki tablet nemogoča).
Stranski učinki
S strani živčni sistem: zaspanost, šibkost, zmanjšana hitrost psihomotoričnih reakcij, motena koordinacija gibov, omotica, tremor, razdražljivost, evforija, vznemirjenost (zlasti pri otrocih), nespečnost.
S strani dihalni sistem: suhost sluznice ust, nosu, bronhijev (povečana viskoznost sputuma).
S strani hematopoeze: hemolitična anemija, trombocitopenija, agranulocitoza.
S strani srčno-žilnega sistema: znižanje krvnega tlaka, tahikardija, ekstrasistola.
Iz sečil: motnje uriniranja.
Alergijske reakcije: urtikarija, fotosenzibilnost, kožni izpuščaj, srbenje.
loratadin (klaritin)
farmakološki učinek
Antialergijsko zdravilo, selektivni blokator perifernih histaminskih H 1 receptorjev. Loratadin je triciklična spojina z izrazitim antihistaminskim učinkom. Ima hiter in dolgotrajen antialergijski učinek.
Loratadin ne prodre v BBB in ne vpliva na centralni živčni sistem. Nima klinično pomembnega antiholinergičnega ali sedativnega učinka, t.j. ne povzroča zaspanosti in ne vpliva na hitrost psihomotoričnih reakcij, če se uporablja v priporočenih odmerkih. Jemanje zdravila Claritin ne podaljša intervala QT na EKG. Pri dolgotrajnem zdravljenju ni bilo klinično pomembnih sprememb vitalnih znakov, podatkov fizičnega pregleda, laboratorijskih izvidov ali EKG.
Loratadin nima pomembne selektivnosti za histaminske H 2 receptorje. Ne zavira ponovnega privzema noradrenalina in ima malo ali nič vpliva na srčno-žilni sistem ali delovanje srčnega spodbujevalnika
Stranski učinki
Iz živčnega sistema: pri otrocih, starih od 2 do 12 let - glavobol (2,7%), živčnost (2,3%), utrujenost (1%); pri odraslih - glavobol (0,6%), zaspanost (1,2%), nespečnost (0,1%).
pri odraslih - povečan apetit (0,5%).
V postmarketinškem obdobju
Iz živčnega sistema: redko (< 1/10 000) - головокружение, утомляемость.
Iz prebavnega sistema: redko (< 1/10 000) - сухость во рту, желудочно-кишечные расстройства (тошнота, гастрит), нарушение функции печени.
Alergijske reakcije: redko (< 1/10 000) - сыпь, анафилаксия.
Na strani srčno-žilnega sistema: redko (< 1/10 000) - сердцебиение, тахикардия.
S strani kože: redko (< 1/10 000) - алопеция.
Indikacije
Sezonski (seneni nahod) in celoletni alergijski rinitis in alergijski konjunktivitis (za odpravo simptomov, povezanih s temi boleznimi - kihanje, srbenje nosne sluznice, rinoreja, pekoč občutek in srbenje v očeh, solzenje); - kronična idiopatska urtikarija; - kožne bolezni alergijskega izvora ...
33. Sredstva, ki odpravljajo splošne manifestacije alergijskih reakcij, kot je anafilaktični šok. Epinefrin, Eufillin, prednizolon. Glavni farmakološki učinki, namen predpisovanja posameznega zdravila in neželeni učinki.
PROTIALERGIJSKA ZDRAVILA(antialergijska; sin. desenzibilizacijska sredstva) - zdravila, ki preprečujejo ali oslabijo manifestacije alergijskih reakcij. Eden od možnih načinov preprečevanja in zdravljenja alergijskih reakcij je ti metoda. specifična hiposenzibilizacija, to je znižanje občutljivosti telesa na kateri koli antigen s ponavljajočim se dajanjem samega antigena v majhnih odmerkih, ki ne povzročajo alergijskih manifestacij. V tem primeru telo postopoma izgubi občutljivost na injicirani antigen.
Adrenalin
Farmakološko delovanje Adrenomimetik, ima neposreden stimulativni učinek na α- in β-adrenergične receptorje. Pod vplivom epinefrina (adrenalina) zaradi stimulacije α-adrenergičnih receptorjev pride do povečanja vsebnosti znotrajceličnega kalcija v gladkih mišicah. poveča aktivnost fosfolipaze C (s stimulacijo G-proteina) in tvorbo inozitol trifosfata in diacilglicerola. Ima izrazit učinek na srčno-žilni sistem. Poveča srčni utrip in moč, možgansko kap in srčni utrip. Izboljša AV prevodnost, poveča avtomatizem. Poveča potrebo po kisiku miokarda. Povzroča vazokonstrikcijo trebušnih organov, kože, sluznice, v manjši meri - skeletnih mišic. Zvišuje krvni tlak (predvsem sistolični), adrenalin (adrenalin) sprošča gladke mišice bronhijev, znižuje tonus in gibljivost prebavil, širi zenice in pomaga zniževati očesni tlak. Povzroča hiperglikemijo in poveča vsebnost prostih maščobnih kislin v plazmi. Indikacije Alergijske reakcije takojšnjega tipa (vključno z urtikarijo, angioedemom, anafilaktičnim šokom), ki se razvijejo ob uporabi zdravil, serumov, transfuzij krvi, hrane, ugrizov žuželk ali drugih alergenov. Bronhialna astma (lajšanje napada), bronhospazem med anestezijo. Da bi ustavili krvavitev. Neželeni učinek S strani srčno-žilnega sistema: angina pektoris, bradikardija ali tahikardija, palpitacije, zvišanje ali znižanje krvnega tlaka; pri uporabi v velikih odmerkih - ventrikularne aritmije; redko - aritmija, bolečine v prsnem košu. Iz živčnega sistema: glavobol, tesnoba, tresenje, omotica, živčnost, utrujenost, psihonevrotične motnje
Eufilin
farmakološki učinek
Bronhodilatator, derivat ksantina; zavira fosfodiesterazo, poveča kopičenje cikličnega adenozin monofosfata v tkivih, blokira adenozinske (purinske) receptorje; zmanjša pretok kalcijevih ionov skozi kanale celičnih membran, zmanjša kontraktilno aktivnost gladkih mišic. Sprošča mišice bronhijev, poveča mukociliarni očistek, stimulira krčenje diafragme, izboljša delovanje dihalnih in medrebrnih mišic, stimulira dihalni center, poveča njegovo občutljivost na ogljikov dioksid in izboljša alveolarno ventilacijo, kar na koncu vodi v zmanjšanje v resnosti in pogostosti epizod apneje. Z normalizacijo dihalne funkcije prispeva k nasičenosti krvi s kisikom in zmanjšanju koncentracije ogljikovega dioksida. Spodbujajoče vpliva na delovanje srca, povečuje moč in število srčnih kontrakcij, povečuje koronarni pretok krvi in potrebo miokarda po kisiku. Zmanjša tonus krvnih žil (predvsem žil možganov, kože in ledvic). Deluje periferno venodilatatorno, zmanjšuje upor pljučnih žil, znižuje pritisk v "majhnem" krogu krvnega obtoka. Poveča ledvični pretok krvi, ima zmeren diuretični učinek. Razširja ekstrahepatični žolčni trakt. Zavira agregacijo trombocitov (zavira faktor aktivacije trombocitov in PgE2 alfa), poveča odpornost eritrocitov na deformacijo (izboljša reološke lastnosti krvi), zmanjša nastajanje trombov in normalizira mikrocirkulacijo. Ima tokolitični učinek, poveča kislost želodčnega soka. Pri uporabi v velikih odmerkih ima enileptogeni učinek.
Stranski učinki
Iz živčnega sistema: omotica, glavobol, nespečnost, vznemirjenost, tesnoba, razdražljivost, tremor.
Na strani srčno-žilnega sistema: palpitacije, tahikardija (vključno pri plodu, če jo jemlje nosečnica v tretjem trimesečju), aritmije, kardialgija, znižanje krvnega tlaka, povečanje pogostosti napadov angine.
Iz prebavnega sistema: gastralgija, slabost, bruhanje, gastroezofagealni refluks, zgaga, poslabšanje peptične ulkusne bolezni, driska, pri dolgotrajni uporabi - zmanjšan apetit.
Alergijske reakcije: kožni izpuščaj, srbenje, vročina.
drugi: bolečine v prsih, tahipneja, zardevanje, albuminurija, hematurija, hipoglikemija, povečano izločanje urina, povečano potenje.
Indikacije
Bronhoobstruktivni sindrom katere koli geneze: bronhialna astma (zdravilo izbire pri bolnikih s fizičnim naporom astme in kot dodatno zdravilo za druge oblike), kronična obstruktivna pljučna bolezen, pljučni emfizem, kronični obstruktivni bronhitis, pljučna hipertenzija, pljučno srce, spanje apneja.
Prednizon
farmakološki učinek
Sintetični GCS. Ima izrazit protivnetni učinek. Zdravilo zavira razvoj simptomov vnetja. Zavira kopičenje makrofagov, levkocitov in drugih celic na območju vnetja. Zavira fagocitozo, sproščanje mikrosomskih encimov, pa tudi sintezo in sproščanje vnetnih mediatorjev. Povzroča zmanjšanje prepustnosti kapilar, zaviranje migracije levkocitov.
Izboljša sintezo lipomodulina, zaviralca fosfolipaze A2, ki sprošča arahidonsko kislino iz fosfolipidnih membran in hkrati zavira njeno sintezo.
Mehanizem imunosupresivnega delovanja prednizolona ni popolnoma razumljen. Zdravilo zmanjšuje število T-limfocitov, monocitov in acidofilnih granulocitov, pa tudi vezavo imunoglobulinov na receptorje na celični površini, zavira sintezo ali sproščanje interlevkinov z zmanjšanjem blastogeneze T-limfocitov; zmanjša zgodnji imunski odziv. Prav tako zavira prodiranje imunoloških kompleksov skozi membrane in zmanjšuje koncentracijo komponent komplementa in imunoglobulinov.
Prednizolon deluje na distalne ledvične tubule, poveča reabsorpcijo natrija in vode ter poveča izločanje kalijevih in vodikovih ionov.
Prednizolon zavira izločanje ACTH v hipofizi, kar vodi do zmanjšanja proizvodnje kortikosteroidov in androgenov v skorji nadledvične žleze. Po dolgotrajni uporabi zdravila v velikih odmerkih se lahko delovanje nadledvičnih žlez obnovi v enem letu, v nekaterih primerih pa se razvije vztrajno zatiranje njihovega delovanja. Prednizolon pospešuje katabolizem beljakovin in inducira encime, ki sodelujejo pri presnovi aminokislin. Zavira sintezo in pospešuje katabolizem beljakovin v limfnem, vezivnem, mišičnem tkivu. Pri dolgotrajni uporabi je možen razvoj atrofije teh tkiv (pa tudi kože).
Poveča koncentracijo glukoze v krvi z induciranjem encimov glukoneogeneze v jetrih, spodbuja katabolizem beljakovin (kar poveča količino aminokislin za glukoneogenezo) in zmanjša porabo glukoze v perifernih tkivih. To vodi do kopičenja glikogena v jetrih, povečanja koncentracije glukoze v krvi in povečanja odpornosti proti insulinu.
Indikacije
Endokrinološke bolezni:
Insuficienca skorje nadledvične žleze: primarna (Addisonova bolezen) in sekundarna; - adrenogenitalni sindrom (prirojena hiperplazija nadledvične žleze); - akutna insuficienca skorje nadledvične žleze;
Pred kirurškimi posegi in v primeru hudih bolezni in poškodb pri bolnikih z insuficienco nadledvične žleze; - subakutni tiroiditis.
Hude alergijske bolezni, odporne na druge terapije: - kontaktni dermatitis; - atopični dermatitis; - serumska bolezen; - preobčutljivostne reakcije na zdravila;
Trajni ali sezonski alergijski rinitis; - anafilaktične reakcije; - angioedem.
Revmatične bolezni:
Revmatoidni artritis, juvenilni revmatoidni artritis (v primerih, odpornih na druga zdravljenja);
Dermatološke bolezni: - eksfoliativni dermatitis - herpetiformis bulozni dermatitis;
hud seboroični dermatitis - hud multiformni eritem (Stevens-Johnsonov sindrom);
Stranski učinki
Pri kratkotrajni uporabi prednizona (tako kot drugih kortikosteroidov) so neželeni učinki redki. Pri dolgotrajni uporabi prednizolona se lahko pojavijo naslednji neželeni učinki.
Na strani vodno-elektrolitnega ravnovesja: zadrževanje v telesu natrija in tekočine, hipokalemija.
Iz mišično-skeletnega sistema: mišična oslabelost, steroidna miopatija, izguba mišične mase, osteoporoza, kompresijski zlom hrbtenice.
Iz prebavnega sistema: steroidni ulkus z možno perforacijo in krvavitvijo, pankreatitis, napenjanje, ulcerozni ezofagitis, prebavne motnje, slabost, povečan apetit.
Dermatološke reakcije: atrofija kože, strije, akne, zapoznelo celjenje ran, redčenje kože, petehije, hematomi, eritem, povečano potenje, alergijski dermatitis, urtikarija, angioedem.
S strani centralnega živčnega sistema in perifernega živčnega sistema: zvišan intrakranialni tlak s sindromom kongestivne bradavice vidnega živca (najpogosteje se pojavlja pri otrocih, po prehitrem zmanjšanju odmerka, simptomi - glavobol, poslabšanje ostrine vida, dvojni vid); konvulzije, omotica, glavobol, motnje spanja.
Glede na stanje endokrinega sistema: sekundarna insuficienca nadledvične žleze in hipotalamus-hipofize (zlasti v stresnih situacijah: bolezen, poškodba, operacija); Cushingov sindrom.
drugi: anafilaktične reakcije, preobčutljivostne reakcije; obliteracijski arteritis, povečanje telesne mase, omedlevica.
1. Bistvo farmakologije kot znanosti. Sekcije in področja sodobne farmakologije. Glavni izrazi in koncepti farmakologije so farmakološka aktivnost, delovanje, učinkovitost kemikalij.
farmakologija- znanost o zdravilih v vseh pogledih - teoretična osnova terapije:
a) znanost o interakciji kemikalij z živimi sistemi
b) znanost o upravljanju vitalnih procesov telesa s pomočjo kemikalij
Razvoj farmakologije gre v dve glavni smeri: temeljne raziskave za razjasnitev načel in mehanizmov delovanja in razvoja zdravil učinkovita zdravila kot osnova za zdravljenje bolezni.
Farmakologija je razdeljena na:
1. General- preučuje splošne zakonitosti medsebojnega delovanja zdravilnih snovi z živimi organizmi.
Zasebno- meni posebne farmakološke skupine in posamezna zdravila
2. Eksperimentalna (osnovna) farmakologija- preučuje učinek zdravil v poskusu.
Klinična farmakologija- preučuje klinično učinkovitost in varnost
uporabo zdravil pri bolnikih, optimizira program zdravljenja bolnika, ob upoštevanju
njegovo stanje.
Toksikologija- preučuje toksične učinke različnih snovi na organe (vključno z
in zdravilni).
Odseki sodobne farmakologije:
1) farmakodinamika- preučuje a) vpliv zdravil na človeško telo, b) medsebojno delovanje različnih zdravil v telesu med predpisovanjem, c) vpliv starosti in različnih bolezni na učinek zdravil
2) farmakokinetika- preučuje absorpcijo, porazdelitev, presnovo in izločanje zdravil (tj. kako se bolnikovo telo odziva na zdravila)
3) farmakogenetika- preučuje vlogo genetskih dejavnikov pri oblikovanju farmakološkega odziva telesa na zdravila
4) farmakoekonomija- ocenjuje rezultate uporabe in stroške zdravil za odločitev o njihovi nadaljnji praktični uporabi
5) farmakoepidemiologija- preučuje uporabo drog in njihove učinke na ravni populacij ali velikih skupin ljudi, da zagotovi uporabo najbolj učinkovitih in varnih zdravil
Osnovni izrazi in pojmi:
Farmakološka (biološka) aktivnost- lastnost snovi, da povzroča spremembe v biosistemu (človeško telo). Farmakološke snovi = biološko aktivne snovi (BAS)
farmakološki učinek- vpliv zdravil na predmet in njegove tarče
Farmakološki učinek- rezultat delovanja snovi v telesu (sprememba fizioloških, biokemičnih procesov, morfoloških struktur) - kvantitativna, ne pa kakovostna sprememba stanja biosistemov (celice, tkiva, organi).
Učinkovitost zdravil- sposobnost zdravil, da povzročijo določene farmakološke učinke, ki so v tem primeru potrebni v telesu. Ocenjeno na podlagi "znatnih dokazov" - ustreznih dobro nadzorovanih študij in kliničnih preskušanj, ki jih izvajajo strokovnjaki z ustreznim znanstvenim usposabljanjem in izkušnjami na področju raziskav zdravil te vrste (FDA)
2. Viri in faze nastanka zdravil. Zdravila - generiki, placebo - učinki Opredelitev pojmov zdravila, zdravila, zdravila in dozirne oblike.
Viri ustvarjanja zdravil:
a) naravne surovine: rastline, živali, minerali, odpadni produkti mikroorganizmov (srčni glikozidi, svinjski inzulin, AB)
b) modificirane naravne biološko aktivne snovi
c) produkti kemične sinteze (metode: farmakološko presejanje, molekularno načrtovanje, reprodukcija biogenih aminov, ciljna modifikacija molekul z že znano aktivnostjo, sinteza farmakološko aktivnih metabolitov, naključne ugotovitve ("serendipična" metoda))
d) proizvodi genskega inženiringa (rekombinantni insulin, interferoni)
Faze ustvarjanja zdravila:
1. Sinteza zdravil v kemijskem laboratoriju
2. Predklinična ocena delovanja in neželenih učinkov zdravil Ministrstva za zdravje in drugih organizmov
3. Klinična preskušanja zdravil Pregled dokumentacije s strani Farmakološke komisije se opravi po zaključku vsake faze. Zdravilo se lahko umakne v kateri koli fazi. (I. faza - ocena tolerance pri zdravih prostovoljcih, starih 20-25 let, II. faza - na bolnih prostovoljcih z manj kot 100 osebami, ki trpijo za določeno boleznijo, III. faza - multicentrična klinična preskušanja na velikih skupinah ljudi (do 1000 ljudi) , faza IV - spremljanje zdravil 5 let po uradnem dovoljenju (izvedeno dne veliko število bolniki (vsaj 1.000-5.000 ljudi). Po zaključku III faze kliničnih preskušanj gre dokumentacija ponovno na farmakološko komisijo (obseg celotne dokumentacije je lahko do 1 milijon strani) in se v 1-2 letih registrira v državni register zdravil in izdelkov medicinski namen... Šele po tem ima farmacevtski koncern pravico začeti z industrijsko proizvodnjo zdravila in njegovo distribucijo prek lekarniške mreže.
Generično zdravilo je generično zdravilo, ki je priredba originalnega zdravila, za katerega je potekel patent. Lahko se razlikuje od prvotnega zdravila po sestavi pomožnih snovi. Potrebna zahteva za prodajo generikov – na dokazih podprta farmacevtska, biološka in terapevtska enakovrednost matičnemu zdravilu. Generična zdravila so vedno cenejša od svojih blagovnih znamk, ker podjetje ne porabi denarja za 10-15 let raziskav zdravil, ampak uporablja že pripravljene podatke
Placebo- katero koli sestavino terapije, ki nima posebnega biološkega učinka na bolezen, ki je predmet zdravljenja.
Uporablja se z namenom nadzora pri ocenjevanju učinka zdravil in v korist bolnika brez farmakoloških učinkovin kot posledica zgolj psihičnega vpliva (tj. placebo učinek).
Vse vrste zdravljenja imajo psihološko komponento ali zadovoljivo ( placebo učinek) ali moteče ( nocebo učinek). Primer placebo učinka: hitro izboljšanje pri bolniku z virusno okužbo z uporabo antibiotikov. Prednost placebo učinka je povezana s psihološkim vplivom na bolnika. Največja bo le ob uporabi. v kombinaciji z metodami zdravljenja ki imajo izrazit specifičen učinek. Drage snovi kot placebo pomaga tudi pri doseganju večjega odziva.
Indikacije za uporabo placeba:
1) šibke duševne motnje
2) psihološka podpora bolniku z neozdravljivo kronično boleznijo ali sumom, da ima težko diagnozo
Zdravilo- katera koli snov ali izdelek, ki se uporablja za spreminjanje ali raziskovanje fizioloških sistemov ali patoloških stanj v korist prejemnika (po WHO, 1966); posamezne snovi, mešanice snovi ali sestavke neznane sestave z dokazanimi zdravilnimi lastnostmi.
Zdravilna snov- posamezna kemična spojina, ki se uporablja kot zdravilo.
Odmerna oblika- priročna oblika za praktično uporabo, ki se daje zdravilu za dosego zahtevanega terapevtskega ali profilaktičnega učinka.
Zdravilo- zdravilo v posebni dozirni obliki, ki jo odobri državni organ.
Na primer: zdravilo je antibiotik ampicilin, zdravilo je ampicilin trihidrat, ki je lahko v obliki tablet ali kapsul. Zdravilo je ampicilin trihidrat tablete po 0,25 g.
Poti vnosa zdravil v telo in njihove značilnosti. Presistemsko izločanje zdravil.
a. enteralni način dajanja: peroralno, sublingvalno, bukalno, rektalno, cevno b. parenteralni način dajanja: intravensko, subkutano, intramuskularno, ... 2. Za lokalno izpostavljenost: koža (epikutarno), na sluznicah, v votlinah (trebušna, plevralna, sklepna), v tkivu ...Prevoz zdravil čez biološke ovire in njegove sorte. Glavni dejavniki, ki vplivajo na transport zdravil v telesu.
1) Filtracija (difuzija vode) - pasivno gibanje molekul snovi vzdolž koncentracijskega gradienta skozi pore, napolnjene z vodo v membrani vsakega ... 2) Pasivna difuzija (difuzija lipidov) - glavni mehanizem prenosa zdravila, ... 3 ) Prevoz s posebnimi nosilci - prenos zdravil z nosilci, vgrajenimi v membrano (pogosteje ...Prevoz zdravilnih snovi s spremenljivo ionizacijo skozi membrane (Henderson-Hasselbalchova ionizcijska enačba). Načela nadzora prenosa.
Vsa zdravila so šibke kisline ali šibke baze, ki imajo svoje vrednosti ionizacijske konstante (pK). Če je pH vrednost medija enaka pK vrednosti zdravila, bo 50 % njegovih molekul v ioniziranem stanju in 50 % v neioniziranem stanju, medij za zdravilo pa bo nevtralen.
V kislem mediju (pH manjši od pK), kjer je presežek protonov, bo šibka kislina v nedisociirani obliki (R-COOH), t.j. bo povezan s protonom - protoniran. Ta oblika kisline je nenapolnjena in je zlahka topna v lipidih. Če se pH premakne na alkalno stran (tj. pH postane večji od pK), se bo kislina začela disociirati in izgubila proton ter prešla v neprotonirano obliko, ki ima naboj in je slabo topna v lipidih. .
V alkalnem mediju, kjer primanjkuje protonov, bo šibka baza v nedisociirani obliki (R-NH 2), t.j. bo neprotoniran in brez naboja. Ta oblika baze je zelo topna v lipidih in se hitro absorbira. V kislem mediju je protonov presežek in šibka baza bo začela disociirati, medtem ko bo protone vezala in tvorila protonirano, nabito obliko baze. Ta oblika je slabo topna v lipidih in se slabo absorbira.
zato absorpcija šibkih kislin poteka predvsem v kislem okolju, šibkih baz pa v alkalnem okolju.
Značilnosti presnove šibkih kislin (SC):
1) želodec: SA v kisli vsebini želodca ni ioniziran, v alkalnem mediju tankega črevesa pa se bo disociral in molekule SA bodo pridobile naboj. Zato bo absorpcija šibkih kislin najbolj intenzivna v želodcu.
2) v krvi je medij dovolj alkalen in absorbirane SC molekule se bodo preoblikovale v ionizirano obliko. Filter ledvičnega glomerula omogoča prehod tako ioniziranim kot neioniziranim molekulam, zato se bo SC kljub naboju molekule izločil v primarni urin
3) če je urin alkalen, bo kislina ostala v ionizirani obliki, se ne bo mogla ponovno absorbirati v krvni obtok in se bo izločila z urinom; Če je urin kisel, bo zdravilo prešlo v neionizirano obliko, ki se zlahka absorbira nazaj v kri.
Značilnosti presnove šibkih baz: nasprotno SC (absorpcija je boljša v črevesju; v alkalnem urinu se reabsorbirajo)
to., za pospešitev izločanja šibke kisline iz telesa je treba urin alkalizirati, za pospešitev izločanja šibke baze pa ga nakisati (razstrupljanje po Popovu).
Kvantitativna odvisnost procesa ionizacije zdravila pri različnih pH vrednostih medija omogoča, da dobimo enačbo Henderson-Hasselbach:
kjer pKa ustreza vrednosti pH, pri kateri so koncentracije ionizirane in neionizirane oblike v ravnotežju .
Henderson-Hasselbachova enačba omogoča oceno stopnje ionizacije zdravila pri dani pH vrednosti in predvidevanje verjetnosti njegove penetracije skozi celično membrano.
(1)Za razredčeno kislino, A,
HA ↔ H + + A -, kjer je HA koncentracija neionizirane (protonirane) oblike kisline in A - koncentracija ionizirane (neprotonirane) oblike.
(2) Za šibka osnova, B,
BH + ↔ H + + B, kjer je BH + koncentracija protonirane oblike baze, B je koncentracija neprotonirane oblike
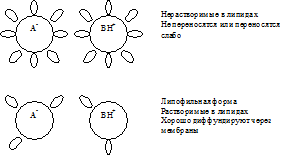
Če poznamo pH medija in pKa snovi, je mogoče iz izračunanega logaritma določiti stopnjo ionizacije zdravila in s tem stopnjo njegove absorpcije iz prebavil, reabsorpcije ali izločanja skozi ledvice pri različnih pH vrednosti urina itd.
Načela nadzora prometa.
Za pospešitev absorpcije
Ø šibke kisline (ASA) - pH želodčnega soka mora biti kisel;
Ø šibka osnova - pH želodčnega soka mora biti nevtralen.
Za pospešitev umika
Ø šibke kisline - urin postane alkalen;
Ø šibke baze - zakisajo urin.
Prenos zdravil v telesu. Difuzija vode in difuzija v lipidih (Fickov zakon). Aktivni transport.
Prenos zdravil v telesu se lahko izvaja z difuzijo vode in lipidov, aktivnim transportom, endocitozo in pinocitozo.
Značilnosti prenosa zdravil v telesu z difuzijo vode:
1. Epitelijske obloge (sluznice gastrointestinalnega trakta, ustne votline itd.) - difuzija vode le zelo majhnih molekul (metanol, litijevi ioni itd.)
2. Kapilare (razen cerebralnih) - filtracija snovi z molekulsko maso do 20-30 tisoč Da.
3. Kapilare možganov - v bistvu nimajo vodnih por, z izjemo predelov hipofize, epifize, prekata IV cone, horoidnega pleksusa, mediane eminence
4. Placenta - nima vodnih por (čeprav je vprašanje sporno).
5. Vezava zdravil na krvne beljakovine preprečuje njihov izstop iz krvnega obtoka in s tem difuzijo vode
6. Difuzija v vodi je odvisna od velikosti molekul zdravila in vodnih por
Značilnosti difuzije lipidov:
1. Glavni mehanizem prenosa zdravila čez celične membrane
2. Določeno z lipofilnostjo razpršene snovi (tj. koeficientom porazdelitve olje/voda) in gradientom koncentracije, jo je mogoče omejiti z zelo nizko topnostjo snovi v vodi (ki preprečuje prodiranje zdravila v vodno fazo). membran)
3. Nepolarne spojine zlahka razpršijo, ione je težko difundirati.
Vsaka difuzija (tako voda kot lipidi) upošteva Fickov zakon difuzije:
Hitrost difuzije - število molekul zdravila, ki se prenašajo na enoto časa; С 1 - koncentracija snovi zunaj membrane; С 2 - koncentracija snovi iz notranjosti membrane.
Posledica Fickovega zakona:
1) večja je filtracija zdravila, večja je njegova koncentracija na mestu injiciranja (S absorbirane površine v črevesju je večji kot v želodcu, zato je absorpcija zdravila v črevesju hitrejša)
2) višja kot je koncentracija zdravila na mestu injiciranja, višja je filtracija zdravila
3) večja je filtracija zdravil, manjša je debelina biološke membrane, ki jo je treba premagati (debelina pregrade v pljučnih alveolah je veliko manjša od kože, zato je stopnja absorpcije višja v pljuča)
Aktivni transport- prenos zdravil, ne glede na koncentracijski gradient z uporabo energije ATP, je značilen za hidrofilne polarne molekule, številne anorganske ione, sladkorje, aminokisline, pirimidine.
Značilen po: a) selektivnost za določene spojine b) možnost konkurence dveh snovi za en transportni mehanizem c) nasičenost pri visokih koncentracijah snovi d) možnost transporta proti koncentracijskemu gradientu e) poraba energije.
7. Osrednji postulat farmakokinetike je koncentracija zdravila v krvi – glavni parameter za nadzor terapevtskega učinka. Problemi rešeni na podlagi poznavanja tega postulata.
Osrednji postulat (dogma) farmakokinetike: koncentracija zdravila v krvni plazmi določa (kvantificira) farmakološki učinek.
V večini primerov je stopnja absorpcije, porazdelitve, presnove in izločanja zdravil sorazmerna z njihovo koncentracijo v krvni plazmi (upošteva zakon množičnega delovanja), torej, če vemo, da je možno:
1) določiti razpolovni čas (za zdravila s kinetiko prvega reda)
2) pojasniti trajanje nekaterih toksičnih učinkov zdravil (za zdravila v velikih odmerkih s kinetiko nasičenosti)
[C] plazma → [C] na tarči → učinek
Določeno z zakoni je določeno z z-usom farmakodinamike
Distribucija
Cilji: naučiti se nadzorovati koncentracijo zdravila v krvi.
Farmakokinetični modeli (enokomorni in dvokomorni), kvantitativni zakoni absorpcije in izločanja zdravila.
Celoten organizem je ena sama homogena posoda. Predpostavke: 1) se vzpostavi hiter dinamičen razvoj med vsebnostjo zdravila v ... 2) zdravilo se hitro in enakomerno porazdeli po volumnu krviPorazdelitev zdravil v telesu. Kompartmenti, ligandi. Glavne determinante distribucije.
Porazdelitveni predelki: 1. Zunajcelični prostor (plazma, medcelična tekočina) 2. Celice (citoplazma, organela membrana)Konstanta izločanja, njeno bistvo, dimenzija, razmerje z drugimi farmakokinetičnimi parametri.
Konstanta hitrosti izločanja(k el, min -1) - prikazuje, kateri del zdravil se izloči iz telesa na enoto časa Þ Kel = A out / A total, kjer je A out količina sproščenih zdravil v enotah. čas, In skupno - skupna količina zdravil v telesu.
Vrednost k el običajno najdemo z reševanjem farmakokinetične enačbe, ki opisuje proces izločanja zdravila iz krvi, zato k el imenujemo modelni kinetični indeks. K el ni neposredno povezan z načrtovanjem režima odmerjanja, vendar se njegova vrednost uporablja za izračun drugih farmakokinetičnih parametrov.
Konstanta izločanja je neposredno sorazmerna z očistkom in obratno sorazmerna z volumnom porazdelitve (iz definicije očistka): Kel = CL / Vd; = ura -1 / min -1 = frakcija na uro.
Razpolovna doba zdravila, njegovo bistvo, dimenzija, razmerje z drugimi farmakokinetičnimi parametri.
Obdobje polovice izločanja(t ½, min) je čas, potreben za zmanjšanje koncentracije zdravil v krvi za natanko polovico. V tem primeru ni pomembno, na kakšen način se doseže znižanje koncentracije – s pomočjo biotransformacije, izločanja ali zaradi kombinacije obeh procesov.
Razpolovni čas je določen s formulo:
![]()
Razpolovna doba je najpomembnejši farmakokinetični parameter, ki omogoča:
b) določi čas popolnega izločanja zdravila
c) kadar koli napovedati koncentracijo zdravil (za zdravila s kinetiko prvega reda)
Očistek kot glavni farmakokinetični parameter za upravljanje režima odmerjanja. Njegovo bistvo, razsežnost in razmerje z drugimi farmakokinetičnimi parametri.
Odstopanje(Cl, ml / min) - volumen krvi, ki se očisti iz zdravil na enoto časa.
Ker plazma (kri) je »vidni« del volumna porazdelitve, nato je očistek delež volumna porazdelitve, iz katerega se zdravilo sprosti na enoto časa. Če označimo celotno količino zdravila v telesu skozi In na splošno, in znesek, ki je bil dodeljen po tem In ven, potem:
Po drugi strani pa iz definicije volumna porazdelitve izhaja, da je skupna količina zdravila v telesu Skupaj = V d ´C ter / plazma... Če to vrednost nadomestimo v formulo za odmik, dobimo:
![]() .
.
Tako je očistek razmerje med hitrostjo izločanja zdravila in njegovo koncentracijo v krvni plazmi.
V tej obliki se formula očistka uporablja za izračun vzdrževalnega odmerka zdravila ( D str), to je odmerek zdravila, ki bi moral nadomestiti izgubo zdravila in vzdrževati njegovo raven na konstantni ravni:
Hitrost dajanja = hitrost izločanja = Cl'C ter (odmerek/min)
D p = hitrost infuzije 't (t je interval med vnosom zdravila)
Odmik od tal je dodatek, tj. izločanje snovi iz telesa lahko poteka s sodelovanjem procesov v ledvicah, pljučih, jetrih in drugih organih: Cl sistemski = Cl ledvični. + Cl jetra + Cl drugi.
Dovoljenje je vezano z razpolovno dobo zdravila in volumnom porazdelitve: t 1/2 = 0,7 * Vd / Cl.
Odmerek. Vrste odmerkov. Odmerne enote zdravila. Cilji odmerjanja zdravil, metode in možnosti dajanja, interval dajanja.
Učinek zdravil na telo je v veliki meri odvisen od njihovega odmerka.
Odmerek- količina snovi, ki se naenkrat vnese v telo; izraženo v teži, prostornini ali konvencionalnih (bioloških) enotah.
Vrste odmerkov:
a) enkratni odmerek - količina snovi na odmerek
b) dnevni odmerek - količina zdravila, predpisana na dan v enem ali več odmerkih
c) tečajni odmerek - skupna količina zdravila za potek zdravljenja
d) terapevtski odmerki - odmerki, v katerih se zdravilo uporablja v terapevtske ali profilaktične namene (prag oz. minimalni učinkovit, povprečni terapevtski in višji terapevtski odmerki).
e) toksični in smrtonosni odmerki - odmerki zdravil, pri katerih začnejo imeti izrazite toksične učinke ali povzročijo smrt telesa.
f) polnilni (uvodni) odmerek - število injiciranih zdravil, ki zapolni celoten volumen porazdelitve telesa v efektivni (terapevtski) koncentraciji: VD = (Css * Vd) / F
g) vzdrževalni odmerek - sistematično uporabljena količina zdravil, ki nadomesti izgubo zdravil z očistkom: PD = (Css * Cl * DT) / F
Farmacevtske dozirne enote:
1) v gramih ali frakcijah grama zdravil
2) število zdravil na 1 kg telesna teža (na primer 1 mg/kg) ali na enoto površine telesa (na primer 1 mg/m2)
Cilji odmerjanja zdravil:
1) določi količino zdravil, ki je potrebna, da se doseže želeni terapevtski učinek z določenim trajanjem
2) preprečiti pojav zastrupitve in stranskih učinkov z uvedbo zdravil
Metode dajanja zdravila: 1) enteralno 2) parenteralno (glejte poglavje 5)
Možnosti dajanja zdravil:
a) neprekinjeno (z dolgotrajno intravaskularno infuzijo zdravil po kapljanju ali prek avtomatskih razpršilnikov). Z neprekinjenim dajanjem zdravil se njegova koncentracija v telesu gladko spreminja in ne doživlja bistvenih nihanj.
b) intermitentno dajanje (z injekcijskimi ali neinjekcijskimi metodami) - dajanje zdravila v rednih časovnih presledkih (dozirni intervali). Z občasnim dajanjem zdravil njegova koncentracija v telesu nenehno niha. Po zaužitju določenega odmerka se najprej dvigne, nato pa postopoma zmanjšuje in doseže minimalne vrednosti pred naslednjim dajanjem zdravila. Nihanja v koncentraciji so pomembnejša, večji kot je uporabljeni odmerek zdravila in interval med injekcijami.
Interval vbrizgavanja- interval med danimi odmerki, ki zagotavlja vzdrževanje terapevtske koncentracije snovi v krvi.
15. Dajanje zdravil s konstantno hitrostjo. Kinetika koncentracije zdravila v krvi. Stacionarna koncentracija zdravila v krvi (C ss), čas, da se doseže, njen izračun in upravljanje.
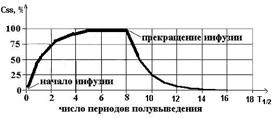 Posebnost vnosa zdravil s konstantno hitrostjo je gladka sprememba njegove koncentracije v krvi ob dajanju, medtem ko:
Posebnost vnosa zdravil s konstantno hitrostjo je gladka sprememba njegove koncentracije v krvi ob dajanju, medtem ko:
1) čas za dosego koncentracije zdravila v stanju dinamičnega ravnovesja je 4-5t ½ in ni odvisen od hitrosti infundiranja (velikosti danega odmerka)
2) s povečanjem hitrosti infundiranja (vbrizganega odmerka) se sorazmerno krat poveča tudi vrednost C SS
3) izločanje zdravila iz telesa po koncu infuzije traja 4-5t ½.
Сss - ravnotežna stacionarna koncentracija- koncentracija zdravil, dosežena pri hitrosti dajanja, ki je enaka hitrosti izločanja, torej:
![]() (iz definicije razmika)
(iz definicije razmika)
Za vsako naslednjo razpolovno dobo se koncentracija zdravila poveča za polovico preostale koncentracije. Vsa zdravila, ki izpolnjujejo zakon o izločitvi prvega reda, so bo Css dosegel v 4-5 razpolovnih časih.
Pristopi k upravljanju ravni Css: spremenite odmerek zdravila ali interval vnosa
16. Občasno dajanje zdravil. Kinetika koncentracije zdravila v krvi, terapevtsko in toksično območje koncentracij. Izračun stacionarne koncentracije (C ss), meja njenih nihanj in njen nadzor. Ustrezen diskretni interval odmerjanja.
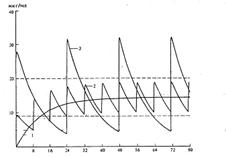 Nihanja koncentracije zdravil v krvni plazmi: 1 - s stalnim intravenskim kapljanjem; 2 - z delno uvedbo enakega dnevnega odmerka z intervalom 8 ur; 3 - z uvedbo dnevnega odmerka v intervalu 24 ur.
Nihanja koncentracije zdravil v krvni plazmi: 1 - s stalnim intravenskim kapljanjem; 2 - z delno uvedbo enakega dnevnega odmerka z intervalom 8 ur; 3 - z uvedbo dnevnega odmerka v intervalu 24 ur.
Intermitentno dajanje zdravil- dajanje določene količine zdravil v intervalih.
Ravnotežna koncentracija v stanju dinamičnega ravnovesja je dosežena po 4-5 obdobjih polovične izločanja, čas njenega doseganja ni odvisen od odmerka (na začetku, ko je koncentracija zdravila nizka, je nizka tudi hitrost njegovega izločanja; ko se količina snovi v telesu poveča, se poveča tudi hitrost njenega izločanja, zato bo zgodaj ali pozno prišel trenutek, ko bo povečana hitrost izločanja uravnotežila dani odmerek zdravila in se bo nadaljnje povečevanje koncentracije ustavilo)
Css je neposredno sorazmeren z odmerkom zdravila in obratno sorazmeren z intervalom injiciranja in očistkom zdravila.
Css Swing Meje: ![]() ; C ss min = C ss max × (1 - e-pošta). Nihanja koncentracije zdravila so sorazmerna s T / t 1/2.
; C ss min = C ss max × (1 - e-pošta). Nihanja koncentracije zdravila so sorazmerna s T / t 1/2.
Terapevtski obseg (varnostni hodnik, terapevtsko okno)- To je razpon koncentracij od minimalne terapevtske do povzročanja prvih znakov stranskih učinkov.
Toksičen obseg- razpon koncentracije od najvišje terapevtske do smrtonosne.
Ustrezno dajanje diskretnih odmerkov: način dajanja, pri katerem nihanje koncentracije zdravila v krvi spada v terapevtsko območje. Za določitev ustreznega režima dajanja zdravila je treba izračunati. Razlika med Css max in Css min ne sme presegati 2Css.
Nadzor nihanj Css:
Obseg nihanj Css je neposredno sorazmeren z odmerkom zdravila in obratno sorazmeren z intervalom njegove uporabe.
1. Spremenite odmerek zdravil: s povečanjem odmerka zdravila se razpon nihanj njegovega Css sorazmerno poveča
2. Spremenite interval dajanja zdravila: s povečanjem intervala dajanja zdravila se razpon nihanj njegovega Css sorazmerno zmanjša
Hkrati spremenite odmerek in interval dajanja
Uvodni (polnilni) odmerek. Terapevtski pomen, izračun po farmakokinetičnih parametrih, pogoji in omejitve uporabe.
Uvodni (polnilni) odmerek- enkratni odmerek, ki zapolni celoten volumen porazdelitve v trenutni terapevtski koncentraciji. VD = (Css * Vd) / F; = mg / l, = l / kg
Terapevtski pomen: začetni odmerek hitro zagotovi učinkovito terapevtsko koncentracijo zdravil v krvi, kar omogoča, na primer, hitro zaustavitev napada astme, aritmij itd.
Uvodni odmerek se lahko daje naenkrat le, ko proces porazdelitve snovi je prezrt
Omejitev uporabe VD: če se zdravilo distribuira veliko počasneje kot vstop v krvni obtok, bo uvedba celotnega polnilnega odmerka naenkrat (zlasti intravensko) ustvarila koncentracijo, ki je bistveno višja od terapevtske, in bo povzročila pojav toksičnih učinkov. VD stanje uporabe: torej uvedba obremenilnih odmerkov mora biti vedno počasen ali delno.
Vzdrževalni odmerki, njihov terapevtski pomen in izračun za optimalni režim odmerjanja.
Terapevtski smisel: PD kompenzira izgube z očistkom v intervalu med injekcijami zdravila. Izračun optimalnega odmerka zdravil (za hitro lajšanje napada): ... 1. Izračunajte VD: VD = (Css * Vd) / FPosamezne, starostne in spolne razlike v farmakokinetiki zdravil. Popravki za izračun posameznih vrednosti za volumen porazdelitve zdravil.
2. Spolne razlike v delovanju zdravil. Za ženske je značilna nižja telesna teža kot za moške, zato bi morala velikost odmerkov zdravila zanje ... 3. Patološka stanja telesa in učinki zdravil a) bolezni jeter: F zdravila zaradi onemogočanja prve- prehaja presnovo, del nevezanih zdravil zaradi pomanjkanja ...Ledvični očistek zdravil, mehanizmi, njihove kvantitativne in kvalitativne značilnosti.
Mehanizmi ledvičnega očistka in njihove značilnosti: 1. Filtracija: zdravila, ki se sproščajo samo s filtracijo (inzulin), bodo imela očistek, ... Določajo: ledvični pretok krvi, nevezana frakcija zdravila in filtracijska zmogljivost ledvic.Dejavniki, ki vplivajo na ledvični očistek zdravil. Odvisnost očistka od fizikalno-kemijskih lastnosti zdravil.
a) glomerularna filtracija b) hitrost ledvičnega krvnega pretoka c) največja hitrost izločanjaOčistek zdravil iz jeter, njegove determinante in omejitve. Enterohepatični cikel zdravil.
1) presnova (biotransformacija) z oksidacijo, redukcijo, alkilacijo, hidrolizo, konjugacijo itd. Glavna strategija presnove ksenobiotikov: nepolarne snovi ® polar ... 2) izločanje (izločanje netransformiranih snovi v žolč)Popravek zdravljenja z zdravili za poškodbe jeter in druga patološka stanja.
Za popravek režima odmerjanja v primeru bolezni ledvic glejte odstavek 26 zgoraj, za splošna načela korekcije glejte odstavek 25. Popravek režima odmerjanja pod nadzorom celotnega očistka zdravila: Popravek odmerka: Din. = Dtypical × Clind. / Cltypical.Popravek režima odmerjanja pod nadzorom preostale ledvične funkcije.
Poznamo: a) preostalo ledvično funkcijo, ki jo določa očistek kreatinina v danem ... b) celotni očistek danega zdravila (CLP / total) in delež ledvičnega očistka zdravila v celotnem očistkuIndividualna strategija zdravljenja z zdravili.
Prepoznavanje pomembne vloge koncentracije kot povezave med farmakokinetiko in farmakodinamiko prispeva k oblikovanju strategije ciljne koncentracije – optimizirati odmerek pri danem bolniku na podlagi merjenja koncentracije zdravila. Sestavljen je iz naslednjih stopenj:
1. Izbira ciljne koncentracije
2. Izračunajte V d in Cl na podlagi tipičnih vrednosti in prilagodite dejavnike, kot sta telesna teža in delovanje ledvic.
3. Vnos polnilnega ali vzdrževalnega odmerka, izračunanega ob upoštevanju vrednosti TC, V d in Cl.
4. Registracija bolnikove reakcije in določanje koncentracije zdravila
5. Revizija V d in Cl na podlagi rezultatov meritev koncentracije.
6. Ponovite korake 3-6, da prilagodite vzdrževalni odmerek, potreben za optimalen odziv na zdravilo.
Biotransformacija zdravil, njen biološki pomen, glavna usmeritev in vpliv na delovanje zdravil. Glavne faze presnovnih transformacij zdravil v telesu.
Biotransformacija zdravil - kemične transformacije zdravil v telesu.
Biološki pomen biotransformacije zdravil: ustvarjanje substrata, ki je primeren za naknadno odlaganje (kot energijski ali plastični material) ali za pospeševanje izločanja zdravil iz telesa.
Glavna smer presnovnih transformacij zdravil: nepolarna zdravila → polarni (hidrofilni) metaboliti, ki se izločajo z urinom.
Obstajata dve fazi presnovnih reakcij zdravil:
1) presnovna transformacija (nesintetične reakcije, faza 1) - transformacija snovi zaradi mikrosomske in ekstra mikrosomske oksidacije, redukcije in hidrolize
2) konjugacija (sintetične reakcije, faza 2) - biosintetični proces, ki ga spremlja dodajanje številnih kemičnih skupin ali molekul endogenih spojin zdravilu ali njegovim metabolitom z a) tvorbo glukuronidov b) glicerolovih estrov c) sulfoestrov d ) acetilacija e) metilacija
Učinek biotransformacije na farmakološko aktivnost zdravil:
1) najpogosteje metaboliti biotransformacije nimajo farmakološke aktivnosti ali pa je njihova aktivnost zmanjšana v primerjavi z začetno snovjo
2) v nekaterih primerih lahko presnovki ohranijo aktivnost in celo presežejo aktivnost matične snovi (kodein se presnovi v bolj farmakološko aktivni morfin)
3) včasih med biotransformacijo nastanejo strupene snovi (metaboliti izoniazida, lidokaina)
4) včasih med biotransformacijo nastanejo presnovki z nasprotnimi farmakološkimi lastnostmi (presnovki neselektivnih agonistov b 2 - adrenergični receptorji imajo lastnosti blokatorjev teh receptorjev)
5) številne snovi so predzdravila, ki sprva ne dajejo farmakoloških učinkov, vendar se med biotransformacijo pretvorijo v biološko aktivne snovi (neaktivna L-dopa, ki prodre v BBB, se v možganih spremeni v aktivni dopamin, medtem ko obstajajo ni sistemskih učinkov dopamina).
Klinični pomen biotransformacije zdravil. Dejavniki, ki vplivajo na njihovo btotransformacijo. Metabolične interakcije z zdravili.
Vpliv različnih dejavnikov na biotransformacijo zdravil: a) funkcionalno stanje jeter: pri njegovih boleznih je očistek zdravil običajno ... b) vpliv okoljskih dejavnikov: kajenje spodbuja indukcijo citokroma P450, saj zaradi česar se metabolizem zdravil v ...Načini in mehanizmi izločanja zdravil iz telesa. Možnosti nadzora izločanja zdravil.
Načini in mehanizmi izločanja zdravila: izločanje zdravil z jetri in ledvicami ter nekaterimi drugimi organi:
a) preko ledvic s filtracijo, izločanjem, reabsorpcijo
b) jetra z biotransformacijo, izločanje z žolčem
c) skozi pljuča, slino, znoj, mleko itd. z izločanjem, izhlapevanjem
Možnosti za vodenje procesov odvzema drog:
1. nadzor pH: v alkalnem urinu se poveča izločanje kislih spojin, v kislem urinu izločanje bazičnih spojin
2.uporaba holeretičnih zdravil (holenzim, alohol)
3.hemodializa, peritonealna dializa, hemosorpcija, limfosorpcija
4. Prisilna diureza (IV NaCl ali glukoza za obremenitev z vodo + furosemid ali manitol)
5.izpiranje želodca, uporaba klistirjev
Pojem receptorjev v farmakologiji, molekularna narava receptorjev, signalni mehanizmi delovanja zdravil (vrste transmembranske signalizacije in sekundarni prenašalci).
Receptorji - molekularne komponente celice ali organizma, ki medsebojno delujejo z zdravili in povzročajo številne biokemične dogodke, ki vodijo do razvoja farmakološkega učinka.
Koncept receptorjev v farmakologiji:
1. Receptorji določajo kvantitativne vzorce delovanja zdravila
2. Receptorji so odgovorni za selektivnost delovanja zdravila
3. Receptorji posredujejo delovanje farmakoloških antagonistov
Koncept receptorjev je osnova za ciljno uporabo zdravil, ki vplivajo na regulacijske, biokemične procese in komunikacijo.
Molekularna narava receptorjev:
1.regulacijski proteini, mediatorji delovanja različnih kemičnih signalov: nevrotransmiterji, hormoni, avtokoidi
2.encimi in transmembranski nosilci beljakovin (Na +, K + ATPaza)
3.strukturne beljakovine (tubulin, citoskeletni proteini, celična površina)
4.jedrske beljakovine in nukleinske kisline
Signalni mehanizmi delovanja zdravila:
1) prodiranje ligandov, topnih v lipidih, skozi membrano in njihov učinek na znotrajcelične receptorje.
2) signalna molekula se veže na zunajcelično domeno transmembranskega proteina in aktivira encimsko aktivnost njegove citoplazemske domene.
3) signalna molekula se veže na ionski kanal in uravnava njegovo odpiranje.
4) signalna molekula se veže na receptor na celični površini, ki je preko G-proteina vezan na efektorski encim. G-protein aktivira sekundarni sel.
Vrste transmembranske signalizacije:
a) prek receptorjev 1-TMS z aktivnostjo tirozin kinaze in brez nje
b) prek receptorjev 7-TMS, povezanih z G-proteinom
c) skozi ionske kanale (odvisne od liganda, napetostno odvisne, kontaktne vrzeli)
Sekundarni posredniki: cAMP, Ca2 + ioni, DAG, IF3.
Fizikalno-kemijski in kemični mehanizmi delovanja zdravilnih učinkovin.
Glavni farmakološki učinki: 1) narkotični 2) splošni depresivni 3) paralizirajoči 4) lokalno dražeč 5) membranolitično delovanje. Kemijska narava snovi: kemično inertni ogljikovodiki, etri, alkoholi, ... Mehanizem delovanja - reverzibilno uničenje membran.Selektivnost in specifičnost delovanja zdravila. Terapevtski, stranski in toksični učinki zdravil, njihova narava z vidika koncepta receptorjev. Terapevtska strategija za boj proti stranskim in toksičnim učinkom zdravil.
Posebnost– Vezava zdravil s strogo specifično vrsto receptorja.
Selektivnost- je sposoben bolj natančno vezati zdravila na eno ali več vrst receptorjev kot druge.
Bolje je uporabiti izraz selektivnost, saj malo verjetno je, da se katera koli molekula zdravila veže samo na eno vrsto receptorske molekule, saj je število potencialnih receptorjev pri vsakem bolniku astronomsko.
Terapevtsko delovanje- glavni želeni farmakološki učinek, ki se pričakuje od danega farmakološkega pripravka.
Stranski učinki- tiste učinke, ki se pojavijo pri uporabi snovi v terapevtskih odmerkih in predstavljajo spekter njihovega farmakološkega delovanja.
Toksični učinki- neželeni učinki, ki se kažejo pri tem zdravilu, ko zapusti terapevtsko območje.
Razmerja med terapevtskimi in toksičnimi učinki zdravil na podlagi analize receptorsko-efektorskih mehanizmov:
1) terapevtski in toksični učinki, ki jih posreduje isti mehanizem receptor-efektor (prazosin deluje kot alfa-selektivni antagonist na vaskularne SMC receptorje in ima hipotenzivni učinek pri esencialni hipertenziji, vendar pri visokem odmerku lahko bolnik doživi posturalno hipotenzijo)
2) terapevtski in toksični učinki, ki jih posredujejo enaki receptorji, vendar različna tkiva ali različne efektorske poti (srčni glikozidi se uporabljajo za povečanje kontraktilnosti miokarda, hkrati pa motijo delovanje gastrointestinalnega trakta, vid zaradi blokade Na + / K + -ATPaza celične membrane)
3) terapevtski in toksični učinki, ki jih posredujejo različne vrste receptorjev (na primer norepinefrin ima hipertenzivni učinek preko 1-Ar, hkrati pa povzroča tahikardijo preko b1-Ar)
Terapevtska strategija za boj proti terapevtskim in stranskim učinkom zdravil:
1. Zdravilo je treba vedno dajati v najmanjšem odmerku, ki povzroči sprejemljiv terapevtski učinek
2. Zmanjšanje odmerka enega zdravila zaradi imenovanja drugega zdravila s podobnim učinkom, vendar prek različnih receptorjev in z drugačnim profilom toksičnosti.
3. Selektivnost delovanja zdravila lahko povečamo z nadzorovanjem koncentracije zdravila v predelu receptorjev različnih delov telesa (lokalna uporaba zdravil - inhalacijska uporaba salbutamola pri bronhialni astmi)
32. Izrazi in pojmi kvantitativne farmakologije: učinek, učinkovitost, aktivnost, agonist (polni, delni), antagonist. Klinična razlika med konceptoma delovanja in učinkovitosti zdravil.
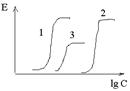 Učinek (odziv)- kvantitativni izkoristek reakcije interakcije celice, organa, sistema ali organizma s farmakološkim sredstvom.
Učinek (odziv)- kvantitativni izkoristek reakcije interakcije celice, organa, sistema ali organizma s farmakološkim sredstvom.
Učinkovitost- merilo reakcije vzdolž osi učinka - velikost odziva biološkega sistema na farmakološki učinek; to je sposobnost zdravila, da zanj zagotovi največji možni učinek... tiste. pravzaprav je to največji učinek, ki ga je mogoče doseči z dajanjem danega zdravila. Številčno označeno z vrednostjo E max. Višji kot je E max, večja je učinkovitost zdravila.
dejavnost- merilo občutljivosti na zdravila vzdolž koncentracijske osi, označuje afiniteto (afiniteto liganda za receptor), kaže, kakšen odmerek (koncentracija) zdravila lahko povzroči razvoj standardnega učinka, enakega 50% največje možno za to zdravilo. Številčno označen z vrednostjo EC 50 ali ED 50. Večja kot je aktivnost zdravila, manjši je odmerek potreben za reprodukcijo terapevtskega učinka.
Učinkovitost: 1 = 2 > 3
Dejavnost: 1> 3> 2
V klinični praksi je bolj pomembno poznati učinkovitost, ne pa aktivnost, ker bolj nas zanima sposobnost zdravil, da povzročijo določen učinek v telesu.
Agonist- ligand, ki se veže na receptor in povzroči biološki odziv, aktivacijo fiziološkega sistema. Popoln agonist- največji odziv, delno- povzročajo manjšo reakcijo, tudi če so vsi receptorji zasedeni.
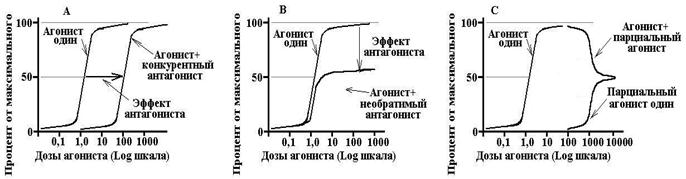 Antagonist- ligandi, ki zasedajo receptorje ali jih spremenijo tako, da izgubijo sposobnost interakcije z drugimi ligandi, sami pa ne povzročijo biološke reakcije (blokirajo delovanje agonistov).
Antagonist- ligandi, ki zasedajo receptorje ali jih spremenijo tako, da izgubijo sposobnost interakcije z drugimi ligandi, sami pa ne povzročijo biološke reakcije (blokirajo delovanje agonistov).
Konkurenčni antagonisti- reverzibilno delujejo z receptorji in tako tekmujejo z agonisti. Povečanje koncentracije agonista lahko popolnoma odpravi učinek antagonista. Kompetitivni antagonist premakne krivuljo odmerka in odziva za agonist, poveča EC 50, ne vpliva na E max.
Nekonkurenčni antagonisti- ireverzibilno spremeni afiniteto receptorjev za agonist, vezava se pogosto ne zgodi z aktivnim mestom receptorja, povečanje koncentracije agonista ne odpravi učinka antagonista. Nekonkurenčni antagonist zmanjša Emax, ne spremeni EC50, krivulja odmerek-učinek pa se stisne okoli navpične osi.
33. Kvantitativni vzorci delovanja zdravil. Zakon padajočega odziva bioloških sistemov. Clarkov model in njegove posledice. Splošni pogled na odvisnost koncentracije - učinek v normalnih in lognormalnih koordinatah.
Clark-Ariens model:
1. Interakcija med ligandom (L) in receptorjem (R) je reverzibilna.
2. Vsi receptorji za dani ligand so enakovredni in neodvisni (njihova nasičenost ne vpliva na druge receptorje).
3. Učinek je neposredno sorazmeren s številom zasedenih receptorjev.
4. Ligand obstaja v dveh stanjih: prost in vezan na receptor.
A), kjer je Kd ravnotežna konstanta, Ke je notranja aktivnost.
B) Ker s povečanjem števila ligandov v nekem trenutku bodo vsi receptorji zasedeni, potem je največje možno število nastalih kompleksov ligand-receptor opisano s formulo:
= [R] × (1)
Učinek je določen z verjetnostjo aktivacije receptorja ob vezavi na ligand, t.j. njegova notranja aktivnost (Ke), torej E = Ke ×. V tem primeru je učinek največji pri Ke = 1 in najmanjši in Ke = 0. Seveda je največji učinek opisan z razmerjem Emax = Ke ×, kjer je skupno število receptorjev za dani ligand
Učinek je torej odvisen tudi od koncentracije liganda na [C] receptorjih
Iz zgornjih razmerij sledi, da je EC 50 = Kd
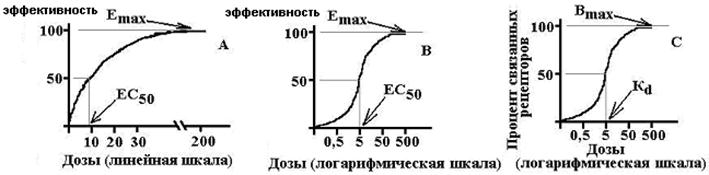
E max je največji učinek, B max je največje število vezanih receptorjev, EC 50 je koncentracija zdravila, pri kateri se pojavi učinek, enak polovici največjega, K d je konstanta disociacije snovi od receptorja, pri na katere je vezanih 50 % receptorjev.
Zakon padajočega odziva ustreza parabolična odvisnost "koncentracija - učinkovitost". Odziv na nizke odmerke zdravil se običajno poveča neposredno sorazmerno z odmerkom... Vendar, ko se odmerek poveča, se povečanje odziva zmanjša in sčasoma je mogoče doseči odmerek, pri katerem ni nadaljnjega povečanja odziva (zaradi zasedenosti vseh receptorjev za dani ligand).
Postopno in kvantno vrednotenje učinka, bistva in klinične uporabe. Kvantifikacija delovanja in učinkovitosti zdravil v eksperimentalni in klinični praksi.
Vse farmakološke učinke lahko v grobem razdelimo v dve kategoriji:
a) postopni (kontinuirani, integralni) učinki- takšni učinki zdravil, ki jih je mogoče kvantitativno izmeriti (učinek antihipertenzivnih zdravil - po ravni krvnega tlaka). Opisana je postopna "krivulja odmerek-učinek" (glej str. 33), na podlagi katere je mogoče oceniti: 1) individualno občutljivost na zdravila; 2) delovanje zdravil; 3) največja učinkovitost zdravila.
b) kvantni učinki- takšni učinki zdravil, ki so diskretna količina, kvalitativna lastnost, t.j. opisuje le nekaj možnosti za stanja (glavobol po jemanju analgetika, bodisi tam ali ne). Opisana je kvantna krivulja odmerek-učinek, kjer je ugotovljena odvisnost manifestacije učinka v populaciji od vrednosti zaužitega odmerka zdravila. Graf odmerka in učinka je v obliki kupole in je identičen Gaussovi krivulji normalne porazdelitve. Na podlagi kvantne krivulje lahko: 1) ocenimo populacijsko občutljivost zdravil; 2) zabeležite prisotnost učinka pri danem odmerku; 3) izberite povprečni terapevtski odmerek.
Razlike med postopnimi in kvantnimi značilnostmi odmerka in učinka:
Kvantitativna ocena aktivnosti in učinkovitosti zdravil temelji na konstrukciji krivulj odmerek-učinek in njihovi kasnejši oceni (glej klavzulo 32).
Vrste delovanja zdravila. Spremembe delovanja zdravil, ko se ponavljajo.
1. Po lokalizaciji: · lokalno - delovanje, ki se pojavi na mestu nanosa zdravila (običajno koža in ... · resorptivno - to je učinek, ki ga ima zdravilo, ko se absorbira v krvni obtok ali neposredno injicira v .. .Odvisnost delovanja zdravil od starosti, spola in posameznih sposobnosti telesa. Pomen cirkadianih ritmov.
· Otroci - področje farmakologije, ki preučuje značilnosti delovanja zdravil na otrokovo telo, se imenuje pediatrična farmakologija ... · starejši ljudje - farmakokinetika ...Spremenljivost in variabilnost delovanja zdravila. Hipo- in hiperreaktivnost, toleranca in tahifilaksija, preobčutljivost in idiosinkrazija. Razlogi za variabilnost delovanja zdravil in racionalne strategije terapije.
Spremenljivost delovanja zdravila – odraža razliko v farmakoloških učinkih enega zdravila pri različnih posameznikih.
Spremenljivost delovanja zdravila - odraža sposobnost zdravila, da ima učinek, ki se razlikuje od njegovih tipičnih farmakoloških učinkov.
Različice variabilnosti in variabilnosti delovanja zdravila:
1. Hiporeaktivnost- zmanjšanje učinka danega odmerka zdravil v primerjavi z učinkom, ki ga opazimo pri večini bolnikov.
2. Hiperreaktivnost- povečanje učinka danega odmerka zdravil v primerjavi z učinkom, ki ga opazimo pri večini bolnikov.
3. Toleranca- zmanjšanje odziva telesa na ponavljajoče se injekcije zdravil; da bi obnovili reakcijo na zdravila, ga je treba dajati v vedno večjih odmerkih.
4. Tahifilaksa- stanje, pri katerem pogosto dajanje zdravil povzroči razvoj tolerance po nekaj urah, pri dovolj redkem dajanju zdravil pa se njegov učinek v celoti ohrani. Razvoj tahifilaksije je običajno povezan z izčrpanjem efektorskih sistemov.
5. Preobčutljivost- razvoj alergijske ali druge imunske reakcije na ponavljajoče se dajanje zdravil.
6. Idiosinkrazija- perverzna reakcija telesa na zdravila, povezana z genetskimi značilnostmi presnove zdravil ali individualno imunološko reaktivnostjo.
Glavni razlogi za variabilnost delovanja zdravila:
1) sprememba koncentracije snovi v receptorskem območju - zaradi razlik v hitrosti absorpcije, njene porazdelitve, presnove, izločanja
2) variacije v koncentraciji endogenega liganda – receptorja – propranolola (β-blokator) upočasni srčni utrip pri ljudeh s povišanimi ravnmi kateholaminov v krvi, ne vpliva pa na srčni utrip v ozadju pri športnikih.
3) spremembe gostote ali delovanja receptorjev.
4) spremembe v reakcijskih komponentah, ki se nahajajo distalno od receptorja.
Strategija racionalne terapije: sestoji iz dejstva, da je za predpisovanje zdravila in za pričakovani učinek potrebno upoštevati posamezne dejavnike telesa (starost, spol itd.), Dnevni ritmi osebe, prisotnost kroničnih bolezni in drugih nepravilnosti. Prav tako je treba predvideti razvoj neznačilnih učinkov ob upoštevanju vseh možne možnosti variabilnost delovanja zdravila.
Ocena varnosti zdravil. Terapevtski indeks in standardne varnostne meje.
Ogromna sredstva se porabijo za ustvarjanje in implementacijo novega zdravila - od 100 do 350 milijonov dolarjev in več. Ti stroški vključujejo delo, porabljeno za ... Da bi prešli vse stopnje ocenjevanja zdravila, morajo ustrezati glavni ... Ocena varnosti novih zdravil se izvaja v dveh fazah:Farmakokinetične interakcije z zdravili (primeri).
Farmakokinetična interakcija zdravil je vrsta farmakološke interakcije, t.j. medsebojno delovanje zdravil, ki se pokaže šele, ko skupaj vstopijo v človeško telo.
Farmakokinetična interakcija se pojavi v fazi absorpcije, porazdelitve in odlaganja, presnove in izločanja.
1. V fazi sesanja- ta vrsta interakcij lahko vodi do povečanja ali zmanjšanja njihove absorpcije. Temu se je mogoče izogniti, če je interval med zdravili vsaj 4 ure.
Ko se zdravilo daje per os, je njegova absorpcija določena z:
· pH medija- neionizirana zdravila se absorbirajo v prebavilih bolje kot ionizirana, zato povečanje pH želodčnega soka poveča absorpcijo šibkih baz in zmanjša absorpcijo šibkih kislin. Primer: antacidi, zaviralci H2-histaminskih receptorjev zavirajo absorpcijo ketokonazola itd. protiglivična zdravila, indirektni antikoagulanti, acetilsalicilna kislina, barbiturati (skoraj popolnoma preprečijo njihov hipnotični učinek); povečanje pH medija izboljša absorpcijo glibutida, pospešuje raztapljanje lupine enterično topnih snovi.
· neposredna interakcija v prebavnem traktu- nastanek kelatnih kompleksov in spojin, ki se ne absorbirajo v prebavilih. P Primeri: aktivno oglje z zdravili tvori netopne spojine, ki preprečujejo njihovo absorpcijo v primeru zastrupitve; tetraciklini medsebojno delujejo s kalcijem, aluminijem, železom, magnezijem, da tvorijo kelatne komplekse, zato se njihova absorpcija zmanjša z uporabo antacidov, bizmutovih pripravkov; fluorokinoloni + antacidi ali sukralfat = zmanjšana učinkovitost antibiotične terapije.
· gibljivost prebavil- lahko povzroči pospeševanje ali upočasnitev absorpcije zdravila. Primeri: prokinetiki (metoklopromid) pospešujejo absorpcijo hitro absorbirajočih zdravil (etanol, paracetamol, tetraciklin) in upočasnijo tiste, ki se počasi absorbirajo (digoksin, cimetidin); odvajala zmanjšajo absorpcijo in biološko uporabnost zdravil; pri jemanju antiholinergičnih zdravil, blokatorjev H 2-histaminskih receptorjev (podaljšanje časa prehoda zdravil skozi prebavila) poveča biološko uporabnost in absorpcijo srčnih glikozidov, pripravkov železa, kar lahko privede do manifestacije toksičnih učinkov.
· črevesna mikroflora- neposredno sodeluje pri absorpciji zdravil, zato se kakršna koli disbioza kaže z motnjami absorpcije zdravil. Primeri: digoksin + eritromicin = povečanje koncentracije digoksina v krvi in razvoj neželenih učinkov; peroralni kontraceptivi + AB širokega spektra = zmanjšan kontracepcijski učinek
· poškodbe črevesnega CO- zavira absorpcijo nekaterih zdravil. Primeri: citostatiki (ciklofosfamid) zavirajo absorpcijo digoksina; motena absorpcija pripravkov železa, cianokobalamina, folne kisline.
V fazi distribucije in depozita
· Konkurenčni premik iz vezi z albuminom krvne plazme - če je zdravilo povezano z beljakovinami manj kot 90 %, potem premik iz vezi z njim ne bo povzročil ... · premik iz vezi z beljakovinami v tkivih: kinidin izpodriva digoksin + ... 3. Na stopnji presnove - zdravila lahko povečajo ali zmanjšajo aktivnost encimskih sistemov, ki sodelujejo pri presnovi zdravil (...V fazi izvalitve
· Spremembe tubularne sekrecije - kinidin + digoksin = povečana koncentracija digoksina v krvi in razvoj toksičnih učinkov (kinidin ... · spremembe tubularne reabsorpcije - samo reabsorpcija je ...Stranski in toksični učinki zdravilnih učinkovin. Teratogeni, embriotoksični, mutageni učinki zdravil. Medicinski in socialni vidiki boja proti odvisnosti od drog, odvisnosti od drog in alkoholizma. Koncept zlorabe snovi.
Stranski učinki- tisti učinki, ki se pojavijo pri uporabi snovi v terapevtskih odmerkih in predstavljajo spekter njihovega farmakološkega delovanja, so lahko primarni in sekundarni:
a) primarni neželeni učinki - kot neposredna posledica učinka tega zdravila na določen substrat (hiposalivacija pri uporabi atropina za odpravo bradiaritmije)
b) sekundarni stranski učinki - posredno nastali neželeni učinki (AB, ki zavira normalno mikrofloro, lahko povzroči superinfekcijo)
Toksični učinki- neželeni učinki, ki se kažejo pri tem zdravilu, ko zapusti terapevtsko območje (preveliko odmerjanje zdravila)
Selektivnost delovanja zdravila je odvisna od njegovega odmerka. Višji kot je odmerek zdravila, manj selektivno postane.
Teratogeno delovanje- sposobnost zdravil pri nosečnici, da povzročijo anatomske nepravilnosti v razvoju ploda (talidomid: fokomelija, antiblastomska zdravila: več okvar)
Embriotoksično delovanje- škodljiv učinek, ki ni povezan s kršitvijo organogeneze v prvih treh mesecih nosečnosti. Kasneje se pojavi fetotoksični učinek.
Mutageni učinek zdravil- poškodba zarodne celice in njenega genetskega aparata zdravil, ki se kaže s spremembo genotipa potomcev (adrenalin, citostatiki).
Rakotvorni učinek zdravil- sposobnost nekaterih zdravil, da inducirajo karcinogenezo.
1) Zasvojenost z mamili- stanje duha in/ali fizično stanje, ki je posledica delovanja zdravil na telo in za katerega so značilne specifične vedenjske reakcije, težko je premagati željo po ponovnem jemanju zdravil, da bi dosegli posebno duševni učinek ali da bi se izognili nelagodju v odsotnosti zdravil v telesu. Za odvisnost od drog je značilno:
a) psihološka odvisnost- razvoj čustvene stiske ob prenehanju jemanja drog. Človek se počuti praznega, pade v depresijo, doživlja občutek strahu, tesnobe, njegovo vedenje postane agresivno. Vsi ti psihopatološki simptomi se pojavijo v ozadju misli o potrebi po injiciranju zdravila, ki je povzročilo odvisnost. Želja po uživanju drog se lahko giblje od preproste želje do strastne žeje po jemanju drog, ki absorbira vse druge potrebe in se spremeni v smisel človekovega življenja. Menijo, da se psihološka odvisnost razvije, ko se človek zave, da lahko optimalno počutje doseže le z uvajanjem drog. Osnova psihološke odvisnosti je človekovo prepričanje v delovanje zdravila (v literaturi so opisani primeri razvoja psihološke odvisnosti od placeba).
b) fizična odvisnost- kršitev normalnega fiziološkega stanja telesa, ki zahteva stalno prisotnost zdravil v njem za vzdrževanje stanja fiziološkega ravnovesja. Prenehanje jemanja zdravila povzroči razvoj specifičnega kompleksa simptomov - odtegnitvenega sindroma - kompleksa duševnih in nevrovegetativnih motenj v obliki disfunkcije v nasprotni smeri od tiste, ki je značilna za delovanje (morfij odpravlja bolečino, zavira dihalni center, zoži zenice, povzroči zaprtje; z odtegnitvenimi simptomi se pri bolniku pojavijo hude bolečine, pogosto hrupno dihanje, zenice so razširjene in se razvije vztrajna driska)
v) toleranca... Toleranca do zdravil, ki povzročajo odvisnost od drog, je pogosto medsektorska, t.j. ne nastane le za dano kemično spojino, ampak za vse strukturno podobne spojine. Na primer, pri bolnikih z odvisnostjo od zdravil od morfija se toleranca ne pojavi le do njega, ampak tudi do drugih opioidnih analgetikov.
Za razvoj odvisnosti od drog prisotnost vseh 3 meril ni nujen pogoj.
Opioidi, barbiturati, alkohol povzročajo močno fizično in psihično odvisnost ter toleranco. Anksiolitiki (diazepam, alprazolam) povzročajo predvsem psihološko odvisnost.
2) Zasvojenost (odvisnost od drog)- To je izredno huda oblika odvisnosti od drog, kompulzivne uporabe drog, za katero je značilna vedno večja, neustavljiva želja po dajanju tega zdravila, povečanju njegovega odmerka. Kompulzivnost želje pomeni, da potreba po dajanju zdravila prevladuje nad vsemi drugimi (celo vitalnimi) potrebami bolnika. S stališča te definicije je hrepenenje po morfiju odvisnost od drog, medtem ko je hrepenenje po nikotinu odvisnost od drog.
3) Odvisen od medicine- zaznamuje manj intenzivno hrepenenje po zdravilih, ko zavrnitev zdravila povzroči le občutek rahlega nelagodja, brez razvoja fizične odvisnosti ali podrobne slike psihične odvisnosti. To Zasvojenost zajema tisti del odvisnosti od drog, ki ne ustreza definiciji odvisnosti. Na primer, prej omenjena odvisnost od nikotina je oblika odvisnosti.
4) Zloraba drog- nedovoljena uporaba zdravil v takih odmerkih in na načine, ki se razlikujejo od sprejetih zdravstvenih ali socialnih standardov v določeni kulturi in v določenem času. To zloraba drog zajema samo družbene vidike uživanja drog. Primer zlorabe je uporaba anaboličnih steroidov v športu ali za izboljšanje postave s strani mladih moških.
5) Alkoholizem- kronična zloraba alkohola (etilnega alkohola), ki danes vodi v okvare številnih organov (jetra, prebavila, centralni živčni sistem, srčno-žilni sistem, imunski sistem) in jo spremlja psihofizična odvisnost.
6) Zloraba substanc- kronična zloraba različnih drog (vključno z drogami, alkoholom, halucinogeni), ki se kaže v različnih duševnih in somatskih motnjah, vedenjskih motnjah, socialni degradaciji.
Zdravljenje odvisnosti od drog težka in nehvaležna naloga. Do sedaj ni bila ustvarjena učinkovita metoda, ki bi zagotovila uspešnost zdravljenja pri več kot 30-40 % bolnikov. Doseganje vidnih rezultatov je možno le ob popolnem sodelovanju bolnikov, zdravnika in družbenega okolja, v katerem je bolna oseba (načelo prostovoljnosti in individualnosti). Sodobne tehnike temeljijo na naslednjih načelih:
Psihoterapevtske in delovnoterapevtske metode;
Skupinsko zdravljenje in rehabilitacija (Društvo anonimnih alkoholikov, odvisnikov od drog)
Postopna ali nenadna ukinitev zdravila med razstrupljevalno terapijo
Nadomestno zdravljenje (zamenjava narkotika s počasnimi in dolgodelujočimi analogi z njihovo kasnejšo odpovedjo; na primer program metadonske nadomestne terapije za odvisnike od heroina)
Zdravljenje s specifičnimi antagonisti (nalokson in naltrekson) ali sredstvi za preobčutljivost (teturam)
Nevrokirurške metode kriodestrukcije cingularnega vijuga in hipokampusa
42. Interakcije s farmacevtskimi zdravili. Opozorila in previdnostni ukrepi za tekočinsko terapijo.
Farmacevtske interakcije - vrsta interakcije, ki je povezana s fizikalno-kemijsko reakcijo med zdravili med izdelavo zdravila, še pred vnosom teh učinkovin v človeško telo
a) tipične napake, ki vodijo v farmacevtsko nezdružljivost: pisanje zapletenih receptov, nepravilno shranjevanje, možnost adsorpcije zdravil na površini plastike (organski nitrati) se ne upošteva
b) težave z infuzijsko terapijo: mešanje topnih soli, derivatov netopnih šibkih kislin ali baz vodi do njihove precipitacije; v tekočih dozirnih oblikah se srčni glikozidi in alkaloidi hidrolizirajo, AB se uniči; pH medija (alkaloidi se oborijo v alkalnem mediju)
c) priporočila: 1) Vse mešanice je bolje pripraviti ex tempore 2) Najbolj zanesljiva rešitev je z enim zdravilom 3) Vse raztopine je treba pred uporabo preveriti glede suspenzije 4) Do interakcije lahko pride brez vidnih sprememb v raztopinah 5) Zdravila ne morejo dodajati v kri in raztopine AK 6) Če ni posebnih navodil, je treba pripravke raztopiti v 5 % raztopini glukoze (pH 3,5-6,5), izotonični raztopini NaCl (pH 4,5-7,0).
Raztopina glukoze, stabilizirana s HCl, ni združljiva z epinefrinom, benzilpenicilinom, apomorfinom, kanamicinom, vitaminom C, oleandomicinom, srčnimi glikozidi. Srčni glikozidi so nezdružljivi z atropinom, papaverinom, platifilinom. AB so nezdružljivi s heparinom, hidrokortizonom. Vitamini skupine B so med seboj nezdružljivi, z vitamini PP, C. Tudi vitamini PP in C so med seboj nezdružljivi.
Ne sme se mešati z drugimi zdravili: fenotiazidom, klorpromazinom, barbiturati, pripravki vitamina C, amfotericinom B, furosemidom, sulfadiazinom, aminofilinom, adrenomimetiki.
Vrste farmakoterapije. Deontološki problemi farmakoterapije.
1. etiotropni PT - popravek in odprava vzroka bolezni (AB pri nalezljivih boleznih) 2. patogenetski PT - vpliv na mehanizem razvoja bolezni (zaviralci ... 3. simptomatski PT - odprava simptomov bolezni, če je to nemogoče vplivati na njegov vzrok ali patogenezo (NSAID ...Osnovna načela zdravljenja in preprečevanja zastrupitve z zdravili. Antidotna terapija (primeri).
Razvrstitev strupenih snovi (OM):
1. Po pripadnosti določenim razredom kemičnih spojin: barbiturati, benzodiazepini, cianidi.
2. Po izvoru: nebiološke narave (kisline, alkalije, soli težkih kovin), strupeni odpadni produkti nekaterih MB (botulinum toksin), rastlinskega izvora (alkaloidi, glikozidi), živalskega izvora (kačji in čebelji strup)
3. Glede na stopnjo strupenosti: a) izjemno strupeno (DL50< 1 мг/кг) б) высоко токсические (1-50) в) сильно токсические (50-500) г) умеренно токсические (500-5000) д) мало токсические (5000-15000) е) практически нетоксические (> 15.000)
4. Po toksikološkem učinku: a) živčno-paralitični (bronhospazem, dispneja) b) kožno resorptivni c) splošno toksični (hipoksični krči, koma, paraliza) d) zadušljiv e) solzni in dražilni e) psihotropni (oslabljena duševna aktivnost, )
5. Glede na področje prednostne uporabe: industrijski strupi, pesticidi, gospodinjski strupi, kemična bojna sredstva, zdravilne snovi.
6. Glede na strupenost zdravil: Seznam A - zdravila, katerih namen, uporabo, odmerjanje in shranjevanje je treba zaradi visoke toksičnosti izvajati zelo previdno. Na istem seznamu so tudi zdravila, ki povzročajo odvisnost od drog; seznam B - zdravila, katerih imenovanje, uporabo, odmerjanje in shranjevanje je treba izvajati previdno v zvezi z možnimi zapleti pri njihovi uporabi brez zdravniškega nadzora.
Selektivno toksični učinek zdravil.
a) kardiotoksični: srčni glikozidi, kalijevi pripravki, antidepresivi
b) nevrotoksični: psihofarmakološka sredstva, oksikinolini, aminoglikozidi
c) hepatotoksični: tetraciklini, kloramfenikol, eritromicin, paracetamol
d) nefrotoksični: vankomicin, aminoglikozidi, sulfonamidi
e) gastroenterotoksični: steroidna protivnetna zdravila, nesteroidna protivnetna zdravila, rezerpin
f) hematotoksični: citostatiki, kloramfenikol, sulfonamidi, nitrati, nitriti
g) pnevmotoksični
Toksikokinetika - preučuje absorpcijo, porazdelitev, presnovo in izločanje zdravil, zaužitih v toksičnih odmerkih.
Vnos strupenih snovi v telo je možen a) enteralno b) parenteralno. Hitrost in popolnost absorpcije odražata hitrost razvoja toksičnega učinka in njegovo resnost.
Porazdelitev v telesu: Vd = D / Cmax - dejanski volumen, v katerem je strupena snov porazdeljena v telesu. Vd> 5-10 l / kg - OM je težko prenašati njegovo odstranitev (antidepresivi, fenotiazini). Vd< 1 л/кг – ОВ легче удалить из организма (теофиллин, салицилаты, фенобарбитал).
Preveliko odmerjanje- spremembe v farmakokinetičnih procesih: topnost, povezava z beljakovinami, presnova ® znatno povečanje proste frakcije zdravil ® toksični učinek.
Kinetika prvega reda se s povečanjem koncentracije zdravila spremeni v kinetiko ničelnega reda.
Toksigena faza je detoksikacijska terapija, somatogena faza je simptomatska terapija.
Toksikodinamika . Glavni mehanizmi toksičnega delovanja:
a) mediator: neposredni (po vrsti kompetitivne blokade - FOS, psihomimetiki) in posredni (aktivatorji ali zaviralci encimov)
b) interakcija z biomolekulami in znotrajceličnimi strukturami (hemolitične snovi)
c) presnova po vrsti smrtonosne sinteze (etilni alkohol, tiofos)
d) encimski (kačji strupi itd.)
Vrste delovanja: lokalno, refleksno, resorptivno.
Razvrstitev zastrupitve:
1. Etiopatogenetika:
a) nenamerno (samozdravljenje, napačen sprejem)
b) namerno (z namenom samomora, umora, razvoja nemočnega stanja pri žrtvi)
2. Klinična:
a) odvisno od stopnje razvoja zastrupitve: akutna (zaužitje enkratnega odmerka ali s kratkim časovnim intervalom toksičnega odmerka snovi), subakutna (zapozen razvoj klinične slike po enkratnem odmerku), kronična
b) odvisno od manifestacije glavnega sindroma: poškodba CVS, poškodba DS itd.
c) odvisno od resnosti bolnikovega stanja: blaga, zmerna, huda, izredno huda
3. Nozološki: upošteva ime zdravila, ime skupine snovi
Splošni mehanizem smrti v primeru zastrupitve:
a) poraz CVS:
1) znižanje krvnega tlaka, hipovolemija perifernih žil, kolaps, bradi- ali tahikardija (triciklični antidepresivi, zaviralci beta, zaviralci kalcijevih kanalčkov)
2) aritmije (ventrikularna tahikardija, fibrilacija - triciklični antidepresivi, teofilin, amfetamin)
b) poškodbe centralnega živčnega sistema: stupor, koma ® depresija dihanja (zdravila, barbiturati, alkohol, hipno-sedativna zdravila)
c) konvulzije, mišična hiperreaktivnost in rigidnost ® hipertermija, mioglobinurija, odpoved ledvic, hiperkaliemija
Toksikološka triada:
1) trajanje uporabe, odmerek in anamneza snovi ®.
2) ocena stanja zavesti po simptomih: dihanje, krvni tlak, telesna temperatura
3) laboratorijski podatki
Osnovna načela zdravljenja:
JAZ. Prva pomoč: umetno dihanje, masaža srca, anti-šok terapija, nadzor vodno-elektrolitnega ravnovesja
II. Zakasnjena absorpcija in odstranitev neabsorbiranega OM iz telesa:
Namen: prekiniti stik z OV
1. Parenteralna pot:
a) skozi pljuča:
1) ustavite vdihavanje
2) dražilne snovi (amoniak, formaldehid) ® za utrjevanje aktivnih gibov, ogrevanje, dajanje kisika in penilcev (za amoniak je sredstvo proti peni kis, za formaldehid pa razredčena raztopina amoniaka)
b) skozi kožo: sperite z veliko količino tople vode z milom ali detergentom, specifičnimi protistrupi, nevtralizacija in prenehanje izpostavljenosti OM na koži (FOS: sperite z vodo, odstranite z 10-15% amoniakom ali 5- 6 % raztopina natrijevega bikarbonata z vodo; fenolkrezol: rastlinsko olje ali etilen glikol, vendar ne vazelinsko olje, KMNO 4: 0,5-1 % raztopina askorbinske kisline ali enake količine 3 % vodikovega peroksida in 3 % raztopine ocetne kisline, CCl 4, terpentin , bencin: topla milnica)
c) pri injiciranju v okončino: podvezek nad mestom injiciranja
d) v primeru stika z očmi: izpirati s toplo fiziološko raztopino ali mlekom 10-20 minut, nakapati lokalni anestetik; v primeru stika s kislinami in alkalijami jih ni mogoče nevtralizirati. Potreben je posvet z oftalmologom.
2. Enteralna pot: osvoboditi želodec pred OM, pospešiti prehod
a) odstranitev OM:
1) predhodni vnos vode. Ne jemljite mleka (z izjemo jedkih strupenih snovi) in etanola (z izjemo metanola).
2) bruhanje - indicirano predvsem v primeru zastrupitve z velikimi tabletami ali kapsulami, ki ne morejo preiti skozi sondo. Lahko se izzove zaradi refleksa ali bruhanja (NaCl: 1 žlica na 1 kozarec vode; Ipecakov sirup: odrasli 2 žlici, otroci 2 žlički; gorčica: 1-2 žlički na kozarec vode; apomorfin: 5-10 mg/kg subkutano, razen za otroke, mlajše od 5 let). Ne povzročajte bruhanja po zaužitju: organska topila - nevarnost vdihavanja, detergenti - penjenje, konvulzivne snovi - nevarnost aspiracije, jedke snovi - poškodbe požiralnika)
3) sonda izpiranje želodca - je nujen in obvezen ukrep. Želodec se opere, če od zastrupitve ni minilo več kot 4-6 ur, včasih tudi do 10 ur; v primeru zastrupitve z acetilsalicilno kislino - po 24 urah. Pacienta predhodno intubiramo s cevko z napihljivo manšeto: v komi brez kašlja in laringealnega refleksa. Želodec speremo z vodo ali fiziološko raztopino 30 ° C, postopek traja 4 ure ali več. Na koncu pranja dodamo aktivno oglje in natrijev sulfat.
b) zmanjšanje absorpcije iz prebavil: aktivno oglje v notranjosti po praznjenju želodca + natrijev ali magnezijev sulfat. Značilnosti ukrepov za zmanjšanje absorpcije:
1) organska topila: ne povzročajte bruhanja, izpiranje želodca po intubaciji, aktivno oglje + tekoči parafin
2) detergenti: ne povzročajte bruhanja in izpirajte želodec, potrebno je dati veliko vode + sredstva proti penjenju (simetikon)
3) kisline in alkalije: bruhanja ni mogoče izzvati, izpiranje želodca skozi cevko, namazano z rastlinskim oljem po dajanju narkotičnega analgetika, je edina indikacija za dajanje mleka. Za zastrupitev s kislino - antacidi, za alkalno zastrupitev - citronska ali ocetna kislina.
III. Odstranitev absorbiranega OM iz telesa
a) prisilna diureza (pogoji: zadosten ledvični pretok krvi in glomerularna filtracija; vlijte 20-25 litrov v 24 urah)
b) peritonealna hemodializa
c) hemosorpcija
d) izmenjava transfuzije krvi
e) prisilna hiperventilacija
IV. Simptomatsko zdravljenje funkcionalnih motenj.
2) toksikokinetični - pospešujejo biotransformacijo OM (trimedoksim bromid, natrijev tiosulfat, etanol, AO) 3) farmakološki - atropin, nalokson 4) imunološki antidotiPravila za predpisovanje strupenih, narkotičnih in močnih zdravil.
Recepti za narkotične snovi (morfij, omnopon, promedol, fenamin, kokain itd.) in z njimi izenačene, ne glede na droge. f-mi smo predpisani za posebne ... V primeru, da je lek. Poročna vsebina. alkohola, nato se pečat položi. institucije »Za ... V primerih, ko je maks. odmerek strupenega ali močnega. in-in presegati, zahtevano. navedite njihovo število z besedami z dodatkom ...Kaj bomo naredili s prejetim materialom:
Če se vam je to gradivo izkazalo za koristno, ga lahko shranite na svojo stran na družbenih omrežjih:








