Активный центр белка и взаимодействие его с лигандом. Активный центр белка и его взаимодействие с лигандом
В основе функционирования любого белка лежит его способность к избирательному взаимодействию с каким-либо другим веществом - лигандом. Лигандом может быть как низкомолекулярное вещество, так и макромолекула, в том числе другой белок. Лиганд присоединяется к определенному участку на поверхности белковой молекулы - центру связывания (активный центр).
Специфичность взаимодействия (узнавания) чаще всего обеспечивается комплементарностью структуры центра связывания структуре лиганда, подобно тому, как это происходит при самосборке гемоглобина из протомеров. Иногда избирательность зависит в основном от реакционной способности атома, к которому непосредственно присоединяется лиганд. Примером может служить присоединение кислорода к атому железа в миоглобине или гемоглобине. Однако и в таких случаях избирательность в значительной мере зависит от белковой части молекулы. Такой же атом железа (в составе гема) в других белках - цитохромах - функционирует совершенно иначе: он служит переносчиком электронов, получая их от одних веществ и передавая другим (при этом железо попеременно становится двух- или трехвалентным).
Связи между белком и лигандом могут быть как ковалентными, так и некова-лентными.
Центр связывания иногда занимает небольшой участок поверхности белковой молекулы (в гемоглобине центр связывания кислорода - это только область атома железа), иногда - значительную часть поверхности (например, контактные поверхности протомеров гемоглобина).
На молекуле белка может быть один, два или больше активных центров, имеющих одинаковую или разную специфичность. Например, каждый протомер гемоглобина имеет три центра для связывания с тремя другими протомерами и один центр для связывания гема. Тетрамерная молекула гемоглобина имеет четыре активных центра (атомы железа) для связывания кислорода.
Активный центр формируется из аминокислотных остатков, зачастую отстоящих далеко друг от друга в пептидной цепи. Собранными в одном месте они оказываются в результате образования вторичной и третичной структуры. Поэтому при денатурации белков активные центры разрушаются и биологическая активность утрачивается.Образование комплекса можно наблюдать по убыли концентрации свободного лиганда L или но нарастанию концентрации комплекса PL, если его образование сопровождается появлением какого-либо нового свойства, например изменением цвета или поглощения в ультрафиолетовой части спектра. Такой способ используют и для количественного определения индивидуальных белков (см. ниже).
При постоянной концентрации Р и возрастающей концентрации L концентрация PL увеличивается по гиперболической кривой, стремясь к максимуму, когда весь белок связан с лигандом (кривая насыщения). Для олигомерных белков кривая насыщения может иметь S-образную форму. Степень насыщения можно выразить в процентах концентрации комплекса от начальной (до добавления лиганда) концентрации белка [Р]0: степень насыщения равна (/[Р]0) 100 (рис. 1.29; см. также рис. 1.26).
Из уравнения равновесия реакции следует, что если [Р] = , то К = [L]. Равенство [Р] и означает полунасыщение белка, т. е. состояние, когда 50 % молекул белка связаны с лигандом, а 50 % остаются свободными: [Р] = = 1/ Последовательно, Ктсс численно равна такой концентрации лиганда, при которой достигается полунасыщение белка. На рис. 1.29 показано, как по кривой насыщения можно определить К и, тем самым, оценить сродство лиганда к белку.
Активный центр белка – это центр связывания белка с лигандом. На поверхности глобулы образуется участок, который может присоединять к себе другие молекулы называемые лигандами . Активный центр белка формируется из боковых групп аминокислот, сближенных на уровне третичной структуры. В линейной последовательности пептидной цепи они могут находиться на расстоянии значительно удаленном друг от друга. Белки проявляют высокую специфичность при взаимодействии с лигандом. Высокая специфичность взаимодействия белка с лигандом обеспечивается комплементарностью структуры активного центра белка структуре лиганда. Комплементарность – это пространственное и химическое соответствие взаимодействующих молекул. Центры связывания белка с лигандом часто располагаются между доменами (например, центр связывания трипсина с его лигандом имеет 2 домена разделенных бороздкой).
В основе функционирования белков лежит их специфическое взаимодействие с лигандами. 50000 индивидуальных белков, содержащих уникальные активные центры, способные связываться только со специфическими лигандами и, благодаря особенностям строения активного центра, проявлять свойственные им функции. Очевидно, в первичной структуре содержится информация о функции белков.
Четвертичная структура - это высший уровень структурной организации, возможный не у всех белков. Под четвертичной структурой понимают способ укладки в пространстве полипептидных цепей и формирование единого в структурном и функциональном отношениях макромолекулярного образования. Каждая отдельно взятая полипептидная цепь, получившая название протомера или субъединицы , чаще всего не обладает биологической активностью. Эту способность белок приобретает при определенном способе пространственного объединения входящих в его состав протомеров. Образовавшуюся молекулу принято называть олигомером (мультимером) .
Четвертичную структуру стабилизируют нековалентные связи, которые возникают между контактными площадками протомеров, которые взаимодействуют друг с другом по типу комплементарности.
К белкам, имеющим четвертичную структуру, относятся многие ферменты (лактатдегидрогеназа, глутаматдегидрогеназа и др.), а также гемоглобин, сократительный белок мышц миозин. Одни белки имеют небольшое число субъединиц 2 – 8, другие сотни и даже тысячи субъединиц. Например, белок вируса табачной мозайки имеет 2130 субъединиц.
Типичным примером белка, имеющего четвертичную структуру, является гемоглобин. Молекула гемоглобина состоит из 4 субъединиц, т. е. полипептидных цепей, каждая из которых связана с гемом, из них 2 полипептидные цепи называются -2афьла и -2бета Они различаются первичной структурой и длиной полипептидной цепи.
Связи, образующие четвертичную структуру менее прочные. Под влиянием некоторых агентов происходит разделение белка на отдельные субъединицы. При удалении агента субъединицы могут вновь объединиться и биологическая функция белка восстанавливается. Так при добавлении к раствору гемоглобина мочевины он распадается на 4 составляющие его субъединицы, при удалении мочевины структурная и функциональная роль гемоглобина восстанавливается.
Конец работы -
Эта тема принадлежит разделу:
Биохимия. Белки. Аминокислоты - структурные компоненты белков
Белки аминокислоты структурные компоненты белков.. белки.. белки это азотсодержащие высокомолекулярные органические соединения состоящие из аминокислот соединенных в цепи с..
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ:
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Все темы данного раздела:
Механизм действия ферментов
Согласно современным представлениям при взаимодействии фермента с субстратом условно можно выделить 3 стадии:
1 стадия характеризуется диффузией субстрата к фермен
Кислотно-основный катализ
В активном центре фермента содержатся группы кислотного и основного типа. Группы кислотного типа отщепляют Н+ и имеют отрицательный заряд. Группы основного типа присоединяют Н+ и имеют поло
А). Гипотеза Фишера
Согласно ей имеется строгое стерическое соответствие субстрата и активного центра фермента. По Фишеру, фермент - это жёсткая структура, а субстрат является как бы слепком его активного цент
Обмен углеводов
ОБМЕН УГЛЕВОДОВ
1. Основные углеводы животного организма, их биологическая роль.
2. Превращение углеводов в органах пищеварительной системы.
3. Биосинтез и распад
Биологическая роль углеводов
БИОЛОГИЧЕСКАЯ РОЛЬ УГЛЕВОДОВ:
1. ЭНЕРГЕТИЧЕСКАЯ.
При окислении1 г углеводов до конечных продуктов (СО2 и Н2О) выделяется 4,1-ккал энергии. На долю углеводов приходится около 60-70
Превращение углеводов в пищеварительном тракте
ПРЕВРАЩЕНИЕ УГЛЕВОДОВ В
ПИЩЕВАРИТЕЛЬНОМ ТРАКТЕ
Основными углеводами пищи для организма человека являются: крахмал, гликоген, сахароза, лактоза.
Поступивший с пищей крахма
Биосинтез и распад гликогена
БИОСИНТЕЗ И РАСПАД ГЛИКОГЕНА В ТКАНЯХ.
ГЛИКОГЕНОВЫЕ БОЛЕЗНИ.
Было установлено, что гликоген может синтезироваться практически во всех органах и тканях. Однако наибольшая его конце
Анаэробный гликолиз
В зависимости от функционального состояния организма, клетки органов и тканей могут находиться как в условиях достаточного снабжения кислородом, так и испытывать его недостаток, то
Аэробный гликолиз (гексозодифосфатный путь)
ГЕКСОЗОДИФОСФАТНЫЙ ПУТЬ.
Это классический путь аэробного катаболизма углеводов в тканях протекает в цитоплазме до стадии образования пирувата и завершается в митохондриях с образование кон
Гексозомонофосфатный путь
ГЕКСОЗОМОНОФОСФАТНЫЙ ПУТЬ ПРЕВРАЩЕНИЯ ГЛЮКОЗЫ
В ТКАНЯХ, ХИМИЗМ РЕАКЦИЙ.
Окисление глюкозы по этому пути протекает в цитоплазме клеток и представлено двумя последовательными ветвям
Глюконеогенез
ГЛЮКОНЕОГЕНЕЗ
Основными источниками глюкозы для организма человека являются:
1. углеводы пищи;
2. гликоген тканей;
3. глюконеогенез.
ГЛЮКОНЕОГЕНЕЗ - это
Основные липиды организма человека их биологическая роль
ЛИПИДАМИ называются сложные органические вещества биологической природы нерастворимые в воде, но растворимые в органических растворителях.
ЛИПИДЫ являются основным продуктом питания. Они п
Переваривание липидов, ресинтез жира
Переваривание липидов.
Поступающие с пищей ЛИПИДЫ в ротовой полости подвергаются только механической переработке. ЛИПОЛИТИЧЕСКИЕ ферменты в ротовой полости не образуются. Переваривание жир
Липопротеины крови
ЛИПИДЫ являются нерастворимыми в воде соединениями, поэтому для их переноса кровью необходимы специальные переносчики, которые растворимы в воде. Такими транспортными формами являются ЛИПОПРОТЕИНЫ.
Окисление высших жирных кислот
Жировая ткань, состоящая из адипозоцитов, выполняет специфическую роль в липидном обмене. Около 65% массы жировой ткани приходится на долю отложенных в ней триацилглицеролов (ТАГ) - они представляю
Биосинтез вжк в тканях
Биосинтез ВЖК происходит в эндоплазматической сети клеток. Заменимые ВЖК (все предельные и непредельные, имеющих одну двойную связь) синтезируются в клетках из АЦЁТИЛ-КоА.
Условиями для би
Обмен холестерина
Обмен холестерина.
Холестерин является предшественником в синтезе стероидов: желчных кислот, стероидных гормонов, витамина D3.Холестерин является обязательным структурным компон
Переваривание белков
Переваривание белков в пищеварительном тракте
Пищевые белки подвергаются гидролитическому расщеплению под действием ПРОТЕОЛИТИЧЕСКИХ ФЕРМЕНТОВ (класс – гидролазы, подкласс - пептидазы).
Гниение аминокислот, обезвреживание продуктов гниения
ГНИЕНИЕ АМИНОКИСЛОТ
Аминокислоты, которые не подверглись всасыванию, поступают в толстую кишку, где подвергаются гниению. ГНИЕНИЕ АМИНОКИСЛОТ - это процесс распада аминокислот под действие
Метаболизм аминокислот
Метаболизм аминокислот
Источниками аминокислот в клетке являются:
1. белки пищи после их гидролиза в органах пищеварения;
2. синтез заменимых аминокислот;
Пути обезвреживания аммиака
Аммиак образуется из аминокислот при распаде других азотсодержащих соединений (биогенных аминов, НУКЛЕОТИДОВ). Значительная часть аммиака образуется в толстой кишке при гниении. Он всасывается в кр
Регуляция обмена веществ
СИГНАЛЬНЫЕ МОЛЕКУЛЫ.
Основные задачи регуляции метаболизма и клеточных функций:
1. внутриклеточное и межклеточное согласование обменных процессов;
2. исключение «холостых
Гормоны гипоталамуса
ГОРМОНЫ ГИПОТАЛАМУСА
ГИПОТАЛАМУС является компонентом и своеобразным «выходным каналом» лимбической системы.
Это отдел промежуточного мозга, контролирующий различные параметры гом
Гормоны гипофиза
Гормоны гипофиза
ГОРМОНЫ ГИПОФИЗА
В гипофизе выделяют переднюю (аденогипофиз) и заднюю доли (нейрогипофиз).
Гормоны аденогипофиза можно разделить на 3 группы в зави
Биосинтез йодтиронинов
Синтез йодтиронинов происходит в составе белка – тиреоглобулина, который находится в фолликулах щитовидной железы. Тиреоглобулин представляет собой гликопротеин, содержащий 115 остатков тирозина. П
Обмен липидов
В печени жировой ткани гормоны стимулируют липолиз. Указанные эффекты на обмен углеводов и липидов связывают с повышением чувствительности клеток к действию адреналина под влиянием тиреоидных гормо
Гипосекреция
В детском возрасте снижение секреции приводит к задержке физического и умственного развития (кретинизм).
У взрослых тяжелым проявлением недостатка гормонов щитовидной железы является миксе
Гиперсекреция
Диффузный токсический зоб (базедова болезнь) наиболее распространенное заболевание, сопровождающееся повышенной продукцией йодтиронинов. При этом заболевании размеры щитовидной железы увеличены и р
Гормоны паращитовидных желез
Паратгормон синтезируется в паращитовидных железах и состоит из 84 аминокислотных остатков. Гормон хранится в секреторных гранулах. Секреция ПТГ регулируется уровнем кальция в крови: при сни
Гормоны половых желез
Гормоны половых желез
По химической природе представляют собой стероиды. Выделяют:
1. Андрогены;
2. Эстрогены;
3. Прогестины.
Гормоны надпочечников
Гормоны надпочечников
Надпочечники – железы внутренней секреции, в которых выделяют корковое и мозговое вещество. В корковом слое синтезируется гормоны стероидной природы, в мозгово
Гормоны поджелудочной железы
Гормоны поджелудочной железы
Функции поджелудочной железы:
· экзокринная;
· эндокринная.
Экзокринная функция заключается в синтезе и секреции пищеварительных фер
Экзаменационные вопросы
ФАРМАЦЕВТИЧЕСКИЙ ФАКУЛЬТЕТ (ЗАОЧНОЕ ОТДЕЛЕНИЕ)
Экзаменационные вопросы по биологической химии
для студентов 3 курса (6 семестр)
1. Биохимия, ее задачи. Связь биохимии с ф
Водородные связи, силы Ван дер Ваальса. Связывание или ассоциация лиганда с рецептором (так называемый «докинг» лиганда в специфическую «нишу» в рецепторе) обычно обратима и кратковременна. Обратный процесс называется диссоциацией лиганда из связи с рецептором. Необратимое ковалентное связывание лиганда с рецептором или другой молекулярной мишенью для данного лиганда является редкостью в биологических системах, по крайней мере в физиологических условиях. Однако искусственные, экзогенные лиганды, необратимо ковалентно связывающиеся с молекулами-мишенями, конечно, существуют, и даже имеют важное значение в медицине, как, например, необратимо алкилирующие ДНК противоопухолевые препараты алкилирующего типа или необратимо инактивирующие МАО антидепрессанты группы ИМАО, или необратимо инактивирующий α-адренорецепторы феноксибензамин. В отличие от принятого определения лиганда в металлоорганической и неорганической химии, для процесса взаимодействия лиганда с биомолекулами-мишенями совершенно неважно (и не требуется), чтобы лиганд взаимодействовал именно с металлом-кофактором в составе биологической молекулы (тем более что не все биологические молекулы содержат металлы в качестве кофакторов). Связывание лиганда именно с металлосодержащим сайтом биологической молекулы, тем не менее, в биологических системах часто встречается и имеет важное биологическое значение и для транспортных белков, таких, как гемоглобин (транспортирующий кислород , углекислый газ и способный транспортировать также другие эндогенные газы, в частности эндогенный угарный газ , эндогенный сероводород и эндогенный оксид серы (IV)), и для каталитических ферментов , многие из которых являются металлоферментами (содержат в составе активного каталитического центра ион того или иного металла в координационном комплексе с белком).
Лиганды, которые связываются с рецепторами, однако не могут или почти не могут активировать рецептор (вернее делают это с пренебрежимо малой вероятностью) и соответственно сами по себе не могут вызывать и не вызывают физиологического ответа рецепторной системы, а лишь предотвращают связывание как агонистов, так и обратных агонистов, и физиологический ответ на них, называются антагонистами .
В примере, показанном слева, кривые зависимости «доза-эффект» показаны для двух лигандов с разной степенью сродства к рецептору (разной аффинностью к нему). Связывание лиганда с рецептором часто характеризуют в терминах того, какая концентрация лиганда требуется для того, чтобы занять 50 % от всех доступных участков связывания рецепторов - так называемая IC 50 . Величина IC 50 связана с константой диссоциации K i , но отличается от неё. Она отличается также и от величины EC 50 , поскольку занятие 50 % доступных рецепторов вовсе не обязательно приводит к продуцированию 50 % от максимального физиологического ответа для данного агониста, или 50 % от максимального физиологического ответа «вообще» (IC 50 может быть как больше, так и меньше EC 50 , в зависимости от особенностей регуляции конкретной физиологической рецепторной системы - существуют как рецепторные системы, в которых занятие относительно малого количества рецепторов производит большой физиологический эффект, так и, наоборот, системы, в которых для создания значительного физиологического эффекта нужно занять большой процент доступных рецепторов, причём зависимость величины физиологического эффекта от процента занятости рецепторов, так же как и от дозы агониста, вовсе не обязана быть линейной). Лиганд, кривая зависимости «доза-эффект» для которого изображена красной линией, имеет более высокую степень сродства к рецептору (большую аффинность связывания), чем лиганд, кривая для которого изображена зелёной линией. Если оба лиганда присутствуют одновременно, то больший процент высокоаффинного (имеющего более высокое сродство к рецептору) лиганда будет связано с доступными сайтами связывания рецептора, по сравнению с менее аффинным лигандом. Этот механизм объясняет, в частности, то, почему оксид углерода (II) даже в низких концентрациях может конкурировать с кислородом за связывание с гемоглобином , являясь более высокоаффинным (имеющим большее сродство к гемоглобину) «агонистом» этого транспортного белка, и почему это часто приводит к отравлению угарным газом.
Аффинность связывания лиганда с рецептором (степень сродства лиганда к рецептору) чаще всего определяют с использованием метода вытеснения меченого радиоактивного лиганда (называемого «горячим лигандом») исследуемым лигандом (называемым «холодным», или «тестовым» лигандом). Эксперименты по гомологичному конкурентному связыванию лиганда с рецептором представляют собой эксперименты, в которых «горячий» (меченый радиоактивной меткой) и «холодный» (не помеченный) лиганд - это одно и то же химическое вещество, и они конкурируют между собой за доступные участки связывания с рецептором. Существуют также методы без использования радиоактивной метки, такие, как поверхностный плазмонный резонанс, двойная поляризационная интерферометрия. Эти методы позволяют определить не только аффинность (степень сродства) агониста к рецептору, но и кинетику его ассоциации и диссоциации из связи с рецептором, а в случае двойной поляризационной интерферометрии - ещё и конфигурационные изменения рецептора, вызванные связыванием с ним агониста. В последнее время был разработан также метод микротермофореза. Этот метод позволяет определять аффинность связывания, не накладывая никаких ограничений на молекулярную массу лиганда.
Для анализа полученных данных о кинетике связывания лиганда с рецептором и об его аффинности используются методы статистической механики, в частности вычисление т. н. «конфигурационного интеграла». .
Сродство к рецепторам (аффинность) и молярная активность («потентность») лиганда
Степень сродства лиганда к рецепторам, или так называемая «аффинность» лиганда к рецепторам само по себе ещё не определяет молярную активность (общую «потентность») того или иного лиганда. Молярная активность (потентность) вещества является результатом сложного взаимодействия между его степенью сродства к рецепторам и его внутренней агонистической активностью (иначе говоря, его рецепторной эффективностью). Внутренняя агонистическая активность (рецепторная эффективность) - это количественная характеристика способности данного лиганда вызывать тот или иной биологический ответ после связывания с рецептором, и мера величины вызываемого им биологического ответа, в процентах от максимально возможного биологического ответа, за который принимается максимальная стимуляция эндогенным агонистом (100 %). В зависимости от природы, характера, знака и величины по модулю вызываемого лигандом биологического ответа, он классифицируется либо как агонист или даже суперагонист , либо как частичный агонист , либо как нейтральный антагонист , либо как обратный агонист .
Селективные и неселективные лиганды
Селективные лиганды имеют тенденцию в клинически/физиологически релевантных (как правило, наномолярных) концентрациях клинически/физиологически значимо связываться только с достаточно ограниченным набором подтипов рецепторов (не обязательно все эти подтипы будут рецепторами к одному и тому же эндогенному лиганду). В то же время неселективные лиганды имеют тенденцию в релевантных концентрациях значимо связываться с достаточно широким набором подтипов рецепторов (часто - к разным эндогенным лигандам) и, тем самым, производить более широкий спектр клинических, биохимических и физиологических эффектов, как желательных, так и, нередко, нежелательных побочных эффектов.
Селективность лиганда является понятием достаточно условным и относительным, поскольку существует очень мало истинно селективных лигандов, которые связываются только с одним подтипом рецепторов во всём диапазоне «разумных», клинически достижимых у человека концентраций, и ещё меньше лигандов, способных сохранять 100 % селективность в тех концентрациях, которые можно создать в экспериментах на животных и тем более «в пробирке» (in vitro ). Часто кажущаяся относительная селективность того или иного лиганда теряется при повышении дозы или концентрации (то есть в более высоких концентрациях или дозах он начинает взаимодействовать и с другими подтипами рецепторов), и это имеет важное клиническое значение (так, высокие дозы селективного агониста опиоидных рецепторов бупренорфина способны значимо угнетать дыхание и вызывать эйфорию, так как селективность по сравнению с морфином утрачивается; аналогичным образом высокие дозы селективных β-адреноблокаторов способны вызывать бронхоспазм , так как утрачивается селективность к подтипу β 1 , а высокие дозы β 2 -адреностимуляторов помимо устранения бронхоспазма способны также вызывать тахикардию ; высокие дозы атипичных антипсихотиков наподобие рисперидона и оланзапина способны вызывать экстрапирамидные побочные явления, подобно типичным антипсихотикам).
Разработка новых, более селективных, лигандов является важной задачей современной экспериментальной и клинической фармакологии, поскольку селективные лиганды, избирательно активируя или блокируя только один «нужный» подтип рецепторов или несколько их подтипов, имеют тенденцию проявлять меньше побочных эффектов, в то время как неселективные лиганды, связываясь с широким кругом рецепторов, производят как желательные, так и нежелательные побочные эффекты. Хорошим примером является сравнение относительно неселективного хлорпромазина с более селективным галоперидолом : хлорпромазин, за счёт своей низкой селективности, производит множество побочных эффектов в дополнение к полезному антипсихотическому эффекту (так, α 1 -адреноблокада приводит к гипотензии и тахикардии, H 1 -гистаминовая блокада к сонливости , седации , повышению аппетита и прибавке массы тела, М-холиноблокада - к сухости рта и запорам и т. п., в то время как галоперидол эти явления вызывает в значительно меньшей мере и в клинически применяемых дозах вызывает в основном экстрапирамидные побочные явления, непосредственно связанные с его основным D 2 -блокирующим действием).
Мерой относительной селективности того или иного лиганда является величина соотношения его сродства (аффинности) к «желаемому», «основному» подтипу рецепторов (например, к D 2 , в случае антипсихотиков), и к ближайшему следующему по порядку величины показателя сродства (аффинности) подтипу рецепторов - то есть значение соотношения K i(1) / K i(2) . Более высокоаффинные к «желаемому» типу рецепторов, более высокоактивные («более высокопотентные») соединения часто, хотя и не всегда, являются также и более селективными, по крайней мере в малых концентрациях (применение которых, опять-таки, становится возможным именно благодаря более высокой аффинности соединения по отношению к рецептору и большей активности соединения). Таким образом, важной задачей экспериментальной и клинической фармакологии является разработка новых, более высокоаффинных (обладающих более высоким сродством к рецептору) и более активных («более высокопотентных») по отношению к тем или иным типам рецепторов, соединений.
Бивалентные лиганды
Бивалентные лиганды состоят из двух соединённых молекул, каждая из которых является лигандом для определённого подтипа рецепторов (одного и того же или разных), причём в силу особенностей пространственного строения обе части молекулы способны одновременно связываться с двумя частями «составного» гомо- или гетеродимерного рецепторного комплекса. Бивалентные лиганды используются в научных исследованиях с целью обнаружения и исследования рецепторных гомо- и гетеродимерных комплексов и изучения их свойств. Бивалентные лиганды обычно являются крупными молекулами и имеют тенденцию не обладать нужными для лекарств свойствами, такими, как удобная фармакокинетика (приемлемая биодоступность, удобство клинического применения, приемлемый период полувыведения и т. д.), низкая аллергенность и приемлемая токсичность и уровень побочных эффектов, что делает их, как правило, непригодными или малопригодными для использования в клинической практике, за пределами исследовательских лабораторий.
Привилегированная структура
Привилегированная структура - это структурная часть молекулы, радикал или химический элемент, который или которая статистически часто повторяется среди уже известных лекарств данного фармакологического класса, среди уже известных лигандов данного типа или подтипа рецепторов или известных ингибиторов данного фермента, или среди некоего другого выделенного по неким общим признакам специфического подмножества уже известных биологически активных соединений. Эти статистически выделенные привилегированные элементы химической структуры могут в дальнейшем быть использованы в качестве основы для разработки новых биологически активных соединений или новых лекарств со сходными или, возможно, даже улучшенными по сравнению с исходными соединениями свойствами, и даже для разработки целых библиотек таких соединений.
Характерными примерами являются, например, трициклические структуры разного химического строения в составе молекул трициклических антидепрессантов , или существование химически сходных целых подклассов антипсихотиков , таких, как производные бутирофенона (галоперидол , спиперон , дроперидол и др.), производные индола (резерпин , карбидин и др.), производные фенотиазина (хлорпромазин , перфеназин и др.).
См. также
Примечания
- Teif V.B. (2005). “Ligand-induced DNA condensation: choosing the model” . Biophysical Journal . 89 (4): 2574-2587. DOI :10.1529/biophysj.105.063909 . PMC . PMID .
- Teif VB, Rippe K. (2010). “Statistical-mechanical lattice models for protein-DNA binding in chromatin”. Journal of Physics: Condensed Matter . 22 (41): 414105.
Ppt%5C34928-slozhnye_belki_ch1_1.jpg" alt=">Активный центр белка и его взаимодействие с лигандом. В процессе формирования третичной структуры"> Активный центр белка и его взаимодействие с лигандом. В процессе формирования третичной структуры на поверхности функционально активного белка, обычно в углублении, образуется участок, сформированный радикалами аминокислот, далеко стоящими друг от друга в первичной структуре. Этот участок, имеющий уникальное строение для данного белка и способный специфично взаимодействовать с определенной молекулой или группой похожих молекул, называется центром связывания белка с лигандом или активным центром. Лигандами называются молекулы, взаимодействующие с белками.
Ppt%5C34928-slozhnye_belki_ch1_2.jpg" alt=">Лигандом может быть как низкомолекулярное, так и высокомолекулярное (макромолекула) вещество, в том числе и"> Лигандом может быть как низкомолекулярное, так и высокомолекулярное (макромолекула) вещество, в том числе и другой белок. Лигандами являются субстраты ферментов, кофакторы, ингибиторы и активаторы ферментов, протомеры в олигомерном белке и т.д.
Ppt%5C34928-slozhnye_belki_ch1_3.jpg" alt=">Высокая специфичность взаимодействия белка с лигандом обеспечивается комплементарностью структуры активного центра структуре лиганда.">
Ppt%5C34928-slozhnye_belki_ch1_4.jpg" alt=">Комплементарность - это пространственное и химическое соответствие взаимодействующих поверхностей. Активный центр должен не только"> Комплементарность - это пространственное и химическое соответствие взаимодействующих поверхностей. Активный центр должен не только пространственно соответствовать входящему в него лиганду, но и между функциональными группами радикалов, входящих в активный центр, и лигандом должны образоваться связи чаще всего нековалентные (ионные, водородные, а также гидрофобные взаимодействия), которые удерживают лиганд в активном центре.
Ppt%5C34928-slozhnye_belki_ch1_5.jpg" alt=">Комплементарное взаимодействие белка с лигандом">
Ppt%5C34928-slozhnye_belki_ch1_6.jpg" alt=">">
Ppt%5C34928-slozhnye_belki_ch1_7.jpg" alt=">">
Ppt%5C34928-slozhnye_belki_ch1_8.jpg" alt=">КЛАССИФИКАЦИЯ БЕЛКОВ 1. Простые белки состоят только из аминокислот. 2. Сложные белки (холопротеины)"> КЛАССИФИКАЦИЯ БЕЛКОВ 1. Простые белки состоят только из аминокислот. 2. Сложные белки (холопротеины) содержат белковую часть (апопротеин) и небелковую (простетическую) группу.
Ppt%5C34928-slozhnye_belki_ch1_9.jpg" alt=">В качестве простетической группы могут выступать различные органические (липиды, углеводы) и неорганические (металлы) вещества."> В качестве простетической группы могут выступать различные органические (липиды, углеводы) и неорганические (металлы) вещества. Связь между простетической группой и апопротеином может быть как ковалентная, так и нековалентная. Простетическую группу порой можно рассматривать в качестве лиганда. Наличие небелковой части обеспечивает выполнение белком его функции. При утрате простетической группы холопротеин теряет свою активность.
Ppt%5C34928-slozhnye_belki_ch1_10.jpg" alt=">Сложные белки - хромопротеины - нуклеопротеины - липопротеины - фосфопротеины - гликопротеины - металлопротеины">
Ppt%5C34928-slozhnye_belki_ch1_11.jpg" alt=">Металлопротеинам можно отнести холоферменты, содержащие негемовые координационно связанные ионы металлов. Среди металлопротеинов есть белки,"> Металлопротеинам можно отнести холоферменты, содержащие негемовые координационно связанные ионы металлов. Среди металлопротеинов есть белки, выполняющие депонирующие и транспортные функции (например, железосодержащие ферритин и трансферрин) и ферменты (например, цинксодержащая карбоангидраза и различные супероксиддисмутазы, содержащие в качестве активных центров ионы меди, марганца, железа и других металлов). Но и хромопротеины, содержащие ионы металлов, также можно отнести к металлопротеинам.
Ppt%5C34928-slozhnye_belki_ch1_12.jpg" alt=">Металлопротеины часто являются ферментами. Ионы металлов в этом случае: - участвуют в ориентации субстрата"> Металлопротеины часто являются ферментами. Ионы металлов в этом случае: - участвуют в ориентации субстрата в активном центре фермента, входят в состав активного центра фермента и участвуют в катализе, являясь, например, акцепторами электронов на определенной стадии ферментативной реакции. Часто ион металла в составе фермента называют кофактором.
Ppt%5C34928-slozhnye_belki_ch1_13.jpg" alt=">К ферментативным металлопротеинам относятся белки, содержащие например: - медь – цитохромоксидаза, в комплексе"> К ферментативным металлопротеинам относятся белки, содержащие например: - медь – цитохромоксидаза, в комплексе с другими ферментами дыхательной цепи митохондрий участвует в синтезе АТФ, - железо – ферритин, депонирующий железо в клетке, трансферрин, переносящий железо в крови, каталаза, обезвреживающая перекись водорода, - цинк – алкогольдегидрогеназа, обеспечивающая метаболизм этанола и других спиртов, лактатдегидрогеназа, участвующая в метаболизме молочной кислоты, - карбоангидраза, образующая угольную кислоту из CO2 и H2O, - щелочная фосфатаза, гидролизующая фосфорные эфиры различных соединений, - α2-макроглобулин, антипротеазный белок крови. - селен – тиреопероксидаза, участвующая в синтезе гормонов щитовидной железы, антиоксидантный фермент глутатионпероксидаза, - кальций – α-амилаза слюны и панкреатического сока, гидролизующая крахмал.
Ppt%5C34928-slozhnye_belki_ch1_14.jpg" alt=">Ферритин">
Ppt%5C34928-slozhnye_belki_ch1_15.jpg" alt=">Фосфопротеины – это белки, в которых присутствует фосфатная группа. Она связывается с пептидной цепью"> Фосфопротеины – это белки, в которых присутствует фосфатная группа. Она связывается с пептидной цепью через остатки тирозина, серина и треонина, т.е. тех аминокислот, которые содержат ОН-группу. Способ присоединения фосфата к белку на примере серина и тирозина
Ppt%5C34928-slozhnye_belki_ch1_16.jpg" alt=">Фосфорная кислота может выполнять: - Структурную роль, придавая заряд, растворимость и изменяя свойства"> Фосфорная кислота может выполнять: - Структурную роль, придавая заряд, растворимость и изменяя свойства белка, например, в казеине молока, яичном альбумине. Наличие остатков фосфорной кислоты способствует связыванию кальция, что необходимо для формирования, например, костной ткани. - Функциональную роль. В клетке присутствует много белков, которые связаны с фосфатом не постоянно, а в зависимости от активности метаболизма. Белок может многократно переходить в фосфорилированную или в дефосфорилированную форму, что играет регулирующую роль в его работе.
Ppt%5C34928-slozhnye_belki_ch1_17.jpg" alt=">Фосфорилирование - процесс переноса остатка фосфорной кислоты от фосфорилирующего агента-донора к субстрату, как правило,"> Фосфорилирование - процесс переноса остатка фосфорной кислоты от фосфорилирующего агента-донора к субстрату, как правило, катализируемый ферментами (киназами) и ведущий к образованию эфиров фосфорной кислоты. Дефосфорилирование (утрату остатка фосфорной кислоты) катализируют фосфатазы. АТФ + R-OH → АДФ + R-OPO3H2 R-OPO3H2 + Н2О → R-OH + Н3РО4
Ppt%5C34928-slozhnye_belki_ch1_18.jpg" alt=">Примеры: 1) ферменты гликогенсинтаза и гликогенфосфорилаза 2) гистоны в фосфорилированном состоянии менее прочно связываются"> Примеры: 1) ферменты гликогенсинтаза и гликогенфосфорилаза 2) гистоны в фосфорилированном состоянии менее прочно связываются с ДНК и активность генома возрастает. Изменение конформации белка в фосфорилированном и дефосфорилированном состоянии
Ppt%5C34928-slozhnye_belki_ch1_19.jpg" alt=">Липопротеины содержат в качестве простетической части нековалентно связанные липиды. Липиды, в частности"> Липопротеины содержат в качестве простетической части нековалентно связанные липиды. Липиды, в частности жиры, холестерол и его эфиры не растворяются в водных фазах организма, поэтому транспорт их кровью и лимфой осуществляется в виде комплексов с белками и фосфолипидами, которые называются липопротеинами.
Ppt%5C34928-slozhnye_belki_ch1_20.jpg" alt=">Все липопротеины имеют сходное строение: ядро состоит из гидрофобных молекул: триацилглицеролов, эфиров холестерола, а"> Все липопротеины имеют сходное строение: ядро состоит из гидрофобных молекул: триацилглицеролов, эфиров холестерола, а на поверхности находится монослой фосфолипидов, полярные группы которых обращены к воде, а гидрофобные погружены в гидрофобное ядро липопротеина. Кроме фосфолипидов, на поверхности находятся белки – аполипопротеины (апобелками). Их выделяют несколько видов: А, В, С, D. В каждом типе липопротеинов преобладают соответствующие ему апобелки. Аполипопротеины выполняют различные функции. Интегральные аполипопротеины являются структурными компонентами. Периферические аполипопротеины в плазме крови могут передаваться от одного типа липопротеинов к другим, определяя их дальнейшие превращения.
Ppt%5C34928-slozhnye_belki_ch1_21.jpg" alt=">Схема строения липопротеина Строение липопротеина">
Ppt%5C34928-slozhnye_belki_ch1_22.jpg" alt=">Строение липопротеинов плазмы крови">
Ppt%5C34928-slozhnye_belki_ch1_23.jpg" alt=">Выделяют четыре основных класса липопротеинов: -липопротеины высокой плотности (ЛПВП), -липопротеины низкой плотности (ЛПНП),"> Выделяют четыре основных класса липопротеинов: -липопротеины высокой плотности (ЛПВП), -липопротеины низкой плотности (ЛПНП), -липопротеины очень низкой плотности (ЛПОНП), -хиломикроны (ХМ). Каждый из типов ЛП образуется в разных тканях и транспортирует определённые липиды. Концентрация и соотношение в крови тех или иных липопротеинов играют ведущую роль в возникновении такой распространенной сосудистой патологии как атеросклероз. ЛПВП являются антиатерогенными, ЛПНП и ЛПОНП – атерогенными.
Ppt%5C34928-slozhnye_belki_ch1_24.jpg" alt=">">
Ppt%5C34928-slozhnye_belki_ch1_25.jpg" alt=">Гликопротеины или, гликоконъюгаты – это белки, содержащие углеводный компонент, ковалентно присоединенный к полипептидной основе."> Гликопротеины или, гликоконъюгаты – это белки, содержащие углеводный компонент, ковалентно присоединенный к полипептидной основе. Содержание углеводов в них варьирует от 1% до 98% по массе. Два подкласса белков, содержащих углеводы: ■ протеогликаны ■ гликопротеины
Description="">
Ppt%5C34928-slozhnye_belki_ch1_27.jpg" alt=">Для гликопротеинов характерно невысокое содержание углеводов, которые присоединены: - N-гликозидной связью к NН2-группе какого-нибудь"> Для гликопротеинов характерно невысокое содержание углеводов, которые присоединены: - N-гликозидной связью к NН2-группе какого-нибудь аминокислотного остатка, например, аспарагина; - О-гликозидной связью к гидроксильной группе остатка серина, треонина,тирозина, гидроксилизина.
Ppt%5C34928-slozhnye_belki_ch1_28.jpg" alt=">Образование О- и N-гликозидных связей в гликопротеинах. 1 - N-гликозидная связь между амидной группой"> Образование О- и N-гликозидных связей в гликопротеинах. 1 - N-гликозидная связь между амидной группой аспарагина и ОН-группой моносахарида; 2 - О-гликозидная связь между ОН-группой серина и ОН-группой моносахарида.
Ppt%5C34928-slozhnye_belki_ch1_29.jpg" alt=">Способ присоединения углевода к белку">
Ppt%5C34928-slozhnye_belki_ch1_30.jpg" alt=">Функцией гликопротеинов являются: 1. Структурная – клеточная стенка бактерий, костный матрикс, например, коллаген, эластин."> Функцией гликопротеинов являются: 1. Структурная – клеточная стенка бактерий, костный матрикс, например, коллаген, эластин. 2. Защитная – например, антитела, интерферон, факторы свертывания крови (протромбин, фибриноген). 3. Рецепторная – присоединение эффектора приводит к изменению конформации белка-рецептора, что вызывает внутриклеточный ответ. 4. Гормональная – гонадотропный, адренокортикотропный и тиреотропный гормоны. 5. Ферментативная – холинэстераза, нуклеаза. 6. Транспортная – перенос веществ в крови и через мембраны, например, трансферрин, транскортин, альбумин, Na+,К+-АТФаза.
Ppt%5C34928-slozhnye_belki_ch1_31.jpg" alt=">Схема строения белка-рецептора">
Ppt%5C34928-slozhnye_belki_ch1_32.jpg" alt=">Хромопротеины - собирательное название сложных белков с окрашенными простетическими группами различной химической природы. "> Хромопротеины - собирательное название сложных белков с окрашенными простетическими группами различной химической природы. гемопротеины (содержат гем), ретинальпротеины (содержат витамин А), флавопротеины (содержат витамин В2), кобамидпротеины (содержат витамин В12).
Ppt%5C34928-slozhnye_belki_ch1_33.jpg" alt=">Флавопротеины - это ферменты окислительно-восстановительных реакций. Содержат производные витамина В2 флавинмононуклеотид (ФМН) и флавинадениндинуклеотид"> Флавопротеины - это ферменты окислительно-восстановительных реакций. Содержат производные витамина В2 флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). Связываются данные простетические группы ковалентно и придают желтое окрашивание. Эти простетические группы являются производными изоаллоксазина.
Ppt%5C34928-slozhnye_belki_ch1_34.jpg" alt=">Изоаллоксазин - гетероциклическое соединения, производное птеридина. Молекула изоаллоксазина состоит из трех ароматических колец -"> Изоаллоксазин - гетероциклическое соединения, производное птеридина. Молекула изоаллоксазина состоит из трех ароматических колец - бензольного, пиримидинового, пиразинового.
Ppt%5C34928-slozhnye_belki_ch1_35.jpg" alt=">Гемопротеины - гем-содержащие хромопротеины. В качестве небелкового компонента включают структурно сходные железо- или магнийпорфирины."> Гемопротеины - гем-содержащие хромопротеины. В качестве небелкового компонента включают структурно сходные железо- или магнийпорфирины. Белковый компонент может быть разнообразным как по составу, так и по структуре. Основу структуры простетической группы большинства гемосодержащих белков составляет порфириновое кольцо, являющееся в свою очередь производным тетрапиррольного соединения – порфирина. Порфирин
Ppt%5C34928-slozhnye_belki_ch1_36.jpg" alt=">Порфириновое кольцо способно образовывать координационные соединения с различными ионами металлов. В результате комплексообразования формируются"> Порфириновое кольцо способно образовывать координационные соединения с различными ионами металлов. В результате комплексообразования формируются металлопорфирины: содержащие ионы железа – гемоглобины, миоглобин, цитохромы, пероксидаза, каталаза и др. (красное окрашивание), содержщие ионы магния – хлорофилл (зеленое окрашивание). Витамин В12 (кобалимин) содержит координированный ион кобальта Со2+ в порфириноподобном макроцикле – коррине, состоящем из четырех частично гидрированных пиррольных колец (розовое окрашивание).
Ppt%5C34928-slozhnye_belki_ch1_37.jpg" alt=">Хлорофилл b. Хлорофиллы участвуют в процессах фотосинтеза.">
Ppt%5C34928-slozhnye_belki_ch1_38.jpg" alt=">Цитохромы различаются аминокислотным составом пептидных цепей, числом цепей и разделяются на типы а, b,"> Цитохромы различаются аминокислотным составом пептидных цепей, числом цепей и разделяются на типы а, b, с, d. Цитохромы находятся в составе дыхательной цепи и цепи микросомального окисления. Степень окисления железа в составе цитохромов меняется в отличие от гемоглобина и миоглобина Fe2+ ↔ Fe3+
Ppt%5C34928-slozhnye_belki_ch1_39.jpg" alt=">Миоглобин (Мв) - белок, находящийся в красных мышцах, основная функция которого - создание запасов"> Миоглобин (Мв) - белок, находящийся в красных мышцах, основная функция которого - создание запасов О2, необходимых при интенсивной мышечной работе. Мв - сложный белок, содержащий белковую часть - апоМв и небелковую часть - гем. Первичная структура апоМв определяет его компактную глобулярную конформацию и структуру активного центра, к которому присоединяется небелковая часть миоглобина - гем. Кислород, поступающий из крови в мышцы, связывается с Fe2+ гема в составе миоглобина. Мв - мономерный белок, имеющий очень высокое сродство к О2, поэтому отдача кислорода миоглобином происходит только при интенсивной мышечной работе, когда парциальное давление O2 резко снижается. Формирование пространственных структур и функционирование миоглобина.
Ppt%5C34928-slozhnye_belki_ch1_40.jpg" alt=">Формирование конформации Мв. В красных мышцах на рибосомах в ходе трансляции идет синтез первичной"> Формирование конформации Мв. В красных мышцах на рибосомах в ходе трансляции идет синтез первичной структуры Мв, представленной специфической последовательностью 153 аминокислотных остатков. Вторичная структура Мв содержит восемь α-спиралей, называемых латинскими буквами от А до Н, между которыми имеются неспирализованные участки. Третичная структура Мв имеет вид компактной глобулы, в углублении которой между F и Е α-спиралями расположен активный центр.
Ppt%5C34928-slozhnye_belki_ch1_41.jpg" alt=">Структура миоглобина">
Ppt%5C34928-slozhnye_belki_ch1_42.jpg" alt=">Особенности строения и функционирования активного центра Мв. Активный центр Мв сформирован преимущественно гидрофобными радикалами"> Особенности строения и функционирования активного центра Мв. Активный центр Мв сформирован преимущественно гидрофобными радикалами аминокислот, далеко отстоящими друг от друга в первичной структуре (например, Три39 и Фен138). К активному центру присоединяется плохо растворимые в воде лиганды - гем и О2. Гем - специфический лиганд апоМв.
Ppt%5C34928-slozhnye_belki_ch1_43.jpg" alt=">Основу гема составляют четыре пиррольных кольца, соединенных метенильными мостиками; в центре расположен атом Fe2+,"> Основу гема составляют четыре пиррольных кольца, соединенных метенильными мостиками; в центре расположен атом Fe2+, соединенный с атомами азота пиррольных колец четырьмя координационными связями. В активном центре Мв кроме гидрофобных радикалов аминокислот имеются также остатки двух аминокислот с гидрофильными радикалами - Гис Е7 (Гис64) и Гис F8 (Гис93).
Ppt%5C34928-slozhnye_belki_ch1_44.jpg" alt=">Гис F8 образует координационную связь с Fe2+ и прочно фиксирует гем в активном центре."> Гис F8 образует координационную связь с Fe2+ и прочно фиксирует гем в активном центре. Гис Е7 необходим для правильной ориентации в активном центре другого лиганда - O2 при его взаимодействии с Fe+2 гема. Микроокружение гема создает условия для прочного, но обратимого связывания O2 с Fe+2 и препятствует попаданию в гидрофобный активный центр воды, что может привести к его окислению в Fе3+.
Ppt%5C34928-slozhnye_belki_ch1_45.jpg" alt=">Олигомерное строение Нв и регуляция сродства Нв к О2 лигандами. Гемоглобины человека -"> Олигомерное строение Нв и регуляция сродства Нв к О2 лигандами. Гемоглобины человека - семейство белков, так же как и миоглобин относящиеся к сложным белкам (гемопротеинам). Они имеют тетрамерное строение и содержат две α-цепи, но различаются по строению двух других полипептидных цепей (2α-, 2х-цепи). Строение второй полипептидной цепи определяет особенности функционирования этих форм Нв. Около 98% гемоглобина эритроцитов взрослого человека составляет гемоглобин А (2α-, 2β-цепи). В период внутриутробного развития функционируют два основных типа гемоглобинов: эмбриональный Нв (2α, 2ε), который обнаруживается на ранних этапах развития плода, и гемоглобин F (фетальный) - (2α, 2γ), который приходит на смену раннему гемоглобину плода на шестом месяце внутриутробного развития и только после рождения замещается на Нв А.
Ppt%5C34928-slozhnye_belki_ch1_46.jpg" alt=">Нв А - белок, родственный миоглобину (Мв), содержится в эритроцитах взрослого человека. Строение его"> Нв А - белок, родственный миоглобину (Мв), содержится в эритроцитах взрослого человека. Строение его отдельных протомеров аналогично таковому у миоглобина. Вторичная и третичная структуры миоглобина и протомеров гемоглобина очень сходны, несмотря на то что в первичной структуре их полипептидных цепей идентичны только 24 аминокислотных остатка (вторичная структура протомеров гемоглобина, так же как миоглобин, содержит восемь α-спиралей, обозначаемых латинскими буквами от А до Н, а третичная структура имеет вид компактной глобулы). Но в отличие от миоглобина гемоглобин имеет олигомерное строение, состоит из четырех полипептидных цепей, соединенных нековалентными связями.
Ppt%5C34928-slozhnye_belki_ch1_47.jpg" alt=">Олигомерная структура гемоглобина">
Ppt%5C34928-slozhnye_belki_ch1_48.jpg" alt=">Каждый протомер Нв связан с небелковой частью - гемом и соседними протомерами. Соединение белковой"> Каждый протомер Нв связан с небелковой частью - гемом и соседними протомерами. Соединение белковой части Нв с гемом аналогично таковому у миоглобина: в активном центре белка гидрофобные части гема окружены гидрофобными радикалами аминокислот за исключением Гис F8 и Гис Е7, которые расположены по обе стороны от плоскости гема и играют аналогичную роль в функционировании белка и связывании его с кислородом. Кроме того, Гис Е7 выполняет важную дополнительную роль в функционировании Нв. Свободный гем имеет в 25 000 раз более высокое сродство к СО, чем к О2. СО в небольших количествах образуется в организме и, учитывая его высокое сродство к гему, он мог бы нарушать транспорт необходимого для жизни клеток О2. Однако в составе гемоглобина сродство гема к оксиду углерода превышает сродство к О2 всего в 200 раз благодаря наличию в активном центре Гис Е7. Остаток этой аминокислоты создает оптимальные условия для связывания гема с O2 и ослабляет взаимодействие гема с СО.
Ppt%5C34928-slozhnye_belki_ch1_49.jpg" alt=">">
Ppt%5C34928-slozhnye_belki_ch1_50.jpg" alt=">Пиррольные кольца гема расположены в одной плоскости, а ион Fe2+ в неоксигенированом состоянии Hb"> Пиррольные кольца гема расположены в одной плоскости, а ион Fe2+ в неоксигенированом состоянии Hb выступает над плоскостью на 0,6 А. При присоединении кислорода ион железа погружается в плоскость колец гема. В результате сдвигается и участок полипептидной цепи, нарушаются слабые связи в молекуле Hb и изменяется конформация всей глобулы. Таким образом, присоединение кислорода вызывает изменение пространственной структуры молекулы миоглобина или протомеров гемоглобина.
Ppt%5C34928-slozhnye_belki_ch1_51.jpg" alt=">Гемоглобин может существовать как в свободной (дезоксигемоглобин), так и в оксигенированной форме, присоединяя до"> Гемоглобин может существовать как в свободной (дезоксигемоглобин), так и в оксигенированной форме, присоединяя до 4 молекул кислорода. Взаимодействие с кислородом 1-го протомера вызывает изменение его конформации, а также кооперативные конформационные изменения остальных протомеров. Сродство к кислороду возрастает, и присоединение О2 к активному центру 2-го протомера происходит легче, вызывая дальнейшую конформационную перестройку всей молекулы. В результате еще сильнее изменяется структура оставшихся протомеров и их активных центров, взаимодействие с О2 еще больше облегчается. В итоге 4-я молекула кислорода присоединяется к Hb примерно в 300 раз легче, чем 1-я. Так происходит в легких при высоком парциальном давлении кислорода.
Ppt%5C34928-slozhnye_belki_ch1_52.jpg" alt=">Кооперативные изменения конформации молекулы гемоглобина при взаимодействии с кислородом">
Ppt%5C34928-slozhnye_belki_ch1_53.jpg" alt=">В тканях, где содержание кислорода ниже, наоборот, отщепление каждой молекулы О2 облегчает освобождение последующих."> В тканях, где содержание кислорода ниже, наоборот, отщепление каждой молекулы О2 облегчает освобождение последующих. Таким образом, взаимодействие олигомерного белка гемоглобина с лигандом (О2) в одном центре связывания приводит к изменению конформации всей молекулы и других, пространственно удаленных центров, расположенных на других субъединицах (принцип «домино»). Подобные взаимосвязанные изменения структуры белка называют кооперативными конформационными изменениями. Они характерны для всех олигомерных белков и используются для регуляции их активности.
Ppt%5C34928-slozhnye_belki_ch1_54.jpg" alt=">Взаимодействие обоих белков (Mb и Hb) с кислородом зависит от его парциального давления в"> Взаимодействие обоих белков (Mb и Hb) с кислородом зависит от его парциального давления в тканях. Эта зависимость имеет разный характер, что связано с их особенностями структуры и функционирования. Гемоглобин имеет S-образную кривую насыщения, которая показывает, что субъединицы белка работают кооперативно, и чем больше кислорода они отдают, тем легче идет освобождение остальных молекул О2. Этот процесс зависит от изменения парциального давления кислорода в тканях. График насыщения миоглобина кислородом имеет характер простой гиперболы, т.е. насыщение Mb кислородом происходит быстро и отражает его функцию - обратимое связывание с кислородом, высвобождаемым гемоглобином, и освобождение в случае интенсивной физической нагрузки.
Ppt%5C34928-slozhnye_belki_ch1_55.jpg" alt=">Кривые насыщения миоглобина и гемоглобина кислородом">
Ppt%5C34928-slozhnye_belki_ch1_56.jpg" alt=">CO2 и Н+, образующиеся при катаболизме органических веществ, уменьшают сродство гемоглобина к О2 пропорционально"> CO2 и Н+, образующиеся при катаболизме органических веществ, уменьшают сродство гемоглобина к О2 пропорционально их концентрации. Энергия, необходимая для работы клеток, вырабатывается преимущественно в митохондриях при окислении органических веществ с использованием O2, доставляемого из легких гемоглобином. В результате окисления органических веществ образуются конечные продукты их распада: СО2 и Н2O, количество которых пропорционально интенсивности протекающих процессов окисления. СO2 диффузией попадает из клеток в кровь и проникает в эритроциты, где под действием фермента карбоангидразы превращается в угольную кислоту. Эта слабая кислота диссоциирует на протон и бикарбонат ион. СО2 + Н2О → Н2СО3 → Н+ + НСО3-
Ppt%5C34928-slozhnye_belki_ch1_57.jpg" alt=">Ионы Н+ способны присоединятся к радикалам Гис146 в β-цепях гемоглобина, т.е. в участках, удаленных"> Ионы Н+ способны присоединятся к радикалам Гис146 в β-цепях гемоглобина, т.е. в участках, удаленных от гема. Протонирование гемоглобина снижает его сродство к О2, способствует отщеплению О2 от оксиНв, образованию дезоксиНв и увеличивает поступление кислорода в ткани пропорционально количеству образовавшихся протонов. Увеличение количества освобожденного кислорода в зависимости от увеличения концентрации Н+ в эритроцитах называется эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект). В легких высокое парциальное давление кислорода способствует его связыванию с дезоксиНв, что уменьшает сродство белка к Н+. Освободившиеся протоны под действием карбоангидразы взаимодействуют с бикарбонатами с образованием СО2 и Н2О
Ppt%5C34928-slozhnye_belki_ch1_58.jpg" alt=">Зависимость сродства Нв к О2 от концентрации СО2 и протонов (эффект Бора): А -"> Зависимость сродства Нв к О2 от концентрации СО2 и протонов (эффект Бора): А - влияние концентрации СО2 и Н+ на высвобождение О2 из комплекса с Нв (эффект Бора); Б - оксигенирование дезоксигемоглобина в легких, образование и выделение СО2.
Ppt%5C34928-slozhnye_belki_ch1_59.jpg" alt=">Образовавшийся СО2 поступает в альвеолярное пространство и удаляется с выдыхаемым воздухом. Таким образом, количество"> Образовавшийся СО2 поступает в альвеолярное пространство и удаляется с выдыхаемым воздухом. Таким образом, количество высвобождаемого гемоглобином кислорода в тканях регулируется продуктами катаболизма органических веществ: чем интенсивнее распад веществ, например при физических нагрузках, тем выше концентрация СО2 и Н+ и тем больше кислорода получают ткани в результате уменьшения сродства Нв к О2.
Ppt%5C34928-slozhnye_belki_ch1_60.jpg" alt=">Изменение функциональной активности белка при взаимодействии с другими лигандами вследствие конформационных изменений называется аллостерической"> Изменение функциональной активности белка при взаимодействии с другими лигандами вследствие конформационных изменений называется аллостерической регуляцией, а соединения-регуляторы - аллостерическими лигандами или эффекторами. Способность к аллостерической регуляции характерна, как правило, для олигомерных белков, т.е. для проявления аллостерического эффекта необходимо взаимодействие протомеров. При воздействии аллостерических лигандов белки меняют свою конформацию (в том числе и активного центра) и функцию.
Ppt%5C34928-slozhnye_belki_ch1_61.jpg" alt=">Аллостерическая регуляция сродства Нв к О2 лигандом - 2,3-бис-фосфоглицератом. В эритроцитах из продукта"> Аллостерическая регуляция сродства Нв к О2 лигандом - 2,3-бис-фосфоглицератом. В эритроцитах из продукта окисления глюкозы - 1,3-бисфосфоглицерата синтезируется аллостерический лиганд гемоглобина - 2,3-бисфосфоглицерат (2,3-БФГ). В нормальных условиях концентрация 2,3-БФГ высокая и сравнима с концентрацией Нв. 2,3-БФГ имеет сильный отрицательный заряд (-5).
Ppt%5C34928-slozhnye_belki_ch1_62.jpg" alt=">В центре тетрамерной молекулы гемоглобина находится полость. Ее образуют аминокислотные остатки всех четырех протомеров."> В центре тетрамерной молекулы гемоглобина находится полость. Ее образуют аминокислотные остатки всех четырех протомеров. В капиллярах тканей протонирование Нв (эффект Бора) приводит к разрыву связи между железом гема и О2. В молекуле дезоксигемоглобина по сравнению с оксигемоглобином возникают дополнительные ионные связи, соединяющие протомеры, вследствие чего размеры центральной полости по сравнению с оксигемоглобином увеличиваются. Центральная полость является местом присоединения 2,3-БФГ к гемоглобину. БФГ поступает в полость дезоксигемоглобина. 2,3-БФГ взаимодействует с гемоглобином в участке, удаленном от активных центров белка и относится к аллостерическим (регуляторным) лигандам, а центральная полость Нв является аллостерическим центром. 2,3-БФГ имеет сильный отрицательный заряд и взаимодействует с положительно заряженными группами двух β-цепей Нв. При этом его сродство к О2 снижается в 26 раз. В результате происходит высвобождение кислорода в капиллярах ткани при низком парциальном давлении О2. В легких высокое парциальное давление О2, наоборот, приводит к оксигенированию Нв и освобождению БФГ.
Ppt%5C34928-slozhnye_belki_ch1_63.jpg" alt=">Центр связывания БФГ находится в положительно заряженной полости между 4 протомерами гемоглобина. Взаимодействие БФГ"> Центр связывания БФГ находится в положительно заряженной полости между 4 протомерами гемоглобина. Взаимодействие БФГ с центром связывания изменяет конформацию α- и β-протомеров НЬ и их активных центров. Сродство НЬ к молекулам О2 снижается и кислород высвобождается в ткани. В легких при высоком парциальном давлении О2 активные центры гемоглобина насыщаются за счет изменения конформации и БФГ вытесняется из аллостерического центра
Ppt%5C34928-slozhnye_belki_ch1_64.jpg" alt=">">
Ppt%5C34928-slozhnye_belki_ch1_65.jpg" alt=">Таким образом, олигомерные белки обладают новыми по сравнению с мономерными белками свойствами. Присоединение лигандов"> Таким образом, олигомерные белки обладают новыми по сравнению с мономерными белками свойствами. Присоединение лигандов на участках, пространственно удаленных друг от друга (аллостерических), способно вызывать конформационные изменения во всей белковой молекуле. Благодаря взаимодействию с регуляторными лигандами происходит изменение конформации и адаптация функции белковой молекулы к изменениям окружающей среды.
Ppt%5C34928-slozhnye_belki_ch1_66.jpg" alt=">Около 15% углекислого газа, присутствующего в крови, переносится молекулами гемоглобина. В тканях часть молекул"> Около 15% углекислого газа, присутствующего в крови, переносится молекулами гемоглобина. В тканях часть молекул углекислого газа может присоединится к каждому протомеру молекулы гемоглобина, при этом снижается сродство Hb к кислороду. В легких, наоборот, из-за высокого парциального давления кислорода, О2 связывается с Hb, а СО2 высвобождается.
Ppt%5C34928-slozhnye_belki_ch1_67.jpg" alt=">">
Ppt%5C34928-slozhnye_belki_ch1_68.jpg" alt=">В молекуле гемоглобина S (так назван аномальный гемоглобин) мутантными оказались 2 β-цепи, в которых"> В молекуле гемоглобина S (так назван аномальный гемоглобин) мутантными оказались 2 β-цепи, в которых глутамат, высокополярная отрицательно заряженная аминокислота в положении 6 была заменена валином, содержащим гидрофобный радикал.
), а также в химии комплексных соединений , обозначая там присоединенные к одному или нескольким центральным (комплексообразующим) атомам металла частицы.
В неорганической химии
Чаще всего такое связывание происходит с образованием так называемой «координационной» донорно-акцепторной связи , где лиганды выступают в роли основания Льюиса , то есть являются донорами электронной пары . При присоединении лигандов к центральному атому химические свойства комплексообразователя и самих лигандов часто претерпевают значительные изменения.
Номенклатура лигандов
- первым в названии соединения в именительном падеже называется анион, а затем в родительном - катион
- в названии комплексного иона сначала перечисляются лиганды в алфавитном порядке, а затем центральный атом
- центральный атом в нейтральных катионных комплексах называются русским названием, а в анионах корнем латинского названия с суффиксом «ат». После названия центрального атома указывается степень окисления.
- число лигандов, присоединенных к центральному атому, указывается приставками «моно», «ди», «три», «тетра», «пента», и т. д.
Характеристики лигандов
Электронное строение
Собственно, важнейшая характеристика лиганда, позволяющая оценить и спрогнозировать его способности к комплексообразованию и саморазрушению D-орбитали - разрушения соединения в целом. В первом приближении включает в себя количество электронных пар, которые лиганд способен выделить на создание координационных связей и электроотрицательность донирующего атома или функциональной группы .
Дентатность
Число занимаемых лигандом координационных мест центрального атома (или атомов), называется дентатностью (от лат. dens, dent- - зуб ). Лиганды, занимающие одно координационное место, называются моно дентатными (например, N H 3), два - би дентатными (оксалат-анион [O -C(=O)-C(=O)-O ] 2−). Лиганды, способные занять большее количество мест, обычно обозначают как поли дентатные. Например, этилендиаминтетрауксусная кислота (EDTA), способная занять шесть координационных мест.
Кроме дентатности, существует характеристика, отражающая количество атомов лиганда, связанных с одним координационным местом центрального атома. В английской литературе обозначается словом hapticity и имеет номенклатурное обозначение с соответствующим надстрочным индексом. Хотя устоявшегося термина в русском языке она, по-видимому, не имеет, в некоторых источниках можно встретить кальку «гаптность» . Как пример, можно привести циклопентадиенильный лиганд в металлоцентровых комплексах, занимающий одно координационное место (то есть, являющийся монодентатным) и связанный через все пять атомов углерода: η 5 - − .
Способы координации
 Лиганды с дентатностью больше двух способны образовывать хелатные комплексы
(греч. χηλή
- клешня) - комплексы, где центральный атом включен в один или более циклов с молекулой лиганда. Такие лиганды называются хелатирующими
. Как пример можно привести комплексы тетрааниона той же EDTA, обратив внимание, что несколько из четырёх связей M-O в нём могут формально являться ионными
.
Лиганды с дентатностью больше двух способны образовывать хелатные комплексы
(греч. χηλή
- клешня) - комплексы, где центральный атом включен в один или более циклов с молекулой лиганда. Такие лиганды называются хелатирующими
. Как пример можно привести комплексы тетрааниона той же EDTA, обратив внимание, что несколько из четырёх связей M-O в нём могут формально являться ионными
.
При образовани хелатных комплексов часто наблюдается хелатный эффект - большая их стабильность по сравнению с аналогичными комплексами не-хелатирующих лигандов. Он достигается за счет большего экранирования центрального атома от замещающих воздействий и энтропийного эффекта. Например, константа диссоциации аммиачного комплекса кадмия 2+ почти в 1500 раз меньше, чем комплекса с этилендиамином 2+ . Причина этого заключается в том, что при взаимодействии гидратированного иона кадмия(II) с этилендиамином две молекулы лиганда вытесняют четыре молекулы воды. При этом число свободных частиц в системе значительно возрастает, и энтропия системы возрастает (а внутренняя упорядоченность комплекса соответственно растёт). То есть причина хелатного эффекта - увеличение энтропии системы при замещении монодентатных лигандов полидентатнымии и, как следствие, снижение энергии Гиббса .
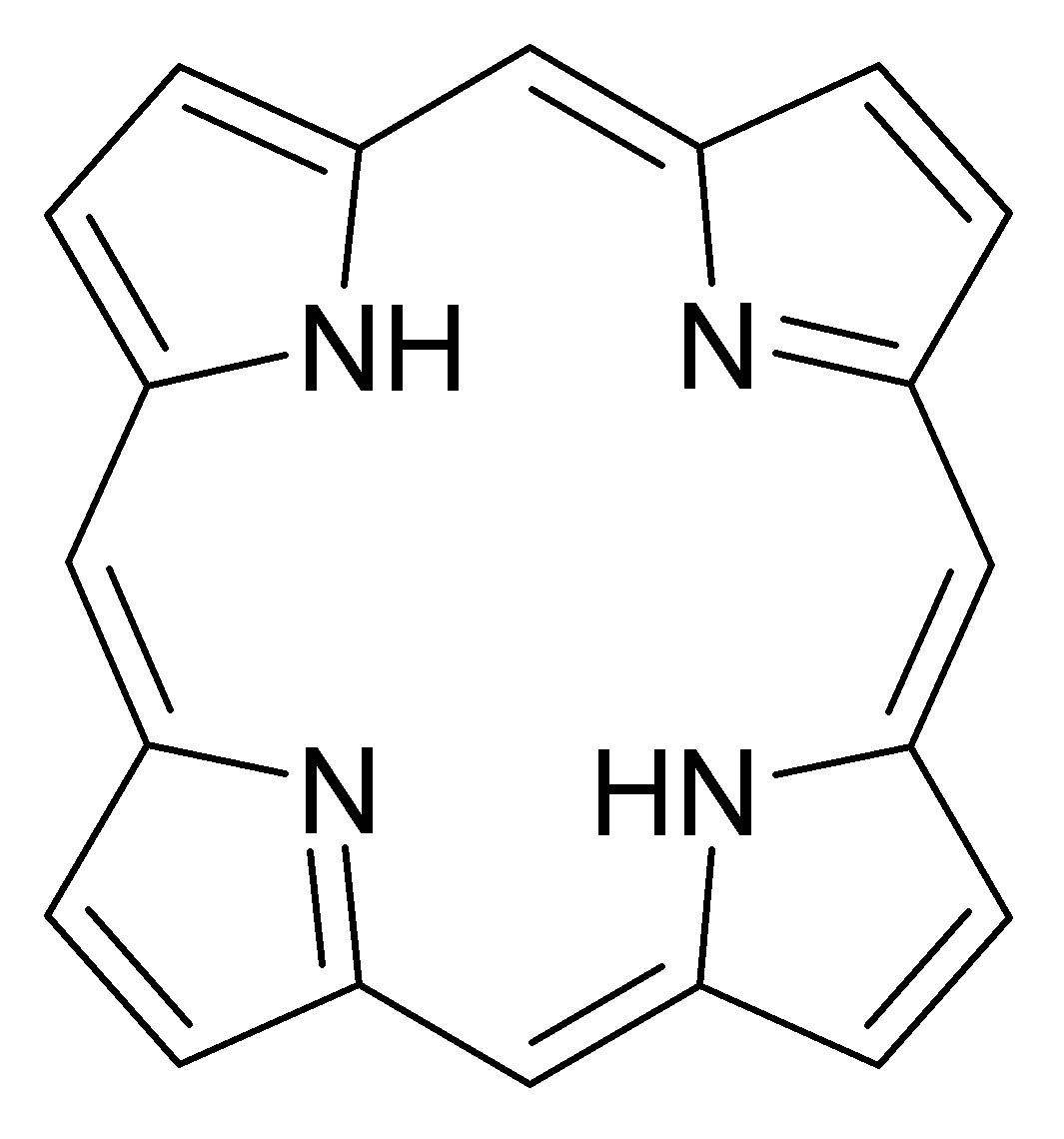 Среди хелатирующих лигандов можно выделить класс макроциклических лигандов - молекул с достаточным для помещения атома комплексообразователя размером внутрициклического пространства. Примером таких соединений могут служить порфириновые основания - основы важнейших биохимических комплексов, таких, как гемоглобин , хлорофилл и бактериохлорофилл . Также в качестве макроциклических лигандов могут выступать краун-эфиры , каликсарены и др.
Среди хелатирующих лигандов можно выделить класс макроциклических лигандов - молекул с достаточным для помещения атома комплексообразователя размером внутрициклического пространства. Примером таких соединений могут служить порфириновые основания - основы важнейших биохимических комплексов, таких, как гемоглобин , хлорофилл и бактериохлорофилл . Также в качестве макроциклических лигандов могут выступать краун-эфиры , каликсарены и др.
Лиганды также могут являться мостиковыми, образуя связи между различными центральными атомами в би- или полиядерных комплексах. Мостиковые лиганды обозначаются греческой буквой μ (мю ).
Напишите отзыв о статье "Лиганд"
Примечания
|
||||||||||||||||||
Отрывок, характеризующий Лиганд
– Ежели бы все воевали только по своим убеждениям, войны бы не было, – сказал он.– Это то и было бы прекрасно, – сказал Пьер.
Князь Андрей усмехнулся.
– Очень может быть, что это было бы прекрасно, но этого никогда не будет…
– Ну, для чего вы идете на войну? – спросил Пьер.
– Для чего? я не знаю. Так надо. Кроме того я иду… – Oн остановился. – Я иду потому, что эта жизнь, которую я веду здесь, эта жизнь – не по мне!
В соседней комнате зашумело женское платье. Как будто очнувшись, князь Андрей встряхнулся, и лицо его приняло то же выражение, какое оно имело в гостиной Анны Павловны. Пьер спустил ноги с дивана. Вошла княгиня. Она была уже в другом, домашнем, но столь же элегантном и свежем платье. Князь Андрей встал, учтиво подвигая ей кресло.
– Отчего, я часто думаю, – заговорила она, как всегда, по французски, поспешно и хлопотливо усаживаясь в кресло, – отчего Анет не вышла замуж? Как вы все глупы, messurs, что на ней не женились. Вы меня извините, но вы ничего не понимаете в женщинах толку. Какой вы спорщик, мсье Пьер.
– Я и с мужем вашим всё спорю; не понимаю, зачем он хочет итти на войну, – сказал Пьер, без всякого стеснения (столь обыкновенного в отношениях молодого мужчины к молодой женщине) обращаясь к княгине.
Княгиня встрепенулась. Видимо, слова Пьера затронули ее за живое.
– Ах, вот я то же говорю! – сказала она. – Я не понимаю, решительно не понимаю, отчего мужчины не могут жить без войны? Отчего мы, женщины, ничего не хотим, ничего нам не нужно? Ну, вот вы будьте судьею. Я ему всё говорю: здесь он адъютант у дяди, самое блестящее положение. Все его так знают, так ценят. На днях у Апраксиных я слышала, как одна дама спрашивает: «c"est ca le fameux prince Andre?» Ma parole d"honneur! [Это знаменитый князь Андрей? Честное слово!] – Она засмеялась. – Он так везде принят. Он очень легко может быть и флигель адъютантом. Вы знаете, государь очень милостиво говорил с ним. Мы с Анет говорили, это очень легко было бы устроить. Как вы думаете?
Пьер посмотрел на князя Андрея и, заметив, что разговор этот не нравился его другу, ничего не отвечал.
– Когда вы едете? – спросил он.
– Ah! ne me parlez pas de ce depart, ne m"en parlez pas. Je ne veux pas en entendre parler, [Ах, не говорите мне про этот отъезд! Я не хочу про него слышать,] – заговорила княгиня таким капризно игривым тоном, каким она говорила с Ипполитом в гостиной, и который так, очевидно, не шел к семейному кружку, где Пьер был как бы членом. – Сегодня, когда я подумала, что надо прервать все эти дорогие отношения… И потом, ты знаешь, Andre? – Она значительно мигнула мужу. – J"ai peur, j"ai peur! [Мне страшно, мне страшно!] – прошептала она, содрогаясь спиною.
Муж посмотрел на нее с таким видом, как будто он был удивлен, заметив, что кто то еще, кроме его и Пьера, находился в комнате; и он с холодною учтивостью вопросительно обратился к жене:
– Чего ты боишься, Лиза? Я не могу понять, – сказал он.
– Вот как все мужчины эгоисты; все, все эгоисты! Сам из за своих прихотей, Бог знает зачем, бросает меня, запирает в деревню одну.
– С отцом и сестрой, не забудь, – тихо сказал князь Андрей.
– Всё равно одна, без моих друзей… И хочет, чтобы я не боялась.
Тон ее уже был ворчливый, губка поднялась, придавая лицу не радостное, а зверское, беличье выраженье. Она замолчала, как будто находя неприличным говорить при Пьере про свою беременность, тогда как в этом и состояла сущность дела.
– Всё таки я не понял, de quoi vous avez peur, [Чего ты боишься,] – медлительно проговорил князь Андрей, не спуская глаз с жены.
Княгиня покраснела и отчаянно взмахнула руками.
– Non, Andre, je dis que vous avez tellement, tellement change… [Нет, Андрей, я говорю: ты так, так переменился…]
– Твой доктор велит тебе раньше ложиться, – сказал князь Андрей. – Ты бы шла спать.
Княгиня ничего не сказала, и вдруг короткая с усиками губка задрожала; князь Андрей, встав и пожав плечами, прошел по комнате.
Пьер удивленно и наивно смотрел через очки то на него, то на княгиню и зашевелился, как будто он тоже хотел встать, но опять раздумывал.
– Что мне за дело, что тут мсье Пьер, – вдруг сказала маленькая княгиня, и хорошенькое лицо ее вдруг распустилось в слезливую гримасу. – Я тебе давно хотела сказать, Andre: за что ты ко мне так переменился? Что я тебе сделала? Ты едешь в армию, ты меня не жалеешь. За что?
– Lise! – только сказал князь Андрей; но в этом слове были и просьба, и угроза, и, главное, уверение в том, что она сама раскается в своих словах; но она торопливо продолжала:
– Ты обращаешься со мной, как с больною или с ребенком. Я всё вижу. Разве ты такой был полгода назад?
– Lise, я прошу вас перестать, – сказал князь Андрей еще выразительнее.
Пьер, всё более и более приходивший в волнение во время этого разговора, встал и подошел к княгине. Он, казалось, не мог переносить вида слез и сам готов был заплакать.
– Успокойтесь, княгиня. Вам это так кажется, потому что я вас уверяю, я сам испытал… отчего… потому что… Нет, извините, чужой тут лишний… Нет, успокойтесь… Прощайте…
Князь Андрей остановил его за руку.
– Нет, постой, Пьер. Княгиня так добра, что не захочет лишить меня удовольствия провести с тобою вечер.
– Нет, он только о себе думает, – проговорила княгиня, не удерживая сердитых слез.
– Lise, – сказал сухо князь Андрей, поднимая тон на ту степень, которая показывает, что терпение истощено.
Вдруг сердитое беличье выражение красивого личика княгини заменилось привлекательным и возбуждающим сострадание выражением страха; она исподлобья взглянула своими прекрасными глазками на мужа, и на лице ее показалось то робкое и признающееся выражение, какое бывает у собаки, быстро, но слабо помахивающей опущенным хвостом.