Fenolos hidroxilcsoportok és antioxidáns aktivitás. Alkoholok oxidációs reakciója aldehidekké Reakciók a hidroxilcsoporton
Fenolos hidroxil egy aromás csoporthoz kapcsolódó hidroxilcsoport. Fenolcsoportból származó gyógyszereket tartalmaz (fenol, rezorcin); fenolsavak és származékaik (szalicilsav, fenil-szalicilát, szalicilamid, oxafenamid); fenantrén-izokinolin-származékok (morfin-hidroklorid, apomorfin); sinestrol, adrenalin stb.
A fenolos hidroxilt tartalmazó vegyületek kémiai tulajdonságait egy elektronpár és az aromás gyűrű π-elektronjainak kölcsönhatása határozza meg. Ez a kölcsönhatás az elektronsűrűség eltolódásához vezet az OH-csoportról a gyűrűre, az elektronok egyenletes eloszlásának megzavarásához, és az ortho-csoportban túlzott negatív töltés létrejöttéhez. O)- és pár ( P)-pozíciók. A hidroxicsoport hidrogénatomja ionizálódik, és a fenoloknak gyenge savas tulajdonságokat ad (fenol pKa = 10,0; rezorcin pKa = 9,44). Ezért az alkoholoktól eltérően sókat képeznek lúgokkal (pH 12-13), oldható komplex vegyületeket vas(III)-kloriddal (semleges, enyhén lúgos és savas oldatokban).
A fenolok erős redukáló tulajdonságokkal rendelkeznek, és nagyon könnyen oxidálódnak még gyenge oxidálószerek hatására is. Kinoid szerkezetű színes vegyületeket képeznek.
A hidrogének elektrofil szubsztitúciójának reakciói O- És P- az aromás gyűrű helyzetei – halogénezés (brómozás), kondenzáció aldehidekkel, nitrálás, kombináció diazóniumsókkal.
A fenolos hidroxil és az általa aktivált aromás gyűrű tulajdonságai alapján a következő reakciókat alkalmazzuk a gyógyszeranalízisben:
1 – komplexképződés;
2 – halogénezés (brómozás);
3 – azo kombinációk;
4 – oxidáció;
5 – indofenol festék képződése;
6 – kondenzáció aldehidekkel.
Azonosítás
2.1. Komplexációs reakció vasionokkal (III)
A fenolos hidroxil tulajdonságain alapul, hogy oldható komplex vegyületeket képezzenek, gyakran kékre (fenol) vagy ibolyára (rezorcin, szalicilsav), ritkábban vörösre (PAS - nátrium) és zöldre (kinoszol, adrenalin).
A komplexek összetételét, következésképpen színüket a fenolos hidroxilok mennyisége, az egyéb funkciós csoportok hatása és a környezet reakciója határozza meg.
Ha túl sok fenol van:

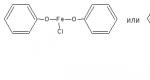
A végtermék feltételezhető összetétele a fenollal történő reakcióban:


2.2. Aromás gyűrűs brómozási reakció
A hidrogén elektrofil helyettesítésén alapul O-És P- pozíciókat a brómon oldhatatlan brómszármazék képződésével (fehér csapadék).

A brómozás alapvető szabályai:
A hidrogént a bróm helyettesíti O-És P- pozícióban van a fenolos hidroxilcsoporthoz képest (a legreaktívabb az P- pozíció):

Ha elérhető benne O- vagy P- a szubsztituensek aromás gyűrűjének helyzete, kevesebb brómatom reagál;
Ha be O- vagy P- pozíciókban karboxilcsoport van, majd brómfelesleg jelenlétében dekarboxilezés megy végbe és tribróm-származék képződik:

Ha a helyettes bent van m- pozícióban, akkor nem zavarja a tribróm-származék képződését:

Ha egy vegyület két fenolos hidroxilcsoportot tartalmaz m- pozícióban, akkor koordinált orientációjuk eredményeként tribróm-származék keletkezik:

Ha két hidroxilcsoport helyezkedik el O- vagy P- egymással szemben, következetlenül hatnak: a brómozás mennyiségileg nem megy végbe:

Ha a fenolos hidroxilcsoportokon kívül a vegyület amid- vagy észtercsoportot is tartalmaz (szalicilamid, fenil-szalicilát), akkor ezek bromatometriás kvantitatív értékeléséhez előzetes hidrolízisre van szükség.
2.3. Azo kapcsolási reakció
A kombináció is megy O-És P- rendelkezéseket, ebben az esetben, valamint a brómozásnál előnyösebb P- pozíció. A diazoreagens a diazóniumsó (diazotizált szulfanilsav). A környezet lúgos. A reakciótermék egy azofesték.

2.4. Oxidációs reakció
A fenolok különféle vegyületekké, de leggyakrabban oxidálódhatnak O- vagy P-kinonok (ciklikus diketonok), rózsaszín vagy ritkábban sárga színűek.


2.5. Indofenol festék képződésének reakciója
A fenolok kinonokká történő oxidációján alapul, amelyek ammóniával vagy amino-származékkal és fenolfelesleggel kondenzálva indofenol festéket, ibolyát képeznek.


Ennek a reakciónak egy változata a Lieberman-nitro-reakció, amely azokra a fenolokra jellemző, amelyekben nincs szubsztituens O-És P- rendelkezések.
Ha savas környezetben nátrium-nitritnek van kitéve, képződik P-nitrozofenol, izomerizálódik P- kinoidoxim, amely savas környezetben fenolfelesleggel reagálva indofenolt képez:

2.6. Nitrozovegyületek képződése
Híg salétromsavval reagálva a fenolok szobahőmérsékleten nitrálódhatnak, ami O-És P- nitro-származékok. A kapott nitro-származék tartalmaz P- a hidroxilcsoport mozgó hidrogénatomjának helyzetében kinoid szerkezetű tautomer aci forma képződik, általában sárga színű. A lúg hozzáadása javítja a színt a jól disszociált só képződése miatt:

2.7. Kondenzációs reakció aldehidekkel vagy savanhidridekkel
Formaldehiddel tömény kénsav jelenlétében vörös színű aurikus (aril-metán) festéket képezve.
A reakció a szalicilsav gyógyszerkönyvében található. A tömény kénsav a reakció első szakaszában vízeltávolító szerként, a másodikban oxidálószerként működik.
Ftálsavanhidriddel (az olvadék fúziója, majd lúgban való feloldása) a gyógyszerkönyv a fenol és a rezorcin azonosítására ajánlja.

mennyiségi meghatározása
2.8. Bromatometria
A módszer az aromás gyűrű hidrogénatomjainak brómmal való elektrofil szubsztitúcióján alapul, amelyet kálium-bromát és kálium-bromid savas környezetben történő reakciójában izolálnak.
K  BrO 3 + 5KBr + 6 HCl → 3Br 2 + 6KCl + 3H 2 O
BrO 3 + 5KBr + 6 HCl → 3Br 2 + 6KCl + 3H 2 O
Közvetlen és fordított titrálási módszereket alkalmaznak. Közvetlenül - titráljon kálium-bromáttal kálium-bromid jelenlétében metilnarancs vagy metilvörös indikátorral, rózsaszíntől elszíneződöttig. Az ekvivalencia ponton egy felesleges csepp kálium-bromát brómot szabadít fel, amely oxidálja az indikátort, és az oldat színtelenné válik. A visszatitrálás során feleslegben kálium-bromátot vezetünk be, kálium-bromidot adunk hozzá, savas környezetet hozunk létre, a brómozáshoz szükséges időt fenntartjuk, majd a brómfelesleget jodometriásan határozzuk meg (indikátorként keményítő).
Br 2 + 2KI → I 2 + 2KBr
I 2 + 2Na 2 S 2 O 3 → Na 2 S 4 O 6 + 2 NaI
Közvetlen titrálással a timolt a GF, a fenolt, a rezorcint, a szalicilsavat, a szinesztrolt és más gyógyszereket pedig fordított titrálással határozzuk meg.
NEKEM. = ¼ M.m. (timol)
NEKEM. = 1/6 M.m. (fenol, rezorcin, szalicilsav)
Nekem. = 1/8 M.m. (sinestrol)
2.9. Jódometria
Az aromás gyűrű hidrogénatomjainak jóddal történő elektrofil helyettesítésén alapul.

A hidrogén-jodid megkötésére, amely az egyensúlyt ellenkező irányba tolja el, nátrium-acetátot vagy nátrium-hidrogén-karbonátot adnak hozzá.
HI + NaHCO 3 → NaI + H 2 O + CO 2
HI + CH 3 COONa → NaI + CH 3 COOH
Közvetlen és fordított titrálási módszereket alkalmaznak. Ez utóbbiban a feleslegben lévő jódot nátrium-tioszulfáttal titráljuk.
I 2 + 2NaS 2 O 3 → 2NaI + Na 2 S 4 O 6
NEKEM. = 1/6 M.m. (fenol)
2.10. Jód klorometria
A módszer az aromás gyűrű hidrogénatomjainak jóddal történő elektrofil szubsztitúcióján alapul, amely a jód-monoklorid része.

Visszatitrálási módszert alkalmazunk - a jód-monoklorid feleslegét jodometriásan határozzuk meg.
ICl + KI → I 2 + KCl
I 2 + 2Na 2 S 2 O 6 → 2 NaI + Na 2 S 4 O 6
NEKEM. = 1/6 M.m. (fenol)
2.11. Acetilezési módszer
A GF X szerint használják a szinesztrol mennyiségi értékelésére.

NEKEM. = ½ M.m.
2.12. Alkalimetriás semlegesítési módszer a protofil oldószerben, a dimetil-formamidban (DMF).
A fenolok gyógyszercsoportjai nagyon gyenge savas tulajdonságokat mutatnak, vizes vagy vegyes közegben történő semlegesítés alkalimetriás módszerével történő meghatározása lehetetlen, ezért a titrálást nem vizes oldószeres közegben, különösen DMF-ben alkalmazzák. A módszer egy meghatározott gyenge sav (fenol) sóképzésén alapul titrálószerrel (nátrium-metilát) egy protofil oldószerben, amely javítja a savas tulajdonságokat.

Teljes:

2.13. Fotokolorimetria (FEC) és spektrofotometria (SPM)
A színes oldatok azon tulajdonságán alapul, hogy a spektrum látható tartományában elnyelik a nem monokromatikus (FEC) vagy monokromatikus (SPM) fényt.
Színes oldatok beszerzése;
Optikai sűrűség (D) mérése, amely az elektromágneses sugárzásnak az analitot tartalmazó oldat általi elnyelését jellemzi;
A fényelnyelés alaptörvényén alapuló számítások elvégzése kalibrációs grafikon, fajlagos abszorpciós együttható és standard mintaoldat segítségével.
Ha ezekkel a módszerekkel fenolos hidroxilt tartalmazó gyógyszereket határozunk meg, a vas(III)-ionokkal végzett komplexképzési reakciók, a diazóniumsókkal való azokapcsolás és az indofenol-festék képződése alapján színes vegyületeket kapunk.
14. sz. előadás
Téma: „Minőségi reakciók funkcionális csoportokra”
1) Hidroxil (alkohol, fenol)
2) Karbonil (aldehid, karboxil, észter)
3) Elsődleges aromás aminocsoport, tercier aminocsoport (tercier nitrogén)
4) Imid, szulfamid.
A funkcionális csoportok (FG) olyan egyedi atomok vagy széngyökhöz kapcsolódó atomcsoportok, amelyek jellegzetes tulajdonságaik miatt gyógyászati anyagok meghatározására használhatók.
I. Alkohol-hidroxil. Az Alr-OH egy alifás szénhidrogéncsoporthoz kapcsolódó hidroxilcsoport.
Az alkohol-hidroxil alapján a következő reakciókat alkalmazzák az azt tartalmazó gyógyszerek elemzéséhez:
észterezés (észterek képzése savakkal vagy anhidridjeikkel);
Oxidáció aldehidekké és bizonyos esetekben savakká;
Komplexálás réz(II)-ionokkal lúgos közegben.
1.Észterezési reakció vízeltávolító szerek jelenlétében savakkal vagy azok anhidridjeivel. Az alkoholok észterképző tulajdonságán alapul. A kis molekulatömegű vegyületek esetében az észtereket a nagy molekulatömegű gyógyszerek elemzésekor az olvadáspont alapján mutatják ki.
Az észterezési reakció az etil-alkohol gyógyszerkönyve.
CH 3 CH 2 OH + CH 3 COOH H2SO4→ CH 3 CH 2 OCOCH 3
2. Oxidációs reakció, az alkoholok azon tulajdonsága alapján, hogy aldehidekké oxidálódnak, amelyeket a szag alapján észlelnek. Reagensként különféle oxidálószereket használnak: kálium-permanganát, kálium-bikromát, kálium-hexaciano-ferrát (III) stb. A kálium-permanganát rendelkezik a legnagyobb analitikai értékkel, amely redukálva +7-ről + 2-re változtatja az oxidációs állapotot és elszíneződik, pl. hatásossá teszi a reakciót.

Komplexációs reakció, az alkoholok azon tulajdonsága alapján, hogy lúgos környezetben réz(II)-szulfáttal színes komplex vegyületeket képeznek.

Többértékű alkohol - glicerin és efedrin-hidroklorid azonosítására szolgál, amelyekben az alkohol-hidroxil mellett egy szekunder amincsoport is részt vesz a komplexképzésben.
Fenolos hidroxil egy aromás csoporthoz kapcsolódó hidroxilcsoport. Gyógyszercsoport fenolokat tartalmaz (fenol, rezorcin); fenolsavak és származékaik (szalicilsav, fenil-szalicilát, szalicilamid, oxafenamid); fenantrén-izokinolin-származékok (morfin-hidroklorid, apomorfin); sinestrol, adrenalin, mezaton stb.
A fenolos hidroxilt tartalmazó vegyületek kémiai tulajdonságait egy elektronpár és az aromás gyűrű π elektronjai közötti kölcsönhatás határozza meg. Ez a kölcsönhatás az elektronsűrűség eltolódásához vezet az OH - csoportról a gyűrűre, az elektronok egyenletes eloszlásának megzavarásához, valamint az orto és para pozíciókban túlzott negatív töltés kialakulásához. A hidroxicsoport hidrogénatomja ionizálódik, és gyenge savas tulajdonságokat ad a fenoloknak, amelyeket azonban ritkán használnak az elemzésben. Az aromás gyűrű o- és n-helyzetében a hidrogének elektrofil szubsztitúciójának reakciói a legnagyobb jelentőséggel bírnak.
A fenolos hidroxil tulajdonságai alapján a következő reakciókat alkalmazzák:
Bonyolultság;
Brómozás;
Azóz kombinációk;
Oxidáció;
Indofenol festék képződése;
Kondenzáció
1. Komplexációs reakciók fenolos hidroxilcsoport vas(III)-ionokkal. A fenolos hidroxil tulajdonságain alapul, hogy oldható komplex vegyületeket képezzenek, gyakran kékre (fenol) vagy lilára (rezorcin, szalicilsav), ritkábban vörösre (PAS - nátrium) és zöldre (kinoszol) festenek.
A komplex összetételét, következésképpen színüket a fenolos hidroxilcsoportok (fenol - kék, rezorcin - lila) mennyisége és más funkciós csoportok hatása határozza meg.

2. Brómozási reakció aromás gyűrű. Az o- és n-helyzetű hidrogén brómmal való elektrofil szubsztitúcióján alapul, így oldhatatlan brómszármazék keletkezik.
 A brómozás alapvető szabályai
A brómozás alapvető szabályai
A bróm helyettesíti a hidrogént az o- és n-helyzetben a fenolos hidroxilcsoporthoz képest (a leghatékonyabb n-helyzet):
 - ha az aromás gyűrű o- vagy n-helyzetében szubsztituensek vannak, akkor kevesebb brómatom lép be a reakcióba:
- ha az aromás gyűrű o- vagy n-helyzetében szubsztituensek vannak, akkor kevesebb brómatom lép be a reakcióba:
 - ha az o- vagy n-helyzetben karboxilcsoport van, akkor feleslegben lévő bróm jelenlétében dekarboxilezés következik be, és tribróm-származék képződik:
- ha az o- vagy n-helyzetben karboxilcsoport van, akkor feleslegben lévő bróm jelenlétében dekarboxilezés következik be, és tribróm-származék képződik:
Ha a szubsztituens az m-helyzetben van, akkor nem zavarja a tribróm-származék képződését:

Ha egy vegyület m-helyzetben két fenolos hidroxilcsoportot tartalmaz, akkor ezek konzisztens orientációja következtében tribróm-származék keletkezik.

ha két hidroxilcsoport egymáshoz képest o- vagy n-helyzetben helyezkedik el, akkor ellentmondásosan hatnak: nem történik brómozás:

3.Azo-kapcsolási reakció fenolokat diazo-reagenssel (diazotizált szulfanilsavval), hogy narancsvörös színű azofestéket képezzenek.

4. Oxidációs reakció. A fenolok különféle vegyületekké oxidálhatók, de leggyakrabban kinonokká, rózsaszínre vagy ritkábban sárgára színezve.


5. Indofenol festék képződésének reakciója. Alapja a fenolok kinonokká történő oxidációja, amelyek ammóniával vagy amino-származékokkal és felesleges fenollal kondenzálva indofenol-festéket, ibolyát képeznek.


6. Kondenzációs reakció aldehidekkel vagy savanhidridekkel:
Formaldehiddel tömény kénsav jelenlétében vörös színű aurinsav (aril-metán) festéket képezve.
A reakció a szalicilsav gyógyszerkönyvében található.

A tömény kénsav a reakció első szakaszában vízeltávolító szerként, a másodikban oxidálószerként működik.
A rezorcin reakció kémiája

Egyértékű fenolok (arenolok). Elnevezéstan. Izomerizmus. Megszerzési módszerek. Fizikai tulajdonságok és szerkezet. Kémiai tulajdonságok: savasság, fenolátok, éterek és észterek képződése; a hidroxilcsoport nukleofil szubsztitúciója; reakciók elektrofil reagensekkel (halogénezés, nitrálás, nitrozálás, azokapcsolás, szulfonálás, acilezés és alkilezés); kölcsönhatás formaldehiddel, fenol-formaldehid gyantákkal; oxidációs és hidrogénezési reakciók.
Kétatomos fenolok (aréndiolok): pirokatekol, rezorcin, hidrokinon. Előkészítési módszerek, tulajdonságok és alkalmazások.
Háromértékű fenolok (arenetriolok): pirogallol, hidroxihidrokinon, floroglucinol. Előkészítési módszerek, tulajdonságok és alkalmazások.
Arénok hidroxil származékai
A fenolok aromás szénhidrogének származékai, amelyekben egy vagy több hidroxilcsoport közvetlenül kapcsolódik a benzolgyűrűhöz.
A magban lévő hidroxilcsoportok számától függően megkülönböztetünk egy-, két- és háromatomos fenolokat.
A fenolok elnevezésére gyakran triviális elnevezéseket használnak (fenol, krezolok, pirokatekol, rezorcin, hidrokinon, pirogallol, hidroxihidrokinon, floroglucinol).
A szubsztituált fenolokat fenolszármazékoknak vagy a megfelelő aromás szénhidrogén hidroxi-származékainak nevezzük.
Egyértékű fenolok (arenolok) Ar-OH
orto-krezol meta-krezol para-krezol
2-metil-fenol 3-metil-fenol 4-metil-fenol
2-hidroxitoluol 3-hidroxitoluol 4-hidroxitoluol
Az aromás sorozatban vannak olyan vegyületek is, amelyek az oldalláncban hidroxilcsoportot tartalmaznak - az úgynevezett aromás alkoholok.
Az aromás alkoholokban lévő hidroxilcsoport tulajdonságai nem különböznek az alifás alkoholok tulajdonságaitól.
Kétatomos fenolok (aréndiolok)

pirokatechin rezorcin hidrokinon
1,2-dihidroxibenzol 1,3-dihidroxibenzol 1,4-dihidroxibenzol
Háromértékű fenolok (arenetriolok)

pirogallol hidroxihidrokinon floroglucinol
1,2,3-trihidroxi-benzol 1,2,4-trihidroxi-benzol 1,3,5-trihidroxi-benzol
Egyértékű fenolok
Megszerzési módszerek
A fenol és homológjainak természetes forrása a szén, amelynek száraz desztillációja során kőszénkátrány képződik. A gyanta desztillálásakor fenolt és krezolokat tartalmazó „karbololaj” frakció (t 0 160-230 0 C) keletkezik.
1. Aromás szulfonsavak sóinak fúziója lúgokkal
A reakció alapja a fenolok előállítására szolgáló ipari eljárások.
A reakció abból áll, hogy benzolszulfonsavat szilárd lúggal (NaOH, KOH) hevítenek 250-300 0 C hőmérsékleten:
A reakció a nukleofil szubsztitúció mechanizmusával megy végbe S N 2 aroma(csatolás-leválás).
Az elektronvonó szubsztituensek jelenléte a szubsztitúció helyéhez képest orto- és para-helyzetben megkönnyíti a nukleofil szubsztitúciós reakciót.
2. Aril-halogenidek hidrolízise
Az aril-halogenidek, amelyek nem tartalmaznak aktiváló elektronvonó szubsztituenseket, nagyon kemény körülmények között reagálnak.
Így a klór-benzolt tömény lúg hatására 350-400 0 C hőmérsékleten és 30 MPa nagy nyomáson fenolgá hidrolizálják, vagy katalizátorok - rézsók és magas hőmérsékleten - jelenlétében:

A reakció a nukleofil szubsztitúció (eliminációs-addíciós) (arin vagy kine mechanizmus) mechanizmusa szerint megy végbe.
Az elektronszívó szubsztituensek jelenléte a halogénhez képest orto és para helyzetben jelentősen megkönnyíti a hidrolízis reakcióját.
Így a para-nitroklór-benzol képes a klórt hidroxilra helyettesíteni, ha hagyományos, lúgos oldattal melegítjük, légköri nyomáson:
 para-nitroklór-benzol para-nitro-fenol
para-nitroklór-benzol para-nitro-fenol
A reakció a mechanizmus szerint megy végbe S N 2
aroma(csatolás-leválás).
3. Fenol előállítása kumolból (kumen módszer)
A kumol alapú szintézis ipari jelentőségű és értékes, mert lehetővé teszi, hogy olcsó alapanyagokból (olaj, kőolaj krakkológázok) egyszerre két műszakilag fontos terméket (fenol és aceton) nyerjünk.
A kumén (izopropil-benzol), amikor a légköri oxigén oxidálja, hidroperoxiddá alakul, amely vizes savoldat hatására fenolra és acetonra bomlik: 
hidroperoxid fenol-aceton
4. Arénok hidroxilezése
A hidroxilcsoportnak a benzolgyűrűbe való közvetlen beviteléhez hidrogén-peroxidot használnak katalizátorok (vas (I) vagy réz (I) sók) jelenlétében:
5. Karbonsavak oxidatív dekarboxilezése
A fenolokat aromás savakból nyerik úgy, hogy vízgőzt és levegőt vezetnek be a reaktorba 200-300 0 C hőmérsékleten, rézsók (P) jelenlétében:
6. Előállítás diazóniumsókból
Amikor az arendiazónium-sókat vizes oldatban hevítik, nitrogén szabadul fel, és fenolok keletkeznek: 
A fenolok fizikai tulajdonságai
Normál körülmények között a legegyszerűbb fenolok alacsony olvadáspontú, színtelen, jellegzetes szagú kristályos anyagok.
A fenolok vízben gyengén, de szerves oldószerekben jól oldódnak. Levegőn tárolva az oxidációs folyamatok következtében elsötétednek.
Mérgező anyagok és égési sérüléseket okoznak.
A fenol elektronikus szerkezete
Az elektronsűrűség szerkezete és eloszlása egy fenolmolekulában a következő diagrammal ábrázolható:

A hidroxilcsoport az 1. típusú szubsztituens, azaz. elektrondonor szubsztituens.
Ennek oka az a tény, hogy a hidroxil-oxigénatom egyik magányos elektronpárja p,π-konjugációba lép a benzolgyűrű π-rendszerével, és +M hatást mutat.
Másrészt a hidroxilcsoport az oxigén nagyobb elektronegativitása miatt –I hatást mutat.
A fenolokban azonban a +M hatás sokkal erősebb, mint az ellentétes irányú –I effektus (+M > -I).
A kapcsolási hatás eredménye:
1) az O-H kötés polaritásának növekedése, ami a fenolok savas tulajdonságainak növekedéséhez vezet az alkoholokhoz képest;
2) a konjugáció következtében a fenolokban a C-OH kötés rövidebbé és erősebbé válik az alkoholokhoz képest, mivel részben kettős természetű. Ezért az OH-csoport szubsztitúciós reakciók bonyolultak;
3) a benzolgyűrű orto- és para-helyzetében lévő szénatomokon az elektronsűrűség növekedése megkönnyíti a hidrogénatomok elektrofil szubsztitúciós reakcióit ezekben a helyzetekben.

A fenolok kémiai tulajdonságai
A fenolok kémiai tulajdonságait egy hidroxilcsoport és egy benzolgyűrű jelenléte határozza meg a molekulában.
1. Reakciók a hidroxilcsoporton
1. Savas tulajdonságok
A fenolok gyenge OH-savak, de sokkal erősebbek, mint az alkanolok. Savasság állandó rK A fenol egyenlő 10.
A fenol magasabb savasságát két tényező magyarázza:
1) az O-H kötés nagyobb polaritása a fenolokban, aminek eredményeként a hidroxilcsoport hidrogénatomja nagyobb mobilitásra tesz szert, és proton formájában eltávolítható. fenolát ion;
2) A fenolát ion az oxigén magányos párnak a benzolgyűrűvel való konjugációja miatt mezomeresen stabilizálódik, azaz. a fenolátion oxigénatomjának negatív töltése jelentősen delokalizálódik:

E határszerkezetek egyike sem írja le önmagában a molekula tényleges állapotát, de használatuk lehetővé teszi számos reakció magyarázatát.
Az elektronszívó szubsztituensek növelik a fenol savas tulajdonságait.
Azáltal, hogy a benzolmagból elektronsűrűséget vonnak ki maguk felé, fokozzák a p,π-konjugációt (+M-effektus), ezáltal növelik az O-H kötés polarizációját és növelik a hidroxilcsoport hidrogénatomjának mobilitását.
Például:
 fenol 2-nitro-fenol 2,4-dinitro-fenol pikrinsav
fenol 2-nitro-fenol 2,4-dinitro-fenol pikrinsav
рК а 9,98 7,23 4,03 0,20
Az elektrondonor szubsztituensek csökkentik a fenolok savasságát.
1. A fenolos hidroxilcsoport helyettesítése halogénnel
A fenolokban lévő hidroxilcsoportot nagyon nehéz halogénnel helyettesíteni.
Amikor a fenol reagál foszfor-pentaklorid PCl 5-tel, a fő termék a trifenil-foszfát, és csak kis mennyiségű klór-benzol képződik:
Trifenil-foszfát klór-benzol
Az elektronvonó szubsztituensek jelenléte a hidroxilcsoporthoz képest orto- és para-helyzetben nagymértékben megkönnyíti az OH-csoport nukleofil szubsztitúciós reakcióit.
Így a pikrinsav azonos körülmények között könnyen átalakul 2,4,6-trinitroklór-benzollá (pikril-klorid):  pikrinsav pikril-klorid
pikrinsav pikril-klorid
2. Kölcsönhatás ammóniával
Amikor ammóniával kölcsönhatásba lép emelt hőmérsékleten és nyomáson alumínium-klorid katalizátor jelenlétében, az OH-csoportot NH2-csoport helyettesíti, és anilint képez:
 fenol-anilin
fenol-anilin
3. Fenol redukció
Amikor a fenolt lítium-alumínium-hidriddel redukáljuk, benzol képződik:
3. A benzolgyűrűt érintő reakciók
1. Elektrofil szubsztitúciós reakciók a benzolgyűrűben
A hidroxilcsoport az 1. típusú szubsztituens, ezért a benzolgyűrűben az elektrofil szubsztitúciós reakciók fenolokkal sokkal könnyebben mennek végbe, mint a benzolnál, és a szubsztituensek az orto és para helyzetbe irányulnak.

1) Halogénezési reakciók
A fenol könnyen reagál a brómos vízzel szobahőmérsékleten, és fehér 2,4,6-tribróm-fenol csapadékot képez:

2,4,6-tribróm-fenol
Ez a reakció a fenolokra kvalitatív.
A fenol klórozása könnyen megtörténik:

2) Nitrálási reakciók
A fenol könnyen nitrálható híg salétromsavval 0 0 C hőmérsékleten, így orto- és para-izomerek keveréke keletkezik, túlsúlyban az ortoizomer: 
orto- és para-nitro-fenolok
Az izomer nitrofenolok könnyen elválaszthatók, mivel csak az orto-izomer illékony a vízgőzzel.
Az orto-nitrofenolok nagyobb illékonysága az intramolekuláris hidrogénkötésekkel magyarázható, míg a para-izomer intermolekuláris hidrogénkötéseket hoz létre: 
Tömény salétromsav használatakor 2,4,6-trinitro-fenol (pikrinsav) képződik:
 pikrinsav
pikrinsav
3) Szulfonációs reakciók
A fenol szobahőmérsékleten könnyen szulfonálható tömény kénsavval, így ortoizomer keletkezik, amely 100 0 C feletti hőmérsékleten para-izomerré rendeződik át:

4) Alkilezési reakciók
A fenolok könnyen alkilezési reakciókon mennek keresztül.
A halogén-alkánokat, alkanolokat és alkéneket alkilezőszerként használják protikus savak (H 2 SO 4, H 3 PO 4) vagy Lewis-savak (AlCl 3, BF 3) jelenlétében: 

5) Acilezési reakciók
A fenolok acilezése könnyen megtörténik halogén-anhidridek vagy karbonsav-anhidridek hatására Lewis-savak jelenlétében: 
6) Nitrozációs reakciók
A nitrozofenolokat fenolok közvetlen nitrozálásával állítják elő:

para-krezol orto-nitrozo-para-krezol
7) Azo-kapcsolási reakciók
A fenolokkal való kombináció vezet enyhén lúgos környezet, mivel a fenolátion sokkal aktívabb, mint maga a fenol:

8) Kondenzációs reakciók
A fenolok olyan aktív komponensek az elektrofil szubsztitúciós reakciókban, hogy savak és bázisok jelenlétében kölcsönhatásba lépnek nagyon gyenge elektrofilekkel - aldehidekkel és ketonokkal.
Kondenzáció formaldehiddel
A formaldehid legkönnyebben kondenzációs reakcióba lép.
Ha a fenol és a formaldehid kondenzációs reakcióját enyhe körülmények között hajtjuk végre, lehetséges az orto- és para-hidroxi-metil-fenolok izolálása: Egyéni képviselők
Fenol– kristályos anyag, op. 43°C, jellegzetes csípős szagú, égési sérüléseket okoz a bőrön. Ez az egyik első antiszeptikum, amelyet az orvostudományban használnak. Nagy mennyiségben használják műanyagok (formaldehiddel történő kondenzáció), gyógyszerek (szalicilsav és származékai), színezékek, robbanóanyagok (pikrinsav) előállítására.
fenol-metil-éter - anizol– aromás anyagok és színezékek előállítására használják.
fenol-etil-éter - fenotol.
Krezolok (metil-fenolok) műanyagok, színezékek és fertőtlenítőszerek gyártásához használják.
A fenolos hidroxilcsoport egy aromás gyűrűhöz kapcsolódó hidroxilcsoport.
1. A sav-bázis tulajdonságok egy mozgó hidrogénatom jelenlétének köszönhetőek a fenolos hidroxilben. A hidroxil elektronpárja az aromás gyűrű felé tolódik el, ezért a savas tulajdonságai erősebbek, mint az alkoholoké. Tehát a szénsav pKa = 6,35 és a fenol pKa = 9,89.
A fenolok lúgok vizes oldatában fenolátok (fenoxidok) képződése közben oldódnak fel:
A fenolok savas természete azonban annyira jelentéktelen, hogy még egy olyan gyenge sav is, mint a szénsav, kiszorítja a fenolokat sóikból:
Ezért a lúgokban oldódó fenolok nem tudnak karbonátokban oldódni, mert az ilyenkor felszabaduló szénsav azonnal lebontja a fenolátot:
A fenolokat ez a tulajdonság különbözteti meg a karbonsavaktól.
A hőmérséklet emelkedésével a reakció előrefelé halad. Az alkálifém-fenolátok, mint erős bázisok és gyenge savak sói, vizes oldatokban részben hidrolizálódnak, ezért a fenolátok oldatai lúgos reakcióba lépnek.
2. Észterezési reakció (hasonlóan az alkohol-hidroxilhez).
Az éterek képződése fenolátok és alkil-halogenidek (vagy alkil-szulfátok) reakciója.
C6H5ONa+JCH3®C6H5OCH3+NaJ
Az észterek nátrium-fenolátok és anhidridek (vagy savkloridok) reakciójával keletkeznek.
3. Redox tulajdonságok.
A fenolok erős redukáló tulajdonságokat mutatnak, és nagyon könnyen oxidálódnak még gyenge oxidálószerek hatására is, aminek eredményeként színes, kinoid szerkezetű vegyületek képződnek.
 | [O] – CaOCl 2, H 2 O 2, Cl 2, Br 2 |
Az oxidációs reakcióra példa az indofenol-festék képződése: a keletkező kinon NH 3-mal kölcsönhatásba lépve kinon-iminné alakul, amely reakcióba lép az el nem reagált fenollal. Ammónia jelenlétében kék színű indofenol képződik.

kinonimin indofenol
n- benzokinoneimin
Az indofenol-reakció egy fajtája a Lieberman-nitrozo reakció, amely azokra a fenolokra jellemző, amelyekben nincsenek szubsztituensek az orto és para pozíciókban.
Ha savas környezetben nátrium-nitritnek van kitéve, képződik n-nitrozofenol, monooximmá izomerizálódik n-benzokinon, amely azután savas környezetben reagál a fenolfelesleggel, és indofenolt eredményez.

Megfigyelhető egy szín, amely lúgos oldat hozzáadásakor megváltozik:
fenol – sötétzöld, cseresznyepirossá válik;
timol – kékeszöld, lilává válik;
rezorcin – ibolya-fekete, ibolyaszínűvé válik;
hexestrol (sinestrol) – vörös-ibolya, cseresznyévé változik.
4. Komplexálási reakció vasionokkal.
A fenolos hidroxilcsoportok mennyiségétől, a molekulában lévő egyéb funkciós csoportok jelenlététől, egymáshoz viszonyított helyzetétől, a környezet pH-jától és hőmérsékletétől függően különböző összetételű és színű komplex vegyületek képződnek (a timol kivételével).



A komplexek színesek:
fenol – kék szín;
rezorcin – kék-lila szín;
szalicilsav - kék-lila vagy vörös-lila színű;
osalmid (oxafenamid) – vörös-ibolya szín;
nátrium-para-aminoszalicilát – vörös-lila színű;
quinosol – kékes-zöld színű.
A reakció a legtöbb fenolos vegyület esetében gyógyszerkönyvi.
5. Elektrofil szubsztitúciós reakciók – hidrogénatom SE az aromás gyűrűben (brómozás, kondenzáció aldehidekkel, kombináció diazóniumsókkal, nitrálás, nitrozálás, jódozás stb.). A fenolok elektrofil szubsztitúciós reakcióba való belépési képességét az oxigénatom magányos elektronpárjának és a benzolgyűrű π-elektronjainak kölcsönhatása magyarázza. Az elektronsűrűség az aromás gyűrű felé tolódik el. Az elektronsűrűség legnagyobb többlete a szénatomoknál figyelhető meg O-És n- a fenolos hidroxilcsoporthoz képest (I. típusú orientáns).
5.1. Halogénezési reakció (brómozás és jódozás).
5.1.1. A brómos vízzel való kölcsönhatás során a brómszármazékok fehér vagy sárga csapadékai képződnek.

Ha a bróm feleslegben van, oxidáció történik:

A fenolok brómozási reakciója a szubsztituensek természetétől és helyzetétől függ.
A jódozás hasonlóan történik, például:

5.1.2. Ha vannak szubsztituensek O-És n- az aromás gyűrű pozícióiban, az aromás gyűrű szubsztituálatlan hidrogénatomjai reagálnak.

5.1.3. Ha be O-És n- A fenolos hidroxilcsoporthoz képest karboxilcsoport van, majd a bróm feleslegének hatására dekarboxilezés megy végbe:

5.1.4. Ha egy vegyület két fenolos hidroxilcsoportot tartalmaz m- helyzetben, akkor bróm-tribróm-származékok képződnek (konzisztens orientáció):

5.1.5. Ha két hidroxilcsoport egymáshoz képest helyezkedik el O- vagy n- pozíciókban, akkor a brómozási reakció nem megy végbe (inkonzisztens orientáció)

5.2. Kondenzációs reakciók
5.2.1. Aldehidekkel.
A fenolok aldehidekkel való kondenzációjára példa a Marquis-reagenssel végzett reakció. Ha a fenolokat formaldehid oldattal tömény H 2 SO 4 jelenlétében hevítjük, színtelen kondenzációs termékek képződnek, amelyek oxidációja során intenzív színű, kinoid szerkezetű vegyületek keletkeznek. Ebben a reakcióban a kénsav dehidratáló, kondenzáló és oxidálószer szerepet játszik.

5.2.2. A fenolok reakciója kloroformmal (CHCl 3) aurine színezékekké.
Amikor a fenolokat kloroformmal lúgos környezetben hevítik, aurinák– trifenil-metán festékek:

Az aurinák színűek:
fenol – sárga szín;
timol – sárga szín, ami lilává változik;
rezorcin – vörös-ibolya szín.
5.2.3. Savanhidridekkel.
A. A fluoreszcein képződésének reakciója (rezorcin kondenzációja ftálsavanhidriddel).


B. Fenolftalein képződésének reakciója (fenol kondenzációja ftálsavanhidriddel).

Nagy feleslegben lévő lúg esetén triszubsztituált nátriumsó képződik.
A timol ftálsavanhidriddel történő kondenzációja hasonlóan megy végbe, mint a fenolftalein képződése, amely lúgos közegben kék színű.
5.3. Nitrálási reakció
A fenolok reakcióba lépnek a híg salétromsavval (HNO 3), és orto- és para-nitro-származékokat képeznek. Nátrium-hidroxid-oldat hozzáadása javítja a színt a jól disszociált só képződése miatt.

5.4. Fenolok azokapcsolásának reakciója diazóniumsóval lúgos közegben.
Amikor a fenolok reakcióba lépnek a diazóniumsóval 9-10 pH-értéken, azofestékek képződnek, amelyek sárgás-narancssárga vagy vörös színűek. Az azo-kapcsolási reakció a fenolos hidroxilcsoporthoz képest orto- és para-helyzetben megy végbe. Diazoreagensként általában diazotizált szulfanilsavat használnak.


Bevezetés
Az orvosi gyakorlatban használt gyógyszerek többsége szerves vegyület. Az ilyen anyagok azonosságát a funkciós csoportokkal való reakciók igazolják.
A funkciós csoport egy szerves vegyület molekulájában reaktív atom, atomcsoport vagy reakcióközpont.
A funkcionális analízis általános elve a meghatározandó csoportokra jellemző reakciók alkalmazása. A reakciónak nemcsak a lehető legspecifikusabbnak kell lennie, hanem kellően gyorsnak is kell lennie, és tartalmaznia kell egy könnyen azonosítható reagenst vagy reakcióterméket.

Az alkohol-hidroxil azonosítása
Alkoholok - Ezek olyan szénhidrogén-származékok, amelyek molekuláiban egy vagy több hidrogénatomot hidroxilcsoportok helyettesítenek. Általában egy alkoholmolekulát ROH-ként ábrázolhatunk.
Észterképződési reakció
Az alkoholok szerves savakkal vagy savanhidridekkel észtereket képeznek vízeltávolító szerek (például tömény kénsav) jelenlétében. A kis molekulatömegű alkoholokból nyert észterek jellegzetes szagúak, a nagy molekulatömegű alkoholokon alapuló észterek pedig kristályos anyagok, tiszta olvadásponttal.
Módszertan. 1 ml etanolhoz adjunk 5 csepp jégecetet, 0,5 ml tömény kénsavat, és óvatosan melegítsük fel; jellegzetes etil-acetát (friss alma) szag észlelhető.

Alkoholok oxidációs reakciója aldehidekké
A keletkező aldehideket a szag érzékeli. Oxidálószerként kálium-hexaciano-(III)-ferrátot, kálium-permanganátot, kálium-dikromátot stb.
Módszertan. Helyezzen 2 csepp etanolt, 1 csepp 10%-os kénsavoldatot és 2 csepp 10%-os kálium-dikromát oldatot az első kémcsőbe. Az így kapott megoldásnak van narancsszín. Láng felett addig melegítjük, amíg az oldat el nem kezd kékes-zöld színű(ugyanakkor jellegzetes acetaldehid szag érezhető, ami az Antonov alma illatára emlékeztet). Adjunk 1 cseppet a kapott oldatból egy második kémcsőbe 3 csepp fukszinkénsavval. Megjelenik rózsaszín-lila színű.
Komplex vegyületek képződésének reakciója
A többértékű alkoholok lúgos közegben (Fehling-reagenssel) réz-szulfáttal kék komplex vegyületeket képeznek.
Módszertan. 0,5 ml glicerinhez adjunk 5 csepp nátrium-hidroxid és réz(II)-szulfát oldatot, intenzív kék színezés.

A fenolos hidroxilcsoport azonosítása
Reakció vas(111)-kloriddal
A fenolokra jellemző minőségi reakció a vas(III)-kloriddal való reakció. A fenolos hidroxilcsoportok mennyiségétől, a fenolmolekulában lévő egyéb funkciós csoportok jelenlététől, relatív helyzetüktől, a környezet pH-jától és hőmérsékletétől függően változatos összetételű és színű komplex vegyületek képződnek.
Módszertan. 0,01 g hatóanyaghoz 1 ml vízben (fenolhoz, rezorcinhoz) 2 csepp vas(III)-klorid oldatot adunk - jellegzetes elszíneződés figyelhető meg (1. táblázat).
1. táblázat Preparációs komplexek festése vas(III)-kloriddal
|
Drog |
Oldószer |
A komplexum színezése |
|
Lila |
||
|
Rezorcin |
Kék ibolya |
|
|
Adrenalin-hidroklorid |
Smaragdzöld, egy csepp ammóniaoldat hozzáadása helyett cseresznyepiros, majd narancsvörös. |
|
|
Morfin-hidroklorid |
Kék, hígított ecetsav vagy sósav hozzáadásával eltűnik |
|
|
Paracetamol |
Kék ibolya |
|
|
Piridoxin-hidroklorid |
Vörös, híg sósav hozzáadásával eltűnik, és híg ecetsavval nem tűnik el. |
|
|
Szalicilsav és nátrium-szalicilát |
Kék ibolya, nem tűnik el néhány csepp hígított sósav vagy ecetsav hozzáadásával. |
|
|
Fenil-szalicilát |
lila, hígított sósav vagy ecetsav hozzáadása után eltűnik és átalakul vérvörös 1-2 csepp ammóniaoldat hozzáadásával. |
Ammóniaoldat segítségével megkülönböztetheti a fenolt a rezorcintól. A reagens hozzáadása után a vas-rezorcin komplex színe megváltozik barnássárga.