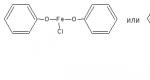
Fenolne hidroksilne grupe i antioksidativna aktivnost. Reakcija oksidacije alkohola u aldehide Reakcije na hidroksilnoj grupi
Fenolni hidroksil je hidroksil vezan za aromatični radikal. Sadrži lijekove iz grupe fenola (fenol, resorcinol); fenolne kiseline i njihovi derivati (salicilna kiselina, fenil salicilat, salicilamid, oksafenamid); derivati fenantren izohinolina (morfijum hidrohlorid, apomorfin); sinestrol, adrenalin itd.
Hemijska svojstva spojeva koji sadrže fenol hidroksil određuju se interakcijom elektronskog para sa π-elektronima aromatičnog prstena. Ova interakcija dovodi do pomaka elektronske gustine iz OH grupe u prsten, narušavanja jednolike distribucije elektrona u njemu i stvaranja viška negativnog naboja u orto ( O)- i par ( P)-pozicije. Atom vodonika hidroksi grupe jonizuje i daje fenolima slaba kisela svojstva (pKa fenola = 10,0; pKa resorcinola = 9,44). Stoga, za razliku od alkohola, formiraju soli sa alkalijama (pri pH 12-13), rastvorljiva kompleksna jedinjenja sa gvožđem (III) hloridom (u neutralnim, slabo alkalnim i kiselim rastvorima).
Fenoli pokazuju jaka redukcijska svojstva i vrlo se lako oksidiraju čak i slabim oksidantima. Formiraju obojena jedinjenja hinoidne strukture.
Reakcije elektrofilne supstitucije vodonika u O- I P-položaji aromatičnog prstena – halogeniranje (bromiranje), kondenzacija sa aldehidima, nitriranje, kombinacija sa diazonijum solima.
Na osnovu svojstava fenolnog hidroksila i aromatičnog prstena koji se njime aktivira, u analizi lijekova koriste se sljedeće reakcije:
1 – kompleksna formacija;
2 – halogeniranje (bromiranje);
3 – azo kombinacije;
4 – oksidacija;
5 – formiranje indofenolne boje;
6 – kondenzacija sa aldehidima.
Identifikacija
2.1. Reakcija kompleksiranja sa ionima gvožđa (III)
Zasnovan je na svojstvima fenolnog hidroksila da formira rastvorljiva kompleksna jedinjenja, često obojena plavo (fenol) ili ljubičasto (resorcinol, salicilna kiselina), rjeđe crveno (PAS - natrijum) i zeleno (kinosol, adrenalin).
Sastav kompleksa, a samim tim i njihova boja determinisani su količinom fenolnih hidroksila, uticajem drugih funkcionalnih grupa i reakcijom sredine.
Ako postoji višak fenola:

Pretpostavljeni sastav konačnog proizvoda u reakciji sa fenolom:


2.2. Reakcija bromiranja aromatičnog prstena
Zasnovano na elektrofilnoj supstituciji vodonika u O- I P- pozicije na bromu sa formiranjem nerastvorljivog derivata broma (bijeli talog).

Osnovna pravila za bromiranje:
Brom zamjenjuje vodonik O- I P- pozicije u odnosu na fenolni hidroksil (najreaktivniji je P- pozicija):

Ako je dostupno u O- ili P- položaji aromatičnog prstena supstituenata, manje atoma broma reaguje;
Ako u O- ili P- pozicijama nalazi se karboksilna grupa, zatim u prisustvu viška broma dolazi do dekarboksilacije i stvaranja tribromo derivata:

Ako je zamjenik unutra m- položaj, onda ne ometa nastanak tribromo derivata:

Ako spoj sadrži dva fenolna hidroksila u m- položaj, tada se kao rezultat njihove koordinirane orijentacije formira tribromo derivat:

Ako se nalaze dvije hidroksilne grupe u O- ili P- položajima jedni prema drugima, djeluju nekonzistentno: bromiranje se ne događa kvantitativno:

Ako, pored fenolnih hidroksila, spoj sadrži amidnu ili estarsku grupu (salicilamid, fenil salicilat), neophodna je preliminarna hidroliza za njihovu kvantitativnu procjenu bromatometrijom.
2.3. Reakcija azo spajanja
Kombinacija takođe ide na O- I P- odredbe, u ovom slučaju, kao i kod bromiranja, poželjno je P- pozicija. Diazo reagens je diazonijumova so (diazotizovana sulfanilna kiselina). Okruženje je alkalno. Produkt reakcije je azo boja.

2.4. Reakcija oksidacije
Fenoli se mogu oksidirati u različite spojeve, ali najčešće u O- ili P-kinoni (ciklični diketoni), obojeni ružičasto ili, rjeđe, žuto.


2.5. Reakcija stvaranja indofenolne boje
Zasnovan je na oksidaciji fenola u kinone, koji, kada se kondenzuju sa amonijakom ili amino derivatom i viškom fenola, formiraju indofenolnu boju, obojenu u ljubičastu boju.


Varijacija ove reakcije je Liebermanova nitro reakcija; ona je karakteristična za fenole koji nemaju supstituente O- I P- odredbe.
Kada je izložen natrijum nitritu u kiseloj sredini, formira se P-nitrozofenol, izomerizirajući u P- kinoidoksim, koji, reagirajući s viškom fenola u kiseloj sredini, stvara indofenol:

2.6. Formiranje nitrozo jedinjenja
Pri interakciji s razrijeđenom dušičnom kiselinom, fenoli se mogu nitrirati na sobnoj temperaturi, formirajući O- I P- nitro derivati. Rezultirajući nitro derivat sadrži P- položaj mobilnog vodikovog atoma hidroksilne grupe, formira se tautomerni kiseli oblik sa kvinoidnom strukturom, obično je obojen žuto. Dodavanje lužine pojačava boju zbog stvaranja dobro disocirane soli:

2.7. Reakcija kondenzacije s aldehidima ili anhidridima kiselina
Sa formaldehidom u prisustvu koncentrovane sumporne kiseline za formiranje aurične (arilmetanske) boje crvene boje.
Reakcija je farmakopejska za salicilnu kiselinu. Koncentrirana sumporna kiselina igra ulogu sredstva za uklanjanje vode u prvoj fazi reakcije, au drugoj djeluje kao oksidant.
Uz ftalni anhidrid (fuzija i naknadno otapanje taline u lužini) preporučuje se farmakopeja za identifikaciju fenola i rezorcinola.

kvantitacija
2.8. Bromatometrija
Metoda se zasniva na elektrofilnoj supstituciji atoma vodika aromatičnog prstena sa bromom, izolovanim u reakciji kalijum bromata sa kalijum bromidom u kiseloj sredini.
K  BrO 3 + 5KBr + 6 HCl → 3Br 2 + 6KCl + 3H 2 O
BrO 3 + 5KBr + 6 HCl → 3Br 2 + 6KCl + 3H 2 O
Koriste se metode direktne i reverzne titracije. Direktno - titrirati kalijum bromatom u prisustvu kalijum bromida sa metil narandžastim ili metil crvenim indikatorom od ružičaste do obezbojene. U tački ekvivalencije, višak kapi kalijum bromata oslobađa brom, koji oksidira indikator i otopina postaje bezbojna. Prilikom povratne titracije unosi se višak kalijum bromata, dodaje se kalijum bromid, stvara se kisela sredina, održava se vreme potrebno za bromiranje, a zatim se višak broma određuje jodometrijski (škrob kao indikator).
Br 2 + 2KI → I 2 + 2KBr
I 2 + 2Na 2 S 2 O 3 → Na 2 S 4 O 6 + 2NaI
Direktnom titracijom timol se određuje GF, a fenol, resorcinol, salicilna kiselina, sinestrol i drugi lijekovi reverznom titracijom.
M.e. = ¼ M.m. (timol)
M.e. = 1/6 M.m. (fenol, resorcinol, salicilna kiselina)
M.e. = 1/8 M.m. (sinestrol)
2.9. Jodometrija
Zasnovano na elektrofilnoj supstituciji atoma vodika aromatičnog prstena jodom.

Za vezanje jodovodične kiseline, koja pomiče ravnotežu u suprotnom smjeru, dodaje se natrijum acetat ili natrijum bikarbonat.
HI + NaHCO 3 → NaI + H 2 O + CO 2
HI + CH 3 COONa → NaI + CH 3 COOH
Koriste se metode direktne i reverzne titracije. U potonjem, višak joda titrira se natrijum tiosulfatom.
I 2 + 2NaS 2 O 3 → 2NaI + Na 2 S 4 O 6
M.e. = 1/6 M.m. (fenol)
2.10. Jodna hlorometrija
Metoda se zasniva na elektrofilnoj supstituciji vodonikovih atoma aromatičnog prstena jodom, koji je dio jod monohlorida.

Koristi se metoda povratne titracije - višak jod monohlorida se određuje jodometrijski.
ICl + KI → I 2 + KCl
I 2 + 2Na 2 S 2 O 6 → 2NaI + Na 2 S 4 O 6
M.e. = 1/6 M.m. (fenol)
2.11. Metoda acetilacije
Koristi se prema GF X za kvantitativnu procjenu sinestrola.

M.e. = ½ M.m.
2.12. Alkalometrijska metoda neutralizacije u protofilnom rastvaraču dimetilformamidu (DMF).
Ljekovite grupe fenola pokazuju vrlo slaba kisela svojstva, njihovo određivanje alkalimetrijskom metodom neutralizacije u vodenoj ili miješanoj sredini je nemoguće, pa se titracija koristi u mediju nevodenih rastvarača, posebno DMF-a. Metoda se zasniva na formiranju soli određene slabe kiseline (fenol) sa titrantom (natrijum metilat) u protofilnom otapalu koje pojačava kisela svojstva.

Ukupno:

2.13. Fotokolorimetrija (FEC) i spektrofotometrija (SPM)
Zasniva se na svojstvu obojenih rastvora da apsorbuju nemonohromatsku (FEC) ili monohromatsku (SPM) svetlost u vidljivom delu spektra.
Dobivanje obojenih otopina;
Mjerenje optičke gustoće (D), koja karakterizira apsorpciju elektromagnetnog zračenja otopinom koja sadrži analit;
Izvođenje proračuna na osnovu osnovnog zakona apsorpcije svjetlosti korištenjem kalibracionog grafikona, specifičnog koeficijenta apsorpcije i standardnog uzorka otopine.
Prilikom određivanja lijekova koji sadrže fenol hidroksil ovim metodama, obojena jedinjenja se dobijaju na osnovu reakcija kompleksiranja sa ionima gvožđa (III), azo kuplovanja sa diazonijum solima i formiranja indofenolne boje.
Predavanje br. 14
Tema: “Kvalitativne reakcije na funkcionalne grupe”
1) hidroksil (alkohol, fenol)
2) karbonil (aldehid, karboksil, ester)
3) Primarna aromatična amino grupa, tercijarna amino grupa (tercijarni dušik)
4) Imid, sulfamid.
Funkcionalne grupe (FG) su pojedinačni atomi ili grupe atoma povezanih s ugljikovim radikalom, koji se zbog svojih karakterističnih svojstava mogu koristiti za definiranje ljekovitih tvari.
I. Alkohol hidroksil. Alr-OH je hidroksil vezan za alifatski ugljikovodični radikal.
Na osnovu alkohola hidroksila, u analizi lijekova koji ga sadrže koriste se sljedeće reakcije:
Esterifikacija (formiranje estera sa kiselinama ili njihovim anhidridima);
Oksidacija u aldehide, au nekim slučajevima i u kiseline;
Kompleksacija sa ionima bakra (II) u alkalnoj sredini.
1.Reakcija esterifikacije u prisustvu sredstava za uklanjanje vode sa kiselinama ili njihovim anhidridima. Zasnovan na svojstvu alkohola da formira estre. U slučaju jedinjenja male molekulske mase, estri se detektuju mirisom kada se analiziraju lekovi sa visokom molekulskom težinom, po tački topljenja;
Reakcija esterifikacije je farmakopeja za etil alkohol.
CH 3 CH 2 OH + CH 3 COOH H2SO4→ CH 3 CH 2 OCOCH 3
2. Reakcija oksidacije, zasnovano na svojstvu alkohola da oksidiraju u aldehide, koji se otkrivaju mirisom. Kao reagensi se koriste različiti oksidanti: kalijum permanganat, kalijum bihromat, kalijum heksacijanoferat (III) itd. Najveću analitičku vrednost ima kalijum permanganat, koji pri redukciji menja oksidaciono stanje sa +7 na +2 i gubi boju, tj. čini reakciju efikasnom.

Reakcija kompleksiranja, zasnovan na svojstvu alkohola da formiraju obojena kompleksna jedinjenja sa bakar (II) sulfatom u alkalnoj sredini.

Koristi se za identifikaciju polihidričnog alkohola - glicerola i efedrin hidroklorida, u kojem, pored alkoholnog hidroksila, u formiranju kompleksa sudjeluje i sekundarna aminska grupa.
Fenolni hidroksil je hidroksil vezan za aromatični radikal. Sadrži fenole grupe lijekova (fenol, resorcinol); fenolne kiseline i njihovi derivati (salicilna kiselina, fenil salicilat, salicilamid, oksafenamid); derivati fenantren izohinolina (morfijum hidrohlorid, apomorfin); sinestrol, adrenalin, mezaton itd.
Hemijska svojstva spojeva koji sadrže fenol hidroksil određuju se interakcijom elektronskog para sa π elektronima aromatičnog prstena. Ova interakcija dovodi do pomaka u gustoći elektrona iz OH - grupe u prsten, narušavanja ravnomjerne raspodjele elektrona u njemu i stvaranja viška negativnog naboja u orto i para pozicijama. Atom vodika hidroksi grupe ionizira i daje fenolima slaba kisela svojstva, koja se, međutim, rijetko koriste u analizi. Reakcije elektrofilne supstitucije vodonika u o- i n-položajima aromatičnog prstena su od najveće važnosti.
Na osnovu svojstava fenolnog hidroksila koriste se sljedeće reakcije:
Kompleksacija;
bromiranje;
Kombinacije azoze;
Oksidacija;
Formiranje indofenolne boje;
Kondenzacija
1. Reakcije kompleksiranja fenolni hidroksil sa ionima gvožđa (III). Zasnovan je na svojstvima fenolnog hidroksila da formira rastvorljiva kompleksna jedinjenja, često obojena plavo (fenol) ili ljubičasto (resorcinol, salicilna kiselina), rjeđe crveno (PAS - natrijum) i zeleno (kinosol).
Sastav kompleksa, a samim tim i njihova boja je određena količinom fenolnih hidroksila (fenol - plavi, resorcinol - ljubičastim), i uticajem drugih funkcionalnih grupa.

2. Reakcija bromiranja aromatični prsten. Zasniva se na elektrofilnoj supstituciji vodika u o- i n-položaju sa bromom da bi se formirao nerastvorljivi derivat broma.
 Osnovna pravila za bromiranje
Osnovna pravila za bromiranje
Brom zamjenjuje vodonik na o- i n-položajima u odnosu na fenolni hidroksil (najefikasniji n-položaj):
 - ako postoje supstituenti na o- ili n-položajima aromatskog prstena, manje atoma broma ulazi u reakciju:
- ako postoje supstituenti na o- ili n-položajima aromatskog prstena, manje atoma broma ulazi u reakciju:
 - ako postoji karboksilna grupa na o- ili n- pozicijama, tada u prisustvu viška broma dolazi do dekarboksilacije i stvaranja tribromo derivata:
- ako postoji karboksilna grupa na o- ili n- pozicijama, tada u prisustvu viška broma dolazi do dekarboksilacije i stvaranja tribromo derivata:
Ako je supstituent u m-poziciji, onda ne ometa nastanak tribromo derivata:

Ako spoj sadrži dva fenolna hidroksila na m-poziciji, tada se kao rezultat njihove konzistentne orijentacije formira tribromo derivat

ako se dvije hidroksilne grupe nalaze u o- ili n-položaju jedna prema drugoj, tada djeluju nekonzistentno: bromiranje se ne događa:

3. Reakcija Azo spajanja fenola sa diazo reagensom (diazotizovana sulfanilna kiselina) da bi se formirala azo boja, obojena narandžasto-crvenom bojom.

4. Reakcija oksidacije. Fenoli se mogu oksidirati u različite spojeve, ali najčešće u kinone, obojene u ružičasto ili, rjeđe, žuto.


5. Reakcija stvaranja indofenolne boje. Zasnovan je na oksidaciji fenola u kinone, koji, kada se kondenzuju sa amonijakom ili amino derivatima i viškom fenola, formiraju indofenolnu boju, obojenu u ljubičastu boju.


6. Reakcija kondenzacije sa aldehidima ili anhidridima kiselina:
Sa formaldehidom u prisustvu koncentrovane sumporne kiseline za formiranje aurinske (arilmetanske) boje obojene u crvenu boju.
Reakcija je farmakopejska za salicilnu kiselinu.

Koncentrirana sumporna kiselina igra ulogu sredstva za uklanjanje vode u prvoj fazi reakcije, au drugoj djeluje kao oksidant.
Hemija reakcije na resorcinol

Monohidrični fenoli (arenoli). Nomenklatura. Izomerizam. Metode dobijanja. Fizička svojstva i struktura. Hemijska svojstva: kiselost, stvaranje fenolata, etera i estera; nukleofilna supstitucija hidroksilne grupe; reakcije sa elektrofilnim reagensima (halogenacija, nitracija, nitrozacija, azo kuplovanje, sulfonacija, acilacija i alkilacija); interakcija sa formaldehidnim, fenol-formaldehidnim smolama; reakcije oksidacije i hidrogenacije.
Dvoatomski fenoli (arenedioli): pirokatehol, resorcinol, hidrokinon. Metode pripreme, svojstva i primjena.
Trihidrični fenoli (arenetrioli): pirogalol, hidroksihidrokinon, floroglucinol. Metode pripreme, svojstva i primjena.
Hidroksilni derivati arena
Fenoli su derivati aromatičnih ugljovodonika u kojima je jedna ili više hidroksilnih grupa direktno vezano za benzenski prsten.
U zavisnosti od broja hidroksilnih grupa u jezgru, razlikuju se jedno-, dvo- i troatomni fenoli.
Za imenovanje fenola često se koriste trivijalni nazivi (fenol, krezoli, pirokatehol, resorcinol, hidrokinon, pirogalol, hidroksihidrokinon, floroglucinol).
Supstituirani fenoli se nazivaju derivati fenola ili hidroksi derivati odgovarajućeg aromatičnog ugljovodonika.
Monohidrični fenoli (arenoli) Ar-OH
orto-krezol meta-krezol para-krezol
2-metilfenol 3-metilfenol 4-metilfenol
2-hidroksitoluen 3-hidroksitoluen 4-hidroksitoluen
U aromatičnom nizu nalaze se i jedinjenja sa hidroksilnom grupom u bočnom lancu - takozvani aromatični alkoholi.
Svojstva hidroksilne grupe u aromatičnim alkoholima ne razlikuju se od svojstava alifatskih alkohola.
Dvoatomski fenoli (arenedioli)

pyrocatechin resorcinol hydroquinone
1,2-dihidroksibenzen 1,3-dihidroksibenzen 1,4-dihidroksibenzen
Trihidrični fenoli (arenetrioli)

pirogalol hidroksihidrokinon floroglucinol
1,2,3-trihidroksibenzen 1,2,4-trihidroksibenzen 1,3,5-trihidroksibenzen
Monohidrični fenoli
Načini dobijanja
Prirodni izvor fenola i njegovih homologa je ugalj, pri čijoj suvoj destilaciji nastaje katran ugljena. Kada se smola destiluje, dobija se frakcija "karboličnog ulja" (t 0 160-230 0 C) koja sadrži fenol i krezole.
1. Fuzija soli aromatičnih sulfonskih kiselina sa alkalijama
Reakcija je u osnovi industrijskih metoda za proizvodnju fenola.
Reakcija se sastoji od zagrijavanja benzensulfonske kiseline sa čvrstom alkalijom (NaOH, KOH) na temperaturi od 250-300 0 C:
Reakcija se odvija mehanizmom nukleofilne supstitucije S N 2 aroma(attachment-detachment).
Prisustvo supstituenata koji povlače elektrone u orto i para položajima u odnosu na mjesto supstitucije olakšava nukleofilnu supstitucijsku reakciju.
2. Hidroliza aril halogenida
Aril halogenidi, koji ne sadrže aktivirajuće supstituente za povlačenje elektrona, reaguju u veoma teškim uslovima.
Tako se hlorobenzen hidrolizira u fenol djelovanjem koncentrirane lužine na temperaturi od 350-400 0 C i visokom pritisku od 30 MPa, ili u prisustvu katalizatora - soli bakra i visoke temperature:

Reakcija se odvija mehanizmom nukleofilne supstitucije (eliminacija-adicija) (arinski ili kine mehanizam).
Prisustvo supstituenata koji povlače elektrone u orto i para položajima u odnosu na halogen značajno olakšava reakciju hidrolize.
Dakle, para-nitroklorobenzen je sposoban zamijeniti hlor hidroksilom konvencionalnim zagrijavanjem s alkalnom otopinom pri atmosferskom tlaku:
 para-nitroklorobenzen para-nitrofenol
para-nitroklorobenzen para-nitrofenol
Reakcija se odvija prema mehanizmu S N 2
aroma(attachment-detachment).
3. Priprema fenola iz kumena (kumenska metoda)
Sinteza na bazi kumena je od industrijskog značaja i dragocena je jer omogućava istovremeno dobijanje dva tehnički važna proizvoda (fenol i aceton) od jeftinih sirovina (nafta, gasovi za krekiranje nafte).
Kumen (izopropilbenzen), kada se oksidira atmosferskim kisikom, prelazi u hidroperoksid, koji se pod djelovanjem vodene otopine kiseline razlaže u fenol i aceton: 
hidroperoksid fenol aceton
4. Hidroksilacija arena
Za direktno uvođenje hidroksilne grupe u benzenski prsten koristi se vodikov peroksid u prisustvu katalizatora (gvožđe (I) ili soli bakra (I):
5. Oksidativna dekarboksilacija karboksilnih kiselina
Fenoli se dobijaju iz aromatičnih kiselina propuštanjem vodene pare i vazduha u reaktor na temperaturi od 200-300 0 C u prisustvu soli bakra (P):
6. Priprema iz diazonijumovih soli
Kada se arendiazonijeve soli zagrijavaju u vodenim otopinama, oslobađa se dušik kako bi se proizveli fenoli: 
Fizička svojstva fenola
Najjednostavniji fenoli u normalnim uslovima su nisko topljive, bezbojne kristalne supstance sa karakterističnim mirisom.
Fenoli su slabo rastvorljivi u vodi, ali su veoma rastvorljivi u organskim rastvaračima. Kada se čuvaju na zraku potamne zbog procesa oksidacije.
Otrovne su tvari i uzrokuju opekline kože.
Elektronska struktura fenola
Struktura i distribucija elektronske gustine u molekuli fenola može se prikazati sledećim dijagramom:

Hidroksilna grupa je supstituent 1. vrste, tj. supstituent koji donira elektron.
To je zbog činjenice da jedan od usamljenih elektronskih parova hidroksilnog atoma kiseonika ulazi u p,π-konjugaciju sa π-sistemom benzenskog prstena, pokazujući +M efekat.
S druge strane, hidroksilna grupa, zbog veće elektronegativnosti kiseonika, ispoljava –I efekat.
Međutim, +M efekat u fenolima je mnogo jači od suprotnog -I efekta (+M > -I).
Rezultat efekta spajanja je:
1) povećanje polariteta O-H veze, što dovodi do povećanja kiselih svojstava fenola u odnosu na alkohole;
2) zbog konjugacije, C-OH veza u fenolima postaje kraća i jača u odnosu na alkohole, jer je djelimično dvostruke prirode. Stoga su reakcije supstitucije OH grupe teške;
3) povećanje elektronske gustine na atomima ugljenika u orto- i para-položajima benzenskog prstena olakšava reakcije elektrofilne supstitucije atoma vodonika u tim pozicijama.

Hemijska svojstva fenola
Hemijska svojstva fenola određena su prisustvom hidroksilne grupe i benzenskog prstena u molekuli.
1. Reakcije na hidroksilnu grupu
1. Svojstva kiselina
Fenoli su slabe OH-kiseline, ali mnogo jače od alkanola. Konstanta kiselosti rK A fenol je jednak 10.
Veća kiselost fenola se objašnjava sa dva faktora:
1) veći polaritet O-H veze u fenolima, usled čega atom vodika hidroksilne grupe dobija veću pokretljivost i može se eliminisati u obliku protona da nastane fenolat ion;
2) Fenolat jon je mezomerno stabilizovan zbog konjugacije usamljenog para kiseonika sa benzenskim prstenom, tj. negativni naboj na atomu kiseonika fenolatnog jona je značajno delokalizovan:

Nijedna od ovih graničnih struktura sama po sebi ne opisuje stvarno stanje molekula, ali njihova upotreba nam omogućava da objasnimo mnoge reakcije.
Supstituenti koji povlače elektrone povećavaju kisela svojstva fenola.
Privlačeći elektronsku gustoću iz jezgra benzena prema sebi, oni pojačavaju p,π-konjugaciju (+M-efekat), čime se povećava polarizacija O-H veze i povećava mobilnost atoma vodika hidroksilne grupe.
Na primjer:
 fenol 2-nitrofenol 2,4-dinitrofenol pikrinska kiselina
fenol 2-nitrofenol 2,4-dinitrofenol pikrinska kiselina
rK a 9,98 7,23 4,03 0,20
Supstituenti koji doniraju elektrone smanjuju kiselost fenola.
1. Zamjena fenolnog hidroksila sa halogenom
Hidroksilnu grupu u fenolima je vrlo teško zamijeniti halogenom.
Kada fenol reaguje sa fosfor pentakloridom PCl 5, glavni proizvod je trifenil fosfat i nastaju samo male količine hlorobenzena:
Trifenilfosfat hlorobenzen
Prisustvo supstituenata koji povlače elektrone u orto- i para-položajima u odnosu na hidroksil uvelike olakšava reakcije nukleofilne supstitucije OH grupe.
Tako se pikrinska kiselina pod istim uslovima lako pretvara u 2,4,6-trinitrohlorobenzen (pikril hlorid):  pikrinska kiselina pikril hlorid
pikrinska kiselina pikril hlorid
2. Interakcija sa amonijakom
Prilikom interakcije s amonijakom na povišenoj temperaturi i tlaku u prisutnosti katalizatora aluminij klorida, OH grupa se zamjenjuje NH 2 grupom kako bi se formirao anilin:
 fenol anilin
fenol anilin
3. Redukcija fenola
Kada se fenol redukuje litij-aluminijum hidridom, nastaje benzen:
3. Reakcije koje uključuju benzenski prsten
1. Reakcije elektrofilne supstitucije u benzenskom prstenu
Hidroksilna grupa je supstituent 1. vrste, pa se reakcije elektrofilne supstitucije u benzenskom prstenu odvijaju sa fenolima mnogo lakše nego sa benzenom, a supstituenti su usmereni na orto i para položaj.

1) Reakcije halogeniranja
Fenol lako reaguje sa bromnom vodom na sobnoj temperaturi da formira beli talog 2,4,6-tribromofenola:

2,4,6-tribromofenol
Ova reakcija je kvalitativna za fenole.
Kloriranje fenola je lako:

2) Reakcije nitracije
Fenol se lako nitrira razrijeđenom dušičnom kiselinom na temperaturi od 0 0 C kako bi se formirala mješavina orto i para izomera s prevlašću orto izomera: 
orto- i para-nitrofenola
Izomerni nitrofenoli se lako odvajaju zbog činjenice da je samo orto izomer isparljiv s vodenom parom.
Veća hlapljivost orto-nitrofenola objašnjava se stvaranjem intramolekularnih vodikovih veza, dok para-izomer formira intermolekularne vodikove veze: 
Kada se koristi koncentrirana dušična kiselina, nastaje 2,4,6-trinitrofenol (pikrinska kiselina):
 pikrinska kiselina
pikrinska kiselina
3) Reakcije sulfoniranja
Fenol se lako sulfonira na sobnoj temperaturi s koncentriranom sumpornom kiselinom kako bi se formirao orto izomer, koji se na temperaturama iznad 100 0 C preuređuje u para izomer:

4) Reakcije alkilacije
Fenoli lako prolaze kroz reakcije alkilacije.
Haloalkani, alkanoli i alkeni se koriste kao alkilirajuća sredstva u prisustvu protonskih kiselina (H 2 SO 4, H 3 PO 4) ili Lewisovih kiselina (AlCl 3, BF 3): 

5) Reakcije acilacije
Acilacija fenola se lako odvija pod dejstvom halogenih anhidrida ili anhidrida karboksilne kiseline u prisustvu Lewisovih kiselina: 
6) Reakcije nitrozacije
Nitrozofenoli se dobijaju direktnom nitrozacijom fenola:

para-krezol orto-nitrozo-para-krezol
7) Reakcije azo kuplovanja
Kombinacija sa fenolima dovodi do blago alkalna sredina, budući da je fenolat ion mnogo aktivniji od samog fenola:

8) Reakcije kondenzacije
Fenoli su tako aktivne komponente u reakcijama elektrofilne supstitucije da stupaju u interakciju sa vrlo slabim elektrofilima - aldehidima i ketonima u prisustvu kiselina i baza.
Kondenzacija sa formaldehidom
Formaldehid najlakše ulazi u reakcije kondenzacije.
Ako se reakcija kondenzacije fenola sa formaldehidom odvija u blagim uslovima, moguće je izolovati orto- i para-hidroksimetilfenole: Pojedinačni predstavnici
fenol– kristalna supstanca sa t.t. 43°C, ima karakterističan oštar miris, izaziva opekotine na koži. Ovo je jedan od prvih antiseptika koji se koristi u medicini. Koristi se u velikim količinama za proizvodnju plastike (kondenzacija sa formaldehidom), lijekova (salicilna kiselina i njeni derivati), bojila, eksploziva (pikrinska kiselina).
fenol metil etar – anisol– koristi se za proizvodnju aromatičnih supstanci i boja.
fenol etil etar - fenetol.
krezoli (metilfenoli) koristi se u proizvodnji plastike, boja i dezinficijensa.
Fenolni hidroksil je hidroksil povezan sa aromatičnim prstenom.
1. Kiselinsko-bazna svojstva su posljedica prisustva mobilnog atoma vodika u fenolnom hidroksilu. Elektronski par hidroksila je pomeren prema aromatičnom prstenu, pa su kisela svojstva jača od alkohola. Dakle, pKa ugljene kiseline = 6,35, a pKa fenola = 9,89.
Fenoli se otapaju u vodenim rastvorima alkalija i formiraju fenolate (fenokside):
Međutim, kisela priroda fenola izražena je tako beznačajno da čak i tako slaba kiselina kao što je ugljična kiselina istiskuje fenole iz njihovih soli:
Stoga se fenoli, rastvarajući se u alkalijama, ne mogu rastvoriti u karbonatima, jer ugljična kiselina oslobođena u ovom slučaju odmah razgrađuje fenolat:
Ovo svojstvo fenola razlikuje ih od karboksilnih kiselina.
Kako temperatura raste, reakcija se odvija u smjeru naprijed. Fenolati alkalnih metala, kao soli jakih baza i slabih kiselina, djelomično se hidroliziraju u vodenim otopinama, pa otopine fenolata imaju alkalnu reakciju.
2. Reakcija esterifikacije (slično alkoholnom hidroksilu).
Stvaranje etera je reakcija fenolata i alkil halogenida (ili alkil sulfata).
C 6 H 5 ONa+JCH 3 ®C 6 H 5 OCH 3 +NaJ
Esteri nastaju reakcijom natrijum fenolata sa anhidridima (ili kiselim hloridima).
3. Redox svojstva.
Fenoli pokazuju jaka redukcijska svojstva i vrlo se lako oksidiraju čak i slabim oksidantima, što rezultira stvaranjem obojenih spojeva hinoidne strukture.
 | [O] – CaOCl 2, H 2 O 2, Cl 2, Br 2 |
Primjer oksidacijske reakcije je stvaranje indofenolne boje: nastali kinon, nakon interakcije s NH 3, pretvara se u kinon imin, koji reagira s neizreagiranim fenolom. U prisustvu amonijaka nastaje indofenol, obojen u plavo.

kinoneimin indofenol
n- benzohinonimin
Vrsta indofenolne reakcije je Liebermanova nitrozo reakcija, koja je karakteristična za one fenole u kojima nema supstituenata na orto i para pozicijama.
Kada je izložen natrijum nitritu u kiseloj sredini, formira se n-nitrozofenol, izomerizirajući u monooksim n-benzohinon, koji zatim reaguje sa viškom fenola u kiseloj sredini dajući indofenol.

Uočava se boja koja se mijenja kada se doda alkalna otopina:
fenol – tamnozeleni, koji prelazi u trešnja crveno;
timol – plavo-zelen, postaje ljubičasti;
resorcinol – ljubičasto-crni, koji prelazi u ljubičastu;
heksestrol (sinestrol) – crveno-ljubičasta, koja se pretvara u trešnju.
4. Reakcija kompleksiranja s ionima željeza.
U zavisnosti od količine fenolnih hidroksila, prisutnosti drugih funkcionalnih grupa u molekuli, njihovog relativnog položaja, pH okoline i temperature, nastaju kompleksna jedinjenja različitog sastava i boja (sa izuzetkom timola).



Kompleksi su obojeni:
fenol – plava boja;
resorcinol – plavo-ljubičasta boja;
salicilna kiselina – plavo-ljubičasta ili crveno-ljubičasta boja;
osalmid (oksafenamid) – crveno-ljubičasta boja;
natrijum para-aminosalicilat – crveno-ljubičasta boja;
quinosol – plavkasto-zelene boje.
Reakcija je farmakopejska za većinu fenolnih spojeva.
5. Reakcije elektrofilne supstitucije – SE atoma vodika u aromatičnom prstenu (bromovanje, kondenzacija sa aldehidima, kombinacija sa diazonijum solima, nitriranje, nitrozacija, jodiranje itd.). Sposobnost fenola da uđu u reakcije elektrofilne supstitucije objašnjava se interakcijom usamljenog elektronskog para atoma kiseonika sa π-elektronima benzenskog prstena. Gustoća elektrona se pomera prema aromatičnom prstenu. Najveći višak elektronske gustoće se opaža kod atoma ugljika u O- I n- pozicije u odnosu na fenolni hidroksil (orijentacija tipa I).
5.1. Reakcija halogeniranja (bromiranje i jodiranje).
5.1.1. U interakciji s bromnom vodom nastaju bijeli ili žuti talozi derivata broma.

Kada postoji višak broma, dolazi do oksidacije:

Reakcija bromiranja fenola ovisi o prirodi i položaju supstituenata.
Jodizacija se događa slično, na primjer:

5.1.2. Ako postoje supstituenti u O- I n- pozicije aromatičnog prstena, nesupstituisani atomi vodika aromatičnog prstena reaguju.

5.1.3. Ako u O- I n- pozicijama u odnosu na fenolni hidroksil postoji karboksilna grupa, tada pod dejstvom viška broma dolazi do dekarboksilacije:

5.1.4. Ako spoj sadrži dva fenolna hidroksila u m- položaj, tada pod dejstvom broma nastaju tribromo derivati (konzistentna orijentacija):

5.1.5. Ako su dvije hidroksilne grupe locirane jedna u odnosu na drugu u O- ili n- pozicije, tada se reakcija bromiranja ne javlja (nekonzistentna orijentacija)

5.2. Reakcije kondenzacije
5.2.1. Sa aldehidima.
Primjer kondenzacije fenola s aldehidima je reakcija s Marquisovim reagensom. Kada se fenoli zagrijavaju otopinom formaldehida u prisustvu koncentrirane H 2 SO 4, nastaju bezbojni produkti kondenzacije, čijom oksidacijom nastaju intenzivno obojena jedinjenja kinoidne strukture. Sumporna kiselina u ovoj reakciji igra ulogu dehidracije, kondenzacije i oksidacije.

5.2.2. Reakcija fenola sa hloroformom (CHCl 3) za stvaranje aurinskih boja.
Kada se fenoli zagrevaju sa CHCl 3 u alkalnoj sredini, aurine– trifenilmetanske boje:

Aurine su obojene:
fenol – žuta boja;
timol – žuta boja koja prelazi u ljubičastu;
resorcinol – crveno-ljubičasta boja.
5.2.3. Sa anhidridima kiselina.
A. Reakcija stvaranja fluoresceina (kondenzacija resorcinola sa ftalnim anhidridom).


B. Reakcija stvaranja fenolftaleina (kondenzacija fenola sa ftalnim anhidridom).

S velikim viškom alkalija nastaje trosupstituirana natrijeva sol.
Kondenzacija timola sa ftalnim anhidridom se odvija slično reakciji stvaranja fenolftaleina, koji ima plavu boju u alkalnom mediju.
5.3. Reakcija nitracije
Fenoli reagiraju s razrijeđenom dušičnom kiselinom (HNO 3) i formiraju orto- i para-nitro derivate. Dodavanje otopine natrijum hidroksida pojačava boju zbog stvaranja dobro disocirane soli.

5.4. Reakcija azo kuplovanja fenola sa diazonijum soli u alkalnoj sredini.
Kada fenoli reaguju sa diazonijum soli pri pH 9-10, nastaju azo boje, obojene u žuto-narandžastu ili crvenu boju. Reakcija azo spajanja se javlja u orto i para pozicijama u odnosu na fenolni hidroksil. Diazotizirana sulfanilna kiselina se obično koristi kao diazo reagens.


Uvod
Većina lijekova koji se koriste u medicinskoj praksi su organska jedinjenja. Identitet takvih supstanci potvrđuje se reakcijama na funkcionalne grupe.
Funkcionalna grupa je reaktivni atom, grupa atoma ili reakcioni centar u molekulu organskog jedinjenja.
Opći princip funkcionalne analize je korištenje karakterističnih reakcija za grupe koje treba odrediti. Reakcija ne samo da mora biti što je moguće specifičnija, već i dovoljno brza, i mora uključivati reaktant ili proizvod reakcije koji se lako može otkriti.

Identifikacija alkoholnog hidroksila
Alkoholi - To su derivati ugljikovodika, u čijim je molekulima jedan ili više atoma vodika zamijenjeno hidroksilnim grupama. Generalno, molekul alkohola se može predstaviti kao ROH.
Reakcija formiranja estera
Alkoholi formiraju estere s organskim kiselinama ili anhidridima kiselina u prisustvu sredstava za uklanjanje vode (na primjer, koncentrovane sumporne kiseline). Esteri dobijeni od alkohola niske molekularne mase imaju karakterističan miris, a estri na bazi alkohola visoke molekulske mase su kristalne supstance sa jasnom tačkom topljenja.
Metodologija. U 1 ml etanola dodajte 5 kapi glacijalne octene kiseline, 0,5 ml koncentrovane sumporne kiseline i pažljivo zagrijte; detektuje se karakterističan miris etil acetata (svježe jabuke).

Reakcija oksidacije alkohola u aldehide
Nastali aldehidi se detektuju mirisom. Kao oksidanti koriste se kalijum heksacijano-(III)-ferat, kalijum permanganat, kalijum dihromat itd.
Metodologija. U prvu epruvetu stavite 2 kapi etanola, 1 kap 10% rastvora sumporne kiseline i 2 kapi 10% rastvora kalij-dihromata. Rezultirajuće rješenje ima narandžasta boja. Zagrijte ga na vatri dok otopina ne počne stjecati plavkasto-zelene boje(istovremeno se osjeća karakterističan miris acetaldehida, koji podsjeća na miris Antonovskih jabuka). Dodajte 1 kap dobijenog rastvora u drugu epruvetu sa 3 kapi fuksinsumporne kiseline. Pojavljuje se roze-ljubičaste boje.
Reakcija stvaranja kompleksnih spojeva
Polihidrični alkoholi formiraju plava kompleksna jedinjenja sa bakar sulfatom u alkalnoj sredini (sa Felingovim reagensom).
Metodologija. U 0,5 ml glicerina dodati 5 kapi rastvora natrijum hidroksida i bakar (II) sulfata, intenzivnog plavo bojenje.

Identifikacija fenolnog hidroksila
Reakcija sa željeznim (111) hloridom
Karakteristična kvalitativna reakcija na fenole je reakcija sa gvožđe (III) hloridom. U zavisnosti od količine fenolnih hidroksila, prisutnosti drugih funkcionalnih grupa u molekulu fenola, njihovog relativnog položaja, pH okoline i temperature nastaju kompleksna jedinjenja različitog sastava i boja.
Metodologija. U 0,01 g lijeka rastvorenog u 1 ml vode (za fenol, resorcinol) dodajte 2 kapi rastvora gvožđe (III) hlorida - primećuje se karakteristična boja (tabela 1).
Tabela 1. Bojenje kompleksa preparata gvožđe (III) hloridom
|
Droga |
Solvent |
Bojanje kompleksa |
|
Ljubičasta |
||
|
Resorcinol |
Plavo-ljubičasta |
|
|
Adrenalin hidrohlorid |
Smaragdno zelena, prelazeći od dodavanja jedne kapi rastvora amonijaka u trešnje crvenu, a zatim narandžasto crvenu. |
|
|
Morfin hidrohlorid |
Plava, koja nestaje dodatkom razrijeđene octene ili hlorovodonične kiseline |
|
|
Paracetamol |
Plavo-ljubičasta |
|
|
Piridoksin hidrohlorid |
Crvena, nestaje dodatkom razrijeđene klorovodične kiseline i ne nestaje s razrijeđenom octenom kiselinom. |
|
|
Salicilna kiselina i natrijum salicilat |
plavo-ljubičasta, ne nestaje dodatkom nekoliko kapi razrijeđene hlorovodonične ili octene kiseline. |
|
|
Fenil salicilat |
ljubičasta, nestaju dodavanjem razrijeđene hlorovodonične ili octene kiseline i pretvaraju se u krvavo crvena dodavanjem 1-2 kapi rastvora amonijaka. |
Koristeći otopinu amonijaka, možete razlikovati fenol od resorcinola. Boja kompleksa rezorcinola sa gvožđem se nakon dodavanja reagensa menja u smeđe žute boje.